L’1-pentanolo è un alcol liquido incolore con cinque atomi di carbonio. È utilizzato come solvente e intermedio nella sintesi chimica e ha varie applicazioni industriali.
| Nome IUPAC | Pentan-1-olo |
| Formula molecolare | C₅H₁₁OH |
| numero CAS | 71-41-0 |
| Sinonimi | Alcool amilico, alcol n-amilico, 1-idrossipentano, alcol n-pentilico, pentanolo, alcol pentilico |
| InChI | InChI=1S/C5H12O/c1-2-3-4-5-6/h6H,2-5H2,1H3 |
Proprietà dell’1-pentanolo
Formula 1-pentanolo
La formula del pentanolo è C₅H₁₁OH. È costituito da cinque atomi di carbonio, undici atomi di idrogeno e un gruppo ossidrile (-OH). La formula rappresenta la disposizione specifica e i tipi di atomi in una molecola di pentanolo.
Massa molare 1-pentanolo
La massa molare del pentanolo si calcola sommando le masse atomiche dei suoi atomi costituenti. La massa molare del pentanolo è di circa 88,15 grammi per mole (g/mol). Fornisce informazioni sulla massa di una mole di molecole di pentanolo.
Punto di ebollizione dell’1-pentanolo
Il pentanolo ha un punto di ebollizione di circa 138 gradi Celsius (280 gradi Fahrenheit). A questa temperatura il pentanolo liquido si trasforma allo stato gassoso. Il punto di ebollizione indica la temperatura alla quale una sostanza passa dalla fase liquida a quella gassosa.
Punto di fusione del 1-pentanolo
Il punto di fusione del pentanolo è di circa -79 gradi Celsius (-110 gradi Fahrenheit). Questa è la temperatura alla quale il pentanolo solido si trasforma nella sua forma liquida. Il punto di fusione rappresenta il passaggio dallo stato solido allo stato liquido.
Densità di 1-pentanolo g/mL
La densità del pentanolo è di circa 0,81 grammi per millilitro (g/mL). La densità è la misura della massa per unità di volume. Ciò indica quanto strettamente sono imballate le molecole di una sostanza.
Peso molecolare dell’1-pentanolo
Il peso molecolare dell’1-pentanolo è di circa 88,15 grammi per mole (g/mol). È la somma dei pesi atomici di tutti gli atomi di una molecola. Il peso molecolare viene utilizzato in vari calcoli, come determinare il numero di moli o la massa di una sostanza.
Struttura dell’1-pentanolo
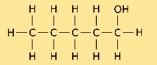
La struttura del pentanolo è costituita da una catena lineare di cinque atomi di carbonio, con un gruppo ossidrile (-OH) attaccato ad un’estremità. Ha la formula chimica CH₃(CH₂)₃CH₂OH. La struttura del pentanolo gioca un ruolo cruciale nel determinare le sue proprietà fisiche e chimiche.
Solubilità dell’1-pentanolo
Il pentanolo è solubile in solventi organici, come etere e acetone, ma ha una solubilità limitata in acqua. Forma legami idrogeno con le molecole d’acqua a causa della presenza del gruppo ossidrile. La solubilità del pentanolo influenza il suo comportamento in diversi ambienti.
| Aspetto | Liquido incolore |
| Peso specifico | 0,809-0,814 g/ml |
| Colore | Incolore |
| Odore | Odore caratteristico |
| Massa molare | 88,15 g/mole |
| Densità | 0,81 g/ml |
| Punto di fusione | -79°C (-110°F) |
| Punto di ebollizione | 138°C (280°F) |
| Punto flash | 54°C (129°F) |
| solubilità in acqua | Leggermente solubile |
| Solubilità | Solubile in solventi organici come etere e acetone |
| Pressione del vapore | 2,5 mmHg (25°C) |
| Densità del vapore | 3.0 (aria = 1) |
| pKa | 16.2 |
| pH | 6.5-8.5 |
1-Pentanolo Sicurezza e pericoli
Il pentanolo pone alcune considerazioni sulla sicurezza e sui rischi. Dovrebbe essere maneggiato con cautela a causa della sua natura infiammabile, con un punto di infiammabilità di 54°c (129°f). Evitare il contatto con fiamme libere o fonti di ignizione. L’inalazione di vapori di pentanolo può causare irritazione del sistema respiratorio. Il contatto diretto con la pelle può causare irritazione o secchezza della pelle. Se ingerito accidentalmente può causare disturbi gastrointestinali. È necessario mantenere una ventilazione adeguata quando si lavora con il pentanolo per ridurre al minimo l’esposizione ai vapori. Per garantire una manipolazione sicura, è necessario utilizzare dispositivi di protezione individuale, come guanti e occhiali di sicurezza. È importante rivedere la scheda dati di sicurezza e seguire i protocolli di sicurezza adeguati quando si lavora con il pentanolo.
| Simboli di pericolo | Infiammabile (F) |
| Descrizione della sicurezza | Tenere lontano da fonti di calore/scintille/fiamme libere/superfici calde. Utilizzare apparecchiature elettriche/di ventilazione/illuminazione a prova di esplosione. Evitare di respirare i vapori. Indossare guanti protettivi/proteggere gli occhi/il viso. |
| Numeri di identificazione delle Nazioni Unite | ONU 1105 |
| Codice SA | 2905.16.00 |
| Classe di pericolo | Classe 3 (Liquidi infiammabili) |
| Gruppo di imballaggio | GE II |
| Tossicità | Può causare irritazione. |
Metodi per la sintesi dell’1-pentanolo
Vari metodi consentono la sintesi del pentanolo.
Un metodo comune è l’idroformilazione dell’1-butene , che prevede la reazione dell’1-butene con monossido di carbonio e idrogeno in presenza di un catalizzatore di rodio. Questo processo porta alla formazione di una miscela di intermedi aldeidici, seguita dall’idrogenazione per produrre pentanolo.
Un altro metodo prevede la riduzione del pentanale, un composto aldeidico, utilizzando un agente riducente come il boroidruro di sodio . Questa reazione di riduzione converte il pentanale in pentanolo.
I chimici possono idratare l’1-pentene, un alchene, per produrre pentanolo. Questa reazione comporta l’aggiunta di acqua attraverso il doppio legame carbonio-carbonio dell’1-pentene, con conseguente formazione di pentanolo.
Inoltre, il pentanolo può essere sintetizzato idrogenando l’acido pentanoico, un acido carbossilico. La reazione avviene in presenza di un catalizzatore adatto, come palladio su carbonio e idrogeno gassoso, portando alla conversione dell’acido pentanoico in pentanolo.
Questi metodi di sintesi offrono percorsi diversi per ottenere il pentanolo, garantendo flessibilità di produzione a seconda delle materie prime disponibili e delle condizioni di reazione desiderate.
Usi dell’1-pentanolo
Il pentanolo ha vari usi in diversi settori grazie alle sue proprietà e versatilità. Ecco alcune delle sue applicazioni degne di nota:
- Solvente: il pentanolo funge da solvente in settori quali quello farmaceutico, dei rivestimenti e dei cosmetici, sciogliendo efficacemente molti composti organici. Svolge un ruolo cruciale nella formulazione di pitture, vernici e prodotti per la cura personale.
- Sintesi chimica: funge da importante intermedio nella sintesi di vari prodotti chimici. Può subire reazioni per produrre esteri, eteri e altri derivati, che trovano applicazioni nella produzione di profumi, aromi e ingredienti farmaceutici.
- Estrazione: nei processi di estrazione, il pentanolo viene utilizzato per separare alcuni composti dai prodotti naturali. Aiuta a estrarre sostanze preziose dai materiali vegetali, contribuendo così alla produzione di oli essenziali, profumi e aromi.
- Agente detergente: industrie come l’elettronica, l’ottica e la produzione di precisione utilizzano il pentanolo come detergente grazie alla sua capacità di dissolvere oli, grassi e altri contaminanti. Garantisce una pulizia profonda rimuovendo i residui dalle superfici.
- Additivo per carburante: in alcuni casi, il pentanolo viene utilizzato come additivo per carburante per migliorare l’efficienza della combustione e ridurre le emissioni. Migliora le prestazioni e l’impatto ambientale dei carburanti se miscelati con benzina o altri carburanti.
- Applicazioni industriali: il pentanolo viene utilizzato in vari processi industriali, tra cui la sverniciatura, lo sgrassaggio dei metalli e la pulizia industriale. Le sue proprietà lo rendono efficace nella rimozione di rivestimenti e contaminanti dalle superfici.
- Ricerca e laboratorio: il pentanolo è utilizzato come reagente o solvente nella ricerca scientifica e nei laboratori. Facilita reazioni, estrazioni e purificazioni in varie procedure sperimentali.
Le diverse applicazioni del pentanolo evidenziano la sua importanza in diversi settori, dove le sue proprietà uniche contribuiscono allo sviluppo di numerosi prodotti e processi.
Domande:
D: Quale dei seguenti è più solubile in acqua: acido acetico, pentanolo, acido butanoico o pentanale?
R: L’acido acetico è il più solubile in acqua tra i composti indicati.
D: Il pentanolo è solubile in acqua?
R: Il pentanolo ha una solubilità limitata in acqua.
D: Qual è la funzione del catalizzatore acido nel promuovere la disidratazione del 4-metil-2-pentanolo?
R: Il catalizzatore acido facilita la rimozione di una molecola d’acqua dal 4-metil-2-pentanolo, favorendone la disidratazione.
D: Quale prodotto si ottiene dalla reazione di acido solforico, acido acetico e 1-pentanolo?
R: La reazione tra acido solforico, acido acetico e pentanolo porta alla formazione di composti esterei.
D: Il pentanolo ha un legame idrogeno?
R: Sì, il pentanolo può mostrare legami idrogeno a causa della presenza del gruppo ossidrile.
D: Come preparare l’acido pentanoico dall’1-pentanolo?
R: L’acido pentanoico può essere ottenuto ossidando l’1-pentanolo utilizzando opportuni agenti ossidanti oppure idrolizzando il suo corrispondente estere.
D: Quale prodotto organico otterresti dalla reazione dell’1-pentanolo con CrO3, H2O e H2SO4?
R: La reazione dell’1-pentanolo con CrO3, H2O e H2SO4 dà luogo alla formazione del corrispondente acido carbossilico.
D: Cos’è meno solubile in acqua, 1-pentanolo o 1-eptanolo? Spiegare.
R: Il pentanolo è meno solubile in acqua dell’1-eptanolo a causa della sua catena idrocarburica più corta, con conseguenti interazioni più deboli con le molecole d’acqua.
D: Quale prodotto organico otterresti dalla reazione dell’1-pentanolo con PBr3?
R: La reazione del pentanolo con PBr3 porta alla sostituzione del gruppo ossidrile, con conseguente formazione di 1-bromopentano.
