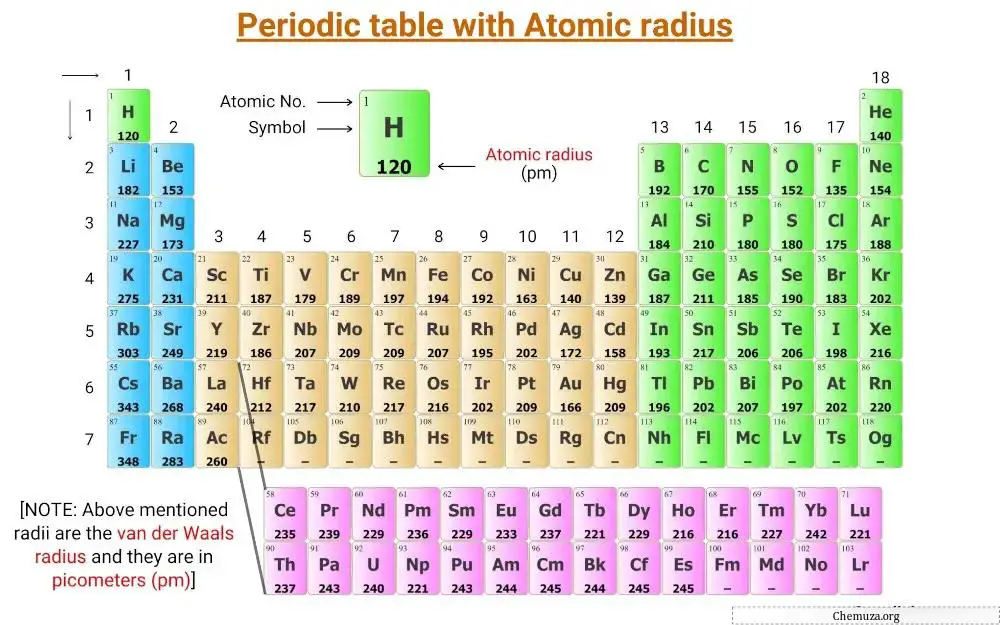
Ini adalah tabel periodik dengan nilai jari-jari atom unsur-unsur yang diberi label di atasnya.
Jari-jari yang disebutkan pada tabel periodik di atas adalah jari-jari van der Waals dan dinyatakan dalam pikometer (pm).
Nah, ada beberapa hal konseptual penting tentang jari-jari atom suatu unsur yang perlu Anda ketahui.
Jadi mari kita langsung ke sana.
Berapa jari-jari atom?
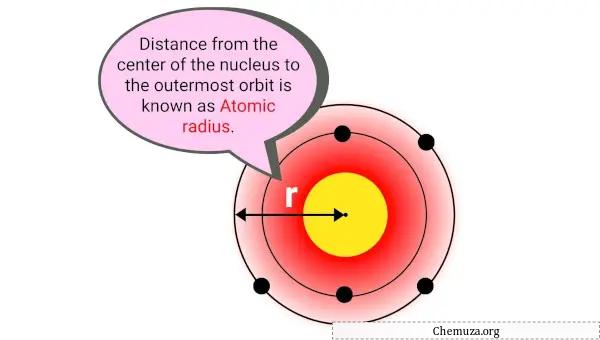
Jari-jari atom adalah jarak antara pusat inti atom dan elektron terluar dalam awan elektronnya.
Dalam istilah sederhana, ini adalah ukuran atom. Jari-jari atom biasanya diukur dalam pikometer (pm), atau sepertriliun meter.
Atom sangatlah kecil dan sulit untuk divisualisasikan, namun konsep jari-jari atom membantu kita memahami bagaimana atom berinteraksi satu sama lain dan bagaimana mereka berperilaku dalam berbagai reaksi kimia.
Ukuran suatu atom dapat mempengaruhi sifat kimianya , misalnya bagaimana ia berikatan dengan atom atau molekul lain.
Bagaimana cara mengukur jari-jari atom?
Jari-jari atom biasanya diukur menggunakan berbagai metode eksperimental seperti kristalografi sinar-X, difraksi elektron, dan spektroskopi.
Metode ini melibatkan mempelajari perilaku atom ketika berinteraksi dengan bentuk energi tertentu, seperti sinar-X atau elektron.
- Dalam kristalografi sinar-X , pancaran sinar-X ditujukan pada kristal unsur yang sedang dipelajari. Sinar-X mendifraksi atom-atom dalam kristal dan pola difraksi yang dihasilkan dapat digunakan untuk menentukan jarak antar atom dan jari-jarinya.
- Dalam difraksi elektron , seberkas elektron diarahkan ke lapisan tipis unsur yang sedang dipelajari. Ketika elektron melewati film, mereka menyebarkan atom, menciptakan pola difraksi yang dapat dianalisis untuk menentukan jari-jari atom.
- Spektroskopi melibatkan mempelajari interaksi antara cahaya dan materi. Dengan menganalisis panjang gelombang cahaya yang diserap atau dipancarkan oleh suatu atom, para ilmuwan dapat menentukan jari-jari atomnya.
Faktor-Faktor yang Mempengaruhi Jari-jari Atom
Besar kecilnya suatu atom dipengaruhi oleh berbagai faktor, antara lain:
- Muatan nuklir
- Konfigurasi elektronik
- Jarak elektron Valensi dari inti, dll.
Muatan nuklir
Jumlah proton dalam inti atom disebut nomor atom. [1]
Dengan bertambahnya nomor atom, jumlah proton dalam inti meningkat, sehingga muatan inti semakin besar.
Peningkatan muatan ini menarik elektron lebih kuat ke arah inti, sehingga jari-jari atom menjadi lebih kecil.
Konfigurasi elektronik
Cara elektron tersusun di sekitar inti atom menentukan konfigurasi elektroniknya. [2]
Semakin dekat elektron ke inti, semakin kecil jari-jari atomnya.
Atom dengan jumlah elektron lebih banyak pada tingkat energi terluarnya (kulit valensi) akan mempunyai jari-jari atom lebih besar, karena jarak elektron lebih jauh dan daya tariknya terhadap inti berkurang.
Jarak elektron Valensi dari inti
Jarak antara elektron valensi dan inti juga mempengaruhi jari-jari atom.
Ketika jumlah kulit elektron bertambah, elektron valensi menjauh dari inti, mengakibatkan peningkatan jari-jari atom.
Penting untuk dicatat bahwa faktor-faktor yang mempengaruhi jari-jari atom saling terkait. Misalnya, peningkatan muatan inti akan menghasilkan jari-jari atom yang lebih kecil, peningkatan jumlah elektron pada tingkat energi terluar (kulit valensi) akan menghasilkan jari-jari atom yang lebih besar. Oleh karena itu, ukuran keseluruhan atom dihasilkan dari keseimbangan antara faktor-faktor ini.
Untuk informasi lebih lanjut, Anda harus membaca tren jari-jari atom pada tabel periodik.
Ringkasan
Jari-jari atom adalah ukuran suatu atom, diukur dalam pikometer, dari pusat inti sampai elektron terluar pada awan elektron.
Ini membantu kita memahami bagaimana atom berinteraksi dan mempengaruhi sifat kimianya. Metode eksperimental, seperti kristalografi sinar-X, difraksi elektron, dan spektroskopi, digunakan untuk mengukur jari-jari atom.
Faktor-faktor yang mempengaruhi jari-jari atom adalah muatan inti, konfigurasi elektron, dan jarak antara elektron valensi dan inti. Faktor-faktor ini saling terkait dan menentukan ukuran keseluruhan suatu atom.
