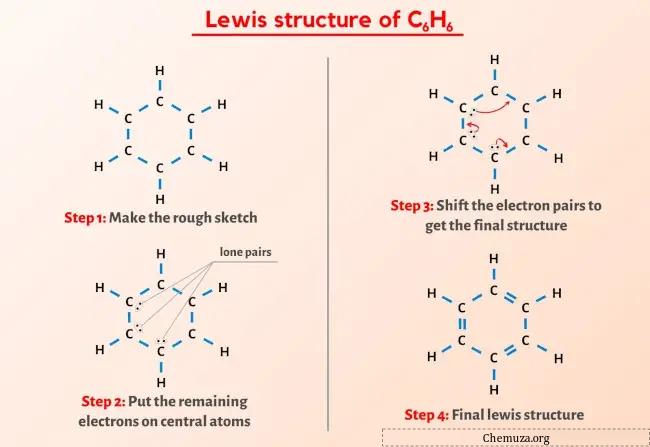
Jadi Anda sudah melihat gambar di atas kan?
Izinkan saya menjelaskan secara singkat gambar di atas.
Struktur Lewis C6H6 (benzena) memiliki 6 atom karbon (C) dalam struktur berbentuk cincin dan setiap atom karbon terikat pada 1 atom hidrogen (H). Terdapat ikatan rangkap berselang-seling pada struktur cincin karbon (C).
Jika Anda tidak memahami apa pun dari gambar struktur Lewis C6H6 di atas, tetaplah bersama saya dan Anda akan mendapatkan penjelasan rinci langkah demi langkah tentang cara menggambar struktur Lewis C6H6 .
Jadi mari kita lanjutkan ke langkah-langkah menggambar struktur Lewis C6H6 (benzena).
Langkah-langkah Menggambar Struktur Lewis C6H6
Langkah 1: Temukan jumlah total elektron valensi dalam molekul C6H6
Untuk mengetahui jumlah total elektron valensi dalam molekul C6H6, pertama-tama Anda perlu mengetahui elektron valensi yang ada dalam atom karbon dan juga atom hidrogen.
(Elektron valensi adalah elektron yang ada di orbit terluar atom mana pun.)
Disini saya akan memberi tahu Anda cara mudah mencari elektron valensi karbon dan hidrogen menggunakan tabel periodik.
Total elektron valensi dalam molekul C6H6
→ Elektron valensi diberikan oleh atom karbon:
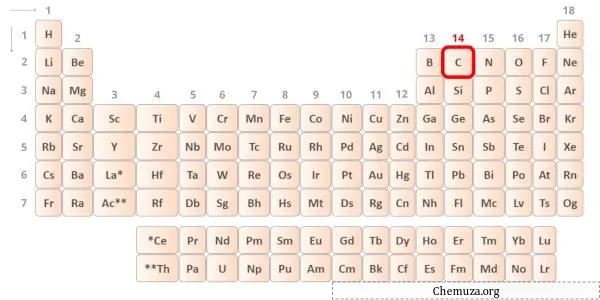
Karbon adalah unsur dalam golongan 14 tabel periodik. [1] Oleh karena itu, elektron valensi yang ada dalam karbon adalah 4 .
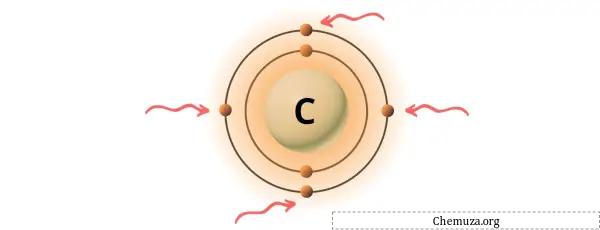
Anda dapat melihat 4 elektron valensi yang ada pada atom karbon seperti terlihat pada gambar di atas.
→ Elektron valensi diberikan oleh atom hidrogen:
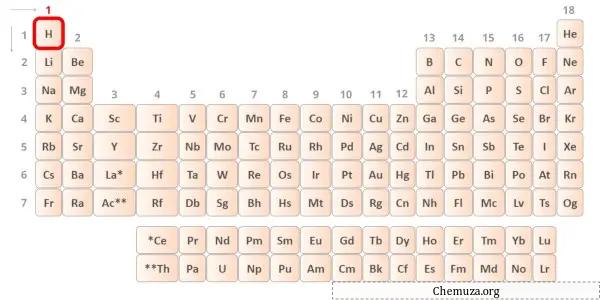
Hidrogen adalah unsur golongan 1 dalam tabel periodik. [2] Oleh karena itu, elektron valensi yang ada dalam hidrogen adalah 1 .

Anda dapat melihat bahwa hanya ada satu elektron valensi dalam atom hidrogen seperti yang ditunjukkan pada gambar di atas.
Jadi,
Jumlah elektron valensi dalam molekul C6H6 = elektron valensi yang disumbangkan oleh 6 atom karbon + elektron valensi yang disumbangkan oleh 6 atom hidrogen = 4(6) + 1(6) = 30 .
Langkah 2: Siapkan sketsa
Struktur Lewis benzena (C6H6) memiliki 6 atom karbon yang tersusun dalam struktur cincin.
Selain itu, masing-masing atom karbon ini terikat pada 1 atom hidrogen.
Jadi mari kita menggambar sketsa yang mewakili cincin dari 6 atom karbon dan atom hidrogen yang terikat pada masing-masing karbon.
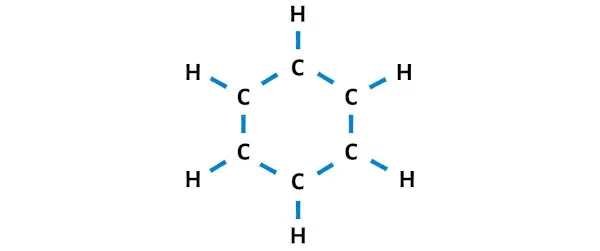
Ada 12 ikatan tunggal pada sketsa di atas. Jadi dari total 30 elektron valensi, 24 elektron valensi digunakan pada diagram di atas.
Langkah 3: Simpan sisa elektron pada atom pusat
Anda dapat melihat bahwa pada langkah 1 kita menghitung jumlah total elektron valensi yang ada dalam molekul C6H6.
Molekul C6H6 memiliki total 30 elektron valensi dan dari jumlah tersebut, hanya 24 elektron valensi yang digunakan pada diagram di atas.
Jadi jumlah elektron yang tersisa = 30 – 24 = 6 .
Anda perlu menempatkan 6 elektron ini (yaitu, 3 pasangan elektron ) pada atom karbon pada diagram molekul C6H6 di atas.
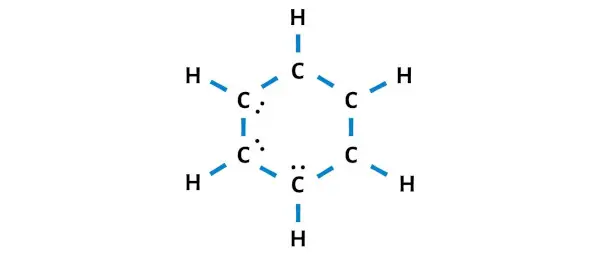
Sekarang mari kita lanjutkan ke langkah berikutnya.
Langkah 4: Jadikan Semua Atom Stabil
Dari sketsa di atas terlihat bahwa atom hidrogen terluar membentuk duplet . Oleh karena itu, mereka stabil.
Nah, dari 6 atom karbon, ketiga atom karbon tersebut tidak membentuk oktet .
Jadi kita perlu memindahkan pasangan elektron sedemikian rupa sehingga semua karbon membentuk oktet dan menjadi stabil.
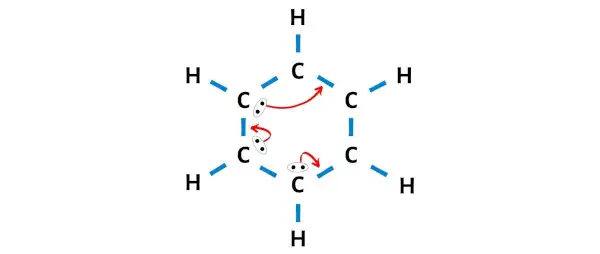
Setelah memindahkan pasangan elektron, Anda dapat melihat bahwa 6 atom karbon membentuk oktet dan sekarang stabil.
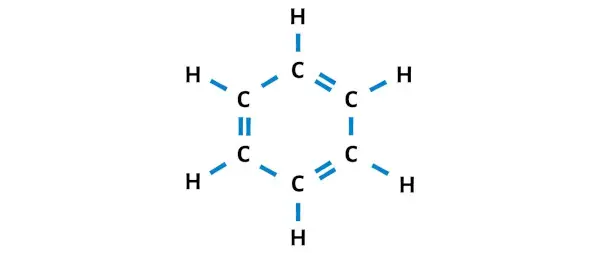
Oleh karena itu, ini adalah struktur Lewis benzena (atau C6H6) yang stabil.
Saya harap Anda telah memahami sepenuhnya semua langkah di atas.
Untuk lebih banyak latihan dan pemahaman yang lebih baik, Anda dapat mencoba struktur Lewis lainnya yang tercantum di bawah.
Cobalah (atau setidaknya lihat) struktur Lewis ini untuk pemahaman yang lebih baik:
