Perak nitrat (AgNO3) adalah senyawa kimia yang tersusun dari perak, nitrogen, dan oksigen. Ini biasa digunakan dalam fotografi, kedokteran dan sebagai reagen laboratorium untuk berbagai reaksi.
| Nama IUPAC | Perak nitrat |
| Formula molekul | AgNO3 |
| nomor CAS | 7761-88-8 |
| Sinonim | Perak mononitrat, perak (1+) garam asam nitrat, perak (I) nitrat |
| Di ChI | InChI=1S/Ag.NO3/c;2-1(3)4/q+1;-1 |
Sifat perak nitrat
Formula Perak Nitrat
Rumus perak mononitrat adalah AgNO3. Terdiri dari satu atom perak (Ag), satu atom nitrogen (N) dan tiga atom oksigen (O). Rumusnya mewakili rasio atom dalam molekul perak mononitrat.
Massa Molar Perak Nitrat
Massa molar perak mononitrat dihitung dengan menjumlahkan massa atom unsur penyusunnya. Perak memiliki massa atom 107,87 g/mol, nitrogen memiliki massa 14,01 g/mol, dan setiap atom oksigen memiliki massa 16,00 g/mol. Penambahannya menghasilkan massa molar sekitar 169,87 g/mol untuk perak mononitrat.
Titik didih perak nitrat
Perak mononitrat memiliki titik didih sekitar 440 derajat Celcius (824 derajat Fahrenheit). Pada suhu ini, senyawa mengalami transisi fasa dari wujud cair ke wujud gas. Titik didih menunjukkan suhu dimana tekanan uap suatu zat sama dengan tekanan atmosfer.
Perak nitrat Titik lebur
Titik leleh perak mononitrat kira-kira 209 derajat Celcius (408 derajat Fahrenheit). Ini adalah suhu di mana bentuk padat perak mononitrat berubah menjadi cair. Titik leleh adalah sifat khas suatu zat dan membantu menentukan perilaku fisiknya dalam berbagai kondisi.
Massa jenis perak nitrat g/mL
Kepadatan perak mononitrat kira-kira 4,35 g/mL. Kepadatan adalah ukuran jumlah massa yang terkandung dalam volume tertentu. Dihitung dengan membagi massa suatu zat dengan volumenya. Kepadatan perak mononitrat menunjukkan seberapa padatnya atau seberapa terkonsentrasinya dalam ruang tertentu.
Berat Molekul Perak Nitrat
Berat molekul perak mononitrat, juga disebut massa molar, adalah sekitar 169,87 g/mol. Ini mewakili jumlah massa atom semua atom dalam molekul perak mononitrat. Berat molekul digunakan dalam berbagai perhitungan dan konversi yang melibatkan jumlah senyawa.
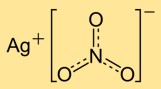
Struktur perak nitrat
Perak mononitrat memiliki struktur kristal yang tersusun dari kation perak (Ag+) dan anion nitrat (NO3-). Ion perak dikelilingi oleh ion nitrat, membentuk jaringan teratur. Struktur ionik ini berkontribusi terhadap stabilitas dan sifat senyawa.
Kelarutan perak nitrat
Perak mononitrat sangat larut dalam air. Ini mudah larut dalam air untuk membentuk larutan bening dan tidak berwarna. Kelarutan perak mononitrat dalam air merupakan karakteristik penting dan memainkan peran penting dalam berbagai aplikasi, seperti dalam bidang kedokteran, fotografi, dan reaksi kimia.
| Penampilan | Padatan kristal putih |
| Berat jenis | 4,35 gram/ml |
| Warna | Tanpa warna |
| Bau | Tidak berbau |
| Masa molar | 169,87 g/mol |
| Kepadatan | 4,35 gram/ml |
| Titik fusi | 209°C (408°F) |
| Titik didih | 440°C (824°F) |
| Titik kilat | Tak dapat diterapkan |
| Kelarutan dalam air | Larut |
| Kelarutan | Larut dalam air dan pelarut organik seperti etanol |
| Tekanan uap | 0,26 mmHg pada 25°C (77°F) |
| Kepadatan uap | Tak dapat diterapkan |
| pKa | – |
| pH | Asam (kira-kira pH 5-6 dalam larutan air) |
Keamanan dan Bahaya Perak Nitrat
Perak mononitrat menimbulkan beberapa risiko keselamatan dan kehati-hatian harus dilakukan saat menangani senyawa tersebut. Ini dianggap berbahaya jika tertelan, terhirup, atau jika terkena kulit atau mata. Tindakan perlindungan seperti sarung tangan, kacamata pengaman dan jas lab harus digunakan. Hal ini dapat menyebabkan iritasi, luka bakar dan noda pada kulit dan permukaan lainnya. Saat dipanaskan, ia dapat melepaskan nitrogen oksida beracun. Itu harus disimpan di tempat sejuk dan kering, jauh dari bahan yang tidak kompatibel. Tumpahan harus segera dibersihkan dan pembuangan limbah harus mengikuti pedoman yang tepat untuk menghindari kontaminasi terhadap lingkungan.
| Simbol bahaya | Korosif, Pengoksidasi |
| Deskripsi Keamanan | Menyebabkan luka bakar kulit yang parah dan kerusakan mata. |
| Pengidentifikasi PBB | UN 1493 (Perak mononitrat padat) |
| kode HS | 2843.10.00 |
| Kelas bahaya | Kelas 5.1 (Bahan pengoksidasi) |
| Kelompok pengepakan | GE II (menengah) |
| Toksisitas | Beracun bagi kehidupan akuatik dengan efek jangka panjang. |
Metode sintesis perak nitrat
Ada beberapa metode berbeda untuk mensintesis perak mononitrat.
Metode yang umum melibatkan reaksi antara perak metalik dan asam nitrat . Dalam proses ini, asam nitrat encer melarutkan perak untuk menghasilkan perak mononitrat. Metode lain melibatkan reaksi perak oksida atau perak karbonat dengan asam nitrat, menghasilkan pembentukan perak mononitrat.
Selain itu, reaksi antara perak klorida dan asam nitrat juga dapat menghasilkan perak mononitrat. Asam nitrat melarutkan perak klorida, menggantikan ion klorida dan membentuk perak mononitrat.
Selain itu, reaksi perak sulfat dengan garam nitrat yang larut, seperti natrium nitrat, memungkinkan perolehan perak mononitrat. Perak sulfat bereaksi dengan garam nitrat dalam larutan berair, menghasilkan pembentukan perak mononitrat dan garam sulfat yang larut.
Saat menerapkan metode sintetik ini, penting untuk mengambil tindakan pencegahan keselamatan yang tepat dan menggunakan asam korosif dan senyawa yang berpotensi beracun. Protokol dan pedoman laboratorium juga harus diikuti untuk memastikan persiapan dan penanganan perak mononitrat yang akurat.
Kegunaan perak nitrat
Perak mononitrat memiliki banyak kegunaan di berbagai bidang. Berikut beberapa aplikasi umum:
- Fotografi: Fotografi hitam putih tradisional menggunakan perak mononitrat sebagai senyawa peka cahaya yang bereaksi dengan cahaya, membentuk partikel perak dan mengembangkan gambar fotografi.
- Kedokteran: Aplikasi medis menggunakan perak mononitrat karena sifat antiseptiknya dalam perawatan luka. Aplikasi topikalnya mencegah infeksi, merangsang penyembuhan dan mengobati luka bakar, bisul dan luka kulit lainnya.
- Reagen Laboratorium: Perak mononitrat berfungsi sebagai reagen laboratorium serbaguna, memungkinkan berbagai reaksi kimia dan digunakan dalam kimia analitik untuk mendeteksi keberadaan halida dan senyawa lainnya.
- Pelapisan Perak: Proses pelapisan listrik menggunakan perak mononitrat untuk secara aktif menyimpan lapisan tipis perak ke berbagai permukaan. Penggunaan ini umum untuk tujuan dekoratif dan untuk memberikan ketahanan terhadap korosi.
- Pewarnaan dan Pewarnaan: Histologi dan mikroskop menggunakan perak mononitrat sebagai pewarna untuk secara aktif meningkatkan visibilitas struktur tertentu dalam sampel biologis. Industri tekstil menggunakannya untuk mewarnai kain.
- Ukiran: Sifat korosif dari perak mononitrat memungkinkan penggunaan aktifnya dalam pola etsa pada kaca dan cermin. Ini secara selektif menghilangkan lapisan permukaan, menciptakan pola yang rumit.
- Pendidikan Kimia: Institusi pendidikan secara aktif menggunakan perak mononitrat untuk melakukan eksperimen dan demonstrasi kimia, karena reaksi dan efek visualnya yang berbeda.
- Katalis Perak: Dalam beberapa reaksi kimia, perak mononitrat bertindak aktif sebagai katalis, memfasilitasi konversi reaktan menjadi produk yang diinginkan.
Pertanyaan:
Q: Apakah AgNO3 larut dalam air?
A: Ya, AgNO3 larut dalam air.
T: Apa itu AgNO3?
A: AgNO3 adalah perak mononitrat, senyawa kimia yang tersusun dari perak, nitrogen, dan oksigen.
Q: Apa yang dimaksud dengan ion penonton pada reaksi antara KCl(aq) dan AgNO3(aq)?
A: Pada reaksi antara KCl(aq) dan AgNO3(aq), ion pengamatnya adalah K+ dan NO3-.
Q: Ion manakah, jika ada, yang merupakan ion penonton dalam reaksi AgNO3(aq) + NaCl(aq) → AgCl(s) + NaNO3(aq)?
A: Pada reaksi AgNO3(aq) + NaCl(aq) → AgCl(s) + NaNO3(aq), ion pengamatnya adalah Na+ dan NO3-.
Q: Berapa mol Cu yang diperlukan untuk bereaksi dengan 5,8 mol AgNO3?
A: Persamaan setara diperlukan untuk menentukan jumlah mol Cu yang diperlukan untuk bereaksi dengan 5,8 mol AgNO3.
Q: Senyawa manakah berikut yang akan menghasilkan endapan dengan AgNO3?
A: Senyawa yang mengandung ion Cl-, Br- atau I- akan menghasilkan endapan dengan AgNO3.
Q: Apakah AgNO3 merupakan senyawa ionik?
A: Ya, AgNO3 merupakan senyawa ionik.
Q: Apakah AgNO3 merupakan elektrolit kuat?
J: Ya, AgNO3 adalah elektrolit yang kuat.
Q: Apakah AgNO3 dapat menghantarkan listrik?
A: Ya, AgNO3 dapat menghantarkan listrik jika dilarutkan dalam air.
T: Apakah perak nitrat termasuk garam?
A: Ya, perak mononitrat adalah garam.
T: Bisakah saya membeli perak nitrat?
J: Ya, perak mononitrat tersedia secara komersial untuk dibeli.
T: Apakah perak nitrat merupakan larutan?
A: Perak mononitrat dapat berbentuk padat atau larutan, bergantung pada kondisinya.
T: Bagaimana cara menghilangkan noda perak nitrat?
J: Noda perak mononitrat dapat dihilangkan dengan merawat area yang terkena dengan bahan pereduksi ringan, seperti hidrogen peroksida atau natrium tiosulfat.
Q: Apakah perak nitrat larut dalam air?
A: Ya, perak mononitrat larut dalam air.
Q: Endapan apa yang terbentuk jika larutan perak nitrat dan kalium kromat dicampur?
A: Ketika larutan perak mononitrat dan kalium kromat dicampur, terbentuk endapan kuning perak kromat (Ag2CrO4).
Q: Berapa massa molar perak nitrat?
A: Massa molar perak mononitrat (AgNO3) kira-kira 169,87 g/mol.
Q: Perak metalik ditambahkan ke dalam larutan timbal(II) nitrat. Apa yang dimaksud dengan reaksi kimia seimbang?
A: Reaksi kimia yang seimbang adalah 2Ag + Pb(NO3)2 → 2AgNO3 + Pb.
