Nikel karbonat (NiCO3) terbentuk dari ion nikel dan ion karbonat. Ini adalah padatan hijau yang digunakan dalam keramik dan katalis karena sifatnya yang unik.
| Nama IUPAC | Nikel(II) karbonat |
| Formula molekul | NiCO3 |
| nomor CAS | 3333-67-3 |
| Sinonim | Nikel karbonat; Asam karbonat, garam nikel, nikel monokarbonat |
| Di ChI | InChI=1S/CH2O3.Ni/c2-1(3)4;/h(H2,2,3,4);/q;+2 |
Sifat nikel karbonat
Formula Nikel Karbonat
Rumus kimia nikel monokarbonat adalah NiCO3. Terdiri dari satu atom nikel (Ni), satu atom karbon (C), dan tiga atom oksigen (O).
Massa Molar Nikel Karbonat
Massa molar nikel monokarbonat (NiCO3) kira-kira 118,7 gram per mol. Nilai ini diperoleh dengan menjumlahkan massa atom unsur-unsur penyusunnya.
Titik didih nikel karbonat
Nikel monokarbonat tidak memiliki titik didih yang jelas karena cenderung terurai sebelum mencapai titik didih. Ketika dipanaskan, ia terurai menjadi nikel oksida, karbon dioksida dan oksigen.
Titik Leleh Nikel Karbonat
Nikel monokarbonat memiliki titik leleh sekitar 200°C (392°F). Pada suhu ini, wujudnya berubah dari padat menjadi cair.
Massa jenis nikel karbonat g/mL
Massa jenis nikel monokarbonat kira-kira 3,6 gram per sentimeter kubik (g/cm³). Nilai massa jenis ini menunjukkan massa senyawa per satuan volume.
Berat Molekul Nikel Karbonat
Berat molekul nikel monokarbonat (NiCO3) kira-kira 118,7 gram per mol. Itu dihitung dengan menjumlahkan berat atom atom penyusunnya.
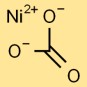
Struktur nikel karbonat
Nikel monokarbonat memiliki struktur dasar dimana atom nikel pusat terikat pada tiga atom oksigen dalam susunan segitiga. Ini membentuk inti ion karbonat. Strukturnya disatukan oleh ikatan ionik dan kovalen.
Kelarutan nikel karbonat
Nikel monokarbonat sulit larut dalam air. Kelarutannya meningkat seiring dengan menurunnya pH larutan. Ia juga dapat larut dalam larutan asam yang mengandung zat seperti asam klorida.
Sifat nikel monokarbonat membuatnya berguna dalam berbagai aplikasi. Ketidaklarutannya dalam air membuatnya cocok untuk aplikasi pada keramik dan pigmen. Penguraiannya pada suhu tinggi berkontribusi terhadap penggunaannya dalam proses katalitik.
| Penampilan | Hijau solid |
| Berat jenis | 3,6 gram/cm³ |
| Warna | Hijau |
| Bau | Tidak berbau |
| Masa molar | 118,7 g/mol |
| Kepadatan | 3,6 gram/cm³ |
| Titik fusi | 200°C (392°F) |
| Titik didih | Rusak sebelum direbus |
| Titik kilat | Tak dapat diterapkan |
| Kelarutan dalam air | Sulit larut |
| Kelarutan | Larut dalam asam seperti asam klorida |
| Tekanan uap | Tidak tersedia |
| Kepadatan uap | Tidak tersedia |
| pKa | Tak dapat diterapkan |
| pH | Tak dapat diterapkan |
Keamanan dan Bahaya Nikel Karbonat
Nikel monokarbonat mempunyai potensi risiko keselamatan. Ini dapat mengiritasi kulit dan mata jika terkena, menyebabkan kemerahan dan ketidaknyamanan. Menghirup debu atau uapnya dapat menyebabkan iritasi saluran pernafasan atau batuk. Dianjurkan untuk menanganinya dengan hati-hati, memakai alat pelindung yang sesuai seperti sarung tangan dan kacamata. Hindari menelan atau menghirup senyawa tersebut. Jika terpapar, cuci area yang terkena dampak dan dapatkan bantuan medis jika gejalanya berlanjut. Ventilasi dan tindakan pengendalian yang memadai sangat penting untuk meminimalkan risiko. Mengikuti protokol keselamatan saat bekerja dengan nikel monokarbonat sangat penting untuk mencegah potensi masalah kesehatan dan memastikan lingkungan yang aman.
| Simbol bahaya | Iritasi, Bahaya kesehatan |
| Deskripsi Keamanan | Mengiritasi; Hindari kontak dan penghirupan; Tangani dengan hati-hati |
| Nomor identifikasi PBB | Tidak diatribusikan |
| kode HS | 2836.40.00 |
| Kelas bahaya | Tidak diklasifikasikan |
| Kelompok pengepakan | Tidak diklasifikasikan |
| Toksisitas | Dapat menyebabkan iritasi kulit dan mata; iritasi pernapasan jika terhirup |
Metode sintesis nikel karbonat
Nikel monokarbonat dapat disintesis dengan berbagai metode. Pendekatan umum melibatkan reaksi antara garam nikel yang larut (seperti nikel klorida atau nikel sulfat ) dan garam karbonat yang larut (seperti natrium karbonat) dalam air. Kedua larutan tersebut dicampur sehingga menghasilkan pembentukan nikel monokarbonat yang tidak larut dalam bentuk endapan berwarna hijau. Endapan ini kemudian disaring, dicuci dan dikeringkan untuk mendapatkan produk akhir.
Metode lain melibatkan reaksi antara nikel oksida atau nikel hidroksida dan gas karbon dioksida dengan adanya uap air. Hal ini menghasilkan pembentukan nikel monokarbonat dengan air. Proses ini sering digunakan secara industri untuk menghasilkan nikel monokarbonat.
Selain itu, proses pengendapan dapat digunakan dengan mencampurkan larutan garam nikel larut dengan larutan garam karbonat larut. Campuran yang dihasilkan diaduk dan endapan nikel monokarbonat yang terbentuk dikumpulkan dan diolah.
Metode sintesis ini menghasilkan nikel monokarbonat untuk berbagai aplikasi seperti keramik, katalis, dan pigmen. Kontrol yang cermat terhadap kondisi reaksi dan langkah pemurnian sangat penting untuk mendapatkan produk nikel monokarbonat berkualitas tinggi.
Kegunaan Nikel Karbonat
Nikel monokarbonat menemukan berbagai aplikasi karena sifatnya yang unik. Beberapa kegunaan penting meliputi:
- Produksi Keramik dan Kaca: Nikel monokarbonat menyempurnakan keramik dan kaca dengan warna-warna cerah untuk ekspresi artistik dan keperluan industri.
- Katalis: Berfungsi sebagai katalis atau prekursor katalis dalam berbagai proses kimia, memfasilitasi reaksi oksidasi melalui pelepasan oksigen selama dekomposisi pada suhu tinggi.
- Pelapisan listrik: Penggunaan nikel monokarbonat sebagai prekursor memungkinkan pelapisan nikel ke berbagai permukaan, sehingga meningkatkan tampilan permukaan dan ketahanan terhadap korosi.
- Industri Baterai: Dalam teknologi baterai, khususnya yang berbahan dasar nikel, menyumbang bahan katoda sehingga mendukung kemajuan sistem baterai.
- Pigmen dan tinta: Nikel monokarbonat merupakan bagian integral dalam menghasilkan spektrum warna hijau pada pigmen, tinta, dan cat.
- Pertanian: Penerapannya sebagai sumber unsur hara nikel dalam pupuk bermanfaat bagi pertumbuhan tanaman dan digunakan dalam pertanian.
- Kedokteran: Meskipun jarang, para peneliti sedang menjajaki potensi aplikasi medis karena senyawa nikel tertentu, terutama nikel monokarbonat, yang menunjukkan sifat antimikroba.
- Fotografi: Secara historis, toner telah berperan dalam toner fotografi hitam putih, yang memperkaya corak dan kontras.
- Tekstil: Industri tekstil menggunakan nikel monokarbonat untuk meningkatkan penyerapan pewarna dan menanamkan warna pada kain.
- Penelitian dan Pendidikan: Atribut kimia nikel monokarbonat membuktikan pentingnya hal ini di laboratorium kimia untuk demonstrasi pendidikan, eksperimen, dan penelitian.
Aplikasi serbaguna ini menunjukkan pentingnya nikel monokarbonat di berbagai industri, mulai dari meningkatkan estetika keramik hingga berperan dalam teknologi canggih seperti baterai dan katalis.
Pertanyaan:
Q: Unsur manakah yang paling reaktif?
J: Natrium.
T: Bahan bermanfaat apa yang dibuat dengan mencampurkan besi dengan kromium, karbon, dan nikel?
J: Baja tahan karat.
T: Apakah nikel karbonat larut dalam air?
A: Tidak terlalu larut.
Q: Berapa mol karbon dalam nikel tetrakarbonil?
A: Empat tahi lalat.
T: Bagaimana cara menghilangkan pelapisan nikel dari baja karbon?
A: Menggunakan bahan pengupas kimia atau metode elektrokimia yang sesuai.
Q: Persamaan ionik bersih dari nikel(II) nitrat dan natrium karbonat?
J: Ni²⁺ + CO₃²⁻ → NiCO₃(s).
T: Peran karbon monoksida dalam ekstraksi nikel?
A: Ia bertindak sebagai zat pereduksi untuk mengekstraksi nikel dari bijihnya.
T: Kelarutan nikel monokarbonat?
A: Kelarutan rendah dalam air.
Q: Nomor atom karbon, natrium dan nikel?
A: Karbon: 6, Natrium: 11, Nikel: 28.
T: Apa yang terjadi jika Anda mencampurkan amonium karbonat, nikel klorida, dan air?
A: Pembentukan endapan nikel monokarbonat dan pelepasan gas amonium klorida.
