Natrium nitrit (NaNO2) adalah senyawa kimia yang biasa digunakan sebagai pengawet makanan untuk mencegah pertumbuhan bakteri dan meningkatkan warna dan rasa daging yang diawetkan seperti bacon dan hot dog.
| Nama IUPAC | Natrium nitrit |
| Formula molekul | NaNO2 |
| nomor CAS | 7632-00-0 |
| Sinonim | Asam nitrat, garam natrium; E250; Natriumnitrit; natrium nitrit; natrium nitrit; PBB 1500 |
| Di ChI | InChI=1S/NO2.Na/c2-1-3;/q-1;+1 |
Sifat natrium nitrit
Rumus Natrium Nitrit
Rumus kimia natrium nitrit adalah NaNO2. Hal ini menunjukkan bahwa satu mol natrium nitrit mengandung satu kation natrium, satu atom nitrogen, dan dua atom oksigen. Rumus tersebut digunakan untuk mewakili komposisi suatu zat dan dapat digunakan untuk memprediksi reaksi yang mungkin dialami suatu zat.
Massa Molar Natrium Nitrit
NaNo2 memiliki massa molar 69,0 g/mol. Ini adalah massa satu mol NaNo2, yang merupakan jumlah zat yang mengandung 6,02 x 10^23 molekul individu senyawa tersebut. Massa molar merupakan sifat fisik penting yang digunakan untuk menghitung berbagai sifat kimia dan fisik suatu zat.
Titik didih natrium nitrit
Titik didih NaNo2 adalah 320°C (608°F). Ini adalah suhu di mana NaNo2 akan berubah dari cair menjadi gas. Titik didih merupakan sifat yang penting karena dapat mempengaruhi penggunaan suatu zat dalam berbagai aplikasi industri, seperti produksi pewarna, pigmen, dan obat-obatan.
Titik lebur natrium nitrit
Titik leleh NaNo2 adalah 271°C (520°F). Ini adalah suhu di mana NaNo2 akan berubah dari padat menjadi cair. Titik leleh merupakan sifat yang penting karena dapat mempengaruhi stabilitas dan reaktivitas suatu zat pada temperatur yang berbeda.
Massa jenis natrium nitrit g/mL
Massa jenis NaNo2 adalah 2,168 g/mL. Massa jenis adalah massa per satuan volume suatu zat dan dapat digunakan untuk menentukan konsentrasi suatu larutan. Kepadatan NaNo2 juga dapat digunakan untuk menentukan kemurnian suatu sampel.
Berat Molekul Natrium Nitrit
Berat molekul NaNo2 adalah 69,0 g/mol. Ini adalah jumlah berat atom seluruh atom dalam molekul senyawa. Berat molekul merupakan sifat penting yang digunakan untuk menghitung berbagai sifat kimia dan fisik suatu zat.
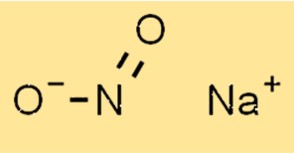
Struktur natrium nitrit
Struktur NaNo2 terdiri dari kation natrium (Na+) dan anion nitrit (NO2-). Anion nitrit memiliki geometri bidang trigonal dengan satu atom nitrogen dan dua atom oksigen. Kation natrium terletak di tengah anion nitrit.
Kelarutan natrium nitrit
NaNo2 larut dalam air, dengan kelarutan 820 g/L pada 20°C. Kelarutan adalah jumlah maksimum suatu zat yang dapat larut dalam sejumlah pelarut tertentu pada suhu tertentu. Kelarutan NaNo2 dapat dipengaruhi oleh faktor-faktor seperti suhu dan keberadaan zat terlarut lainnya.
| Penampilan | Bubuk kristal berwarna putih sampai agak kekuningan |
| Berat jenis | 2,168 gram/mL |
| Warna | Berwarna putih hingga agak kekuningan |
| Bau | Tidak berbau |
| Masa molar | 69,0 g/mol |
| Kepadatan | 2,168 gram/mL |
| Titik fusi | 271°C (520°F) |
| Titik didih | 320°C (608°F) |
| Titik kilat | Tak dapat diterapkan |
| Kelarutan dalam air | 820 g/L pada 20°C |
| Kelarutan | Larut dalam etanol dan gliserol |
| Tekanan uap | 1,33 kPa pada 20°C |
| Kepadatan uap | 2.3 (udara = 1) |
| pKa | 3.34 |
| pH | 7-8 (larutan 10%) |
Keamanan dan Bahaya Natrium Nitrit
NaNo2 dapat menimbulkan sejumlah bahaya terhadap kesehatan manusia dan lingkungan. Hal ini dianggap beracun jika tertelan, terhirup, atau diserap melalui kulit dan dapat menyebabkan methemoglobinemia, suatu kondisi di mana darah tidak mampu membawa oksigen ke jaringan tubuh. NaNo2 juga dapat menyebabkan iritasi pada mata, kulit, dan sistem pernapasan. Penting untuk menangani NaNo2 dengan hati-hati, menggunakan peralatan pelindung diri yang sesuai dan mengikuti prosedur penanganan dan pembuangan yang benar. Selain itu, NaNo2 dapat menimbulkan risiko terhadap lingkungan jika tidak ditampung dan dibuang dengan benar.
| Simbol bahaya | T+,C |
| Deskripsi Keamanan | Jauhkan dari bahan yang mudah terbakar. Jangan menghirup debu/asap/gas/kabut/uap/semburan. Kenakan sarung tangan/pakaian pelindung dan pelindung mata/wajah. Jika terjadi kebakaran: Gunakan CO2, bubuk kimia atau busa untuk memadamkan. Buang isi/wadah sesuai dengan peraturan lokal/regional/nasional/internasional. |
| Nomor identifikasi PBB | UN1500 |
| kode HS | 283410 |
| Kelas bahaya | 5.1 |
| Kelompok pengepakan | II |
| Toksisitas | Sangat beracun jika tertelan, terhirup dan terserap oleh kulit. Dapat menyebabkan methemoglobinemia. Mengiritasi mata, kulit dan sistem pernafasan. |
Metode sintesis natrium nitrit
Ada beberapa metode untuk mensintesis NaNo2.
Metode yang umum adalah dengan mereaksikan asam nitrat dan natrium hidroksida , yang menghasilkan natrium nitrat. Zat pereduksi seperti besi atau seng mereduksi natrium nitrat, membentuk NaNo2.
Metode lain melibatkan reaksi natrium nitrat dengan asam klorida , menghasilkan campuran asam nitrat dan natrium klorida. Natrium hidroksida bereaksi dengan asam nitrat menghasilkan NaNo2.
Sintesis NaNo2 dapat terjadi melalui reaksi antara amonia dan natrium nitrat , yang menghasilkan NaNo2 dan air sebagai produknya.
Proses pembuatan asam nitrat menghasilkan NaNo2 sebagai produk sampingan sekaligus mengoksidasi amonia dalam prosesnya.
Kegunaan natrium nitrit
NaNo2 memiliki kegunaan yang beragam di berbagai industri, beberapa di antaranya antara lain:
- Pengawetan Makanan: Biasa digunakan sebagai pengawet makanan, terutama pada daging yang diawetkan seperti bacon dan hot dog. Ini membantu mencegah pertumbuhan bakteri berbahaya dan menjaga warna dan rasa daging.
- Aplikasi Industri: Digunakan dalam berbagai aplikasi industri, seperti pengolahan logam dan sebagai penghambat korosi. Juga digunakan dalam produksi pewarna dan bahan kimia lainnya.
- Aplikasi Medis: Digunakan sebagai obat untuk mengobati keracunan sianida karena mengubah hemoglobin menjadi methemoglobin, yang dapat mengikat ion sianida dan mencegahnya mengikat hemoglobin.
- Pengolahan Air: Digunakan dalam pengolahan air untuk mengendalikan pertumbuhan bakteri dan ganggang berbahaya dalam sistem air.
- Pertanian: Digunakan dalam pertanian sebagai pupuk, membantu meningkatkan hasil dan kualitas tanaman.
- Fotografi: Digunakan dalam fotografi sebagai agen pengembangan.
Pertanyaan:
T: Apa itu natrium nitrit?
A: NaNo2 adalah senyawa kimia dengan rumus NaNO2. Ini adalah bubuk kristal berwarna putih atau agak kekuningan yang biasa digunakan sebagai pengawet makanan dan dalam berbagai aplikasi industri.
T: Siapa yang menemukan natrium nitrit?
J: NaNO2 pertama kali ditemukan pada tahun 1805 oleh ahli kimia Perancis Louis Nicolas Vauquelin.
T: Apakah natrium nitrit buruk bagi Anda?
A: Konsumsi NaNo2 yang berlebihan dapat membahayakan kesehatan manusia. Penyakit ini telah dikaitkan dengan masalah kesehatan seperti kanker dan methemoglobinemia, penyakit di mana darah tidak mampu mengangkut oksigen secara efektif. Namun bila digunakan dalam jumlah yang diatur dan terbatas, NaNo2 dianggap aman untuk dikonsumsi.
Q: Apa rumus natrium nitrit?
A: Rumus natrium nitrit adalah NaNO2.
T: Apakah natrium nitrit aman?
J: NaNo2 secara umum dianggap aman untuk dikonsumsi bila digunakan dalam jumlah yang diatur dan terbatas. Namun konsumsi berlebihan dapat berdampak buruk bagi kesehatan manusia.
T: Bagaimana cara membuat natrium nitrit?
A: NaNo2 dapat disintesis dengan berbagai metode, seperti reaksi asam nitrat dan natrium hidroksida, reaksi natrium nitrat dengan asam klorida, dan reaksi amonia dengan natrium nitrat. Namun, sintesis NaNo2 harus dilakukan dengan hati-hati, karena melibatkan penggunaan bahan kimia berbahaya dan memerlukan tindakan keselamatan yang tepat.
T: Apakah natrium nitrit merupakan oksidan?
A: Ya, NaNo2 adalah oksidan. Ini biasanya digunakan dalam kembang api sebagai zat pengoksidasi.
T: Bagaimana natrium nitrit mempengaruhi warna daging?
J: NaNO2 umumnya digunakan sebagai pengawet makanan pada daging yang diawetkan seperti bacon dan hot dog. Membantu menjaga warna daging dengan menghambat pertumbuhan bakteri berbahaya yang dapat menyebabkan perubahan warna.
T: Bagaimana NaNO2 dan NaNO3 diproduksi secara komersial?
A: NaNO3 dan NaNO2 diproduksi secara komersial dengan berbagai metode, seperti oksidasi amonia dan reaksi natrium hidroksida dengan asam nitrat. Mereka digunakan dalam berbagai aplikasi industri, medis dan pertanian, serta dalam pengawetan makanan.
