Metanol (CH3OH) adalah cairan tidak berwarna, mudah terbakar, dan berbau manis. Ini digunakan sebagai pelarut, bahan bakar dan antibeku. Ini bisa menjadi racun jika tertelan dan menyebabkan kebutaan atau kematian.
| Nama IUPAC | Metanol |
| Formula molekul | CH4O |
| nomor CAS | 67-56-1 |
| Sinonim | Metil alkohol, alkohol kayu, hidroksimetana, karbinol, nafta kayu, semangat kolonial |
| Di ChI | InChI=1S/CH4O/c1-2/h2H,1H3 |
Catatan: InChI adalah rantai panjang yang mewakili struktur unik suatu molekul. Ini mungkin tidak ditampilkan dengan benar di beberapa perangkat.
Sifat metanol
Massa molar metanol
Massa molar metanol adalah 32,04 g/mol. Ini dihitung dengan menambahkan berat atom atom karbon, hidrogen dan oksigen dalam satu molekul metanol. Nilai ini berguna untuk menentukan jumlah metanol yang dibutuhkan untuk menyiapkan larutan dengan konsentrasi tertentu atau untuk menentukan stoikiometri suatu reaksi kimia.
Titik didih metanol
Metanol memiliki titik didih 64,7°C (148,46°F). Titik didih yang relatif rendah ini menjadikan metanol berguna sebagai pelarut dalam berbagai aplikasi industri, termasuk produksi formaldehida, asam asetat, dan metil metakrilat. Namun, titik didih metanol yang rendah juga membuatnya mudah menguap dan mudah terbakar, sehingga dapat menimbulkan risiko keselamatan selama penyimpanan, penanganan, dan transportasi.
Titik leleh metanol
CH3OH memiliki titik leleh -97,6°C (-143,68°F). Artinya CH3OH berbentuk cair pada suhu kamar tetapi dapat dengan mudah dibekukan menjadi padat dengan mendinginkannya di bawah titik lelehnya. Titik leleh CH3OH yang rendah juga berguna dalam beberapa aplikasi laboratorium, seperti pembuatan pelarut kriogenik untuk spektroskopi resonansi magnetik nuklir.
Massa jenis metanol g/mL
Massa jenis CH3OH adalah 0,792 g/mL pada 20°C (68°F). Artinya CH3OH kurang padat dibandingkan air dan dapat mengapung di atasnya. Massa jenis CH3OH juga dapat digunakan untuk menghitung volume CH3OH yang diperlukan untuk memperoleh massa atau konsentrasi larutan tertentu.
Berat Molekul Metanol
Berat molekul CH3OH adalah 32,04 g/mol. Nilai ini dihitung dengan menjumlahkan berat atom atom karbon, hidrogen, dan oksigen dalam satu molekul CH3OH. Berat molekul CH3OH berguna dalam menentukan sifat fisiknya, seperti titik didih, titik leleh, dan massa jenis.
Struktur metanol
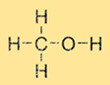
Metanol memiliki struktur sederhana yang terdiri dari gugus metil (CH3) dan gugus hidroksil (-OH) yang terikat pada satu atom karbon. Rumus molekul metanol adalah CH3OH. Metanol merupakan molekul polar karena adanya gugus hidroksil, yang membuatnya larut dalam pelarut polar seperti air dan etanol.
Rumus metanol
Rumus kimia metanol adalah CH3OH. Artinya setiap molekul metanol mengandung satu atom karbon, empat atom hidrogen, dan satu atom oksigen. Rumus metanol dapat digunakan untuk menentukan berat molekul dan sifat fisik metanol lainnya. Rumus kimia metanol juga berguna untuk menulis persamaan kimia dan menyeimbangkan reaksi kimia yang melibatkan metanol.
| Penampilan | Cairan tidak berwarna |
| Berat jenis | 0,792 g/ml pada 20°C |
| Warna | Tanpa warna |
| Bau | Manis, pedas |
| Masa molar | 32,04 g/mol |
| Kepadatan | 0,792 g/ml pada 20°C |
| Titik fusi | -97,6°C |
| Titik didih | 64,7°C |
| Titik kilat | 11,1°C |
| Kelarutan dalam air | Dapat bercampur |
| Kelarutan | Dapat larut dengan etanol, eter, aseton, dan banyak pelarut organik |
| Tekanan uap | 13,02 kPa pada 20°C |
| Kepadatan uap | 1.11 (udara = 1) |
| pKa | 15.5 |
| pH | 7 (netral) |
Catatan: Nilai yang tercantum dalam tabel ini merupakan perkiraan dan dapat bervariasi tergantung pada kondisi spesifik dan sumber metanol.
Keamanan dan bahaya metanol
CH3OH menimbulkan berbagai risiko keselamatan dan harus ditangani dengan hati-hati. Ini adalah cairan yang mudah terbakar dan dapat terbakar jika terkena panas, percikan api, atau nyala api. Uap CH3OH juga dapat membentuk campuran yang mudah meledak dengan udara. Menghirup uap CH3OH dapat menyebabkan pusing, sakit kepala, mual dan gangguan kesehatan lainnya. CH3OH juga beracun dan dapat diserap melalui kulit atau tertelan, menyebabkan komplikasi kesehatan yang serius termasuk kebutaan, koma, dan kematian. Penting untuk mengenakan pakaian pelindung dan menangani CH3OH di area yang berventilasi baik dan dilengkapi peralatan keselamatan yang sesuai, seperti kacamata, sarung tangan, dan respirator. Tumpahan harus segera dibersihkan dan dibuang dengan benar.
| Simbol bahaya | Tengkorak dan Tulang Bersilang, Mudah Terbakar |
| Deskripsi Keamanan | Jauhkan dari panas/percikan api/api terbuka/permukaan panas. Gunakan peralatan listrik/ventilasi/pencahayaan yang tahan ledakan. Jaga agar wadah tetap tertutup rapat. Kontainer yang dibumikan/ditebus dan peralatan penerimanya. Gunakan hanya alat yang tidak menimbulkan percikan api. Ambil tindakan pencegahan terhadap pelepasan listrik statis. Hindari menghirup uap. Cuci bersih setelah ditangani. Jangan makan, minum atau merokok saat menggunakan produk ini. |
| Sebuah pengidentifikasi | UN1230 |
| kode HS | 29051100 |
| Kelas bahaya | 3 |
| Kelompok pengepakan | II |
| Toksisitas | Metanol bersifat racun dan dapat menyebabkan kebutaan, koma dan kematian jika tertelan, terhirup atau terserap melalui kulit. Ini juga dapat menyebabkan iritasi, kemerahan dan luka bakar jika terkena. Paparan uap metanol dapat menyebabkan sakit kepala, pusing, mual dan gangguan kesehatan lainnya. Metanol harus ditangani dengan sangat hati-hati dan dengan peralatan pelindung yang sesuai. |
Catatan: Nilai yang tercantum dalam tabel ini merupakan perkiraan dan dapat bervariasi tergantung pada kondisi spesifik dan sumber metanol. Penting untuk mengacu pada lembar data keselamatan dan peraturan yang berlaku saat menangani metanol.
Metode sintesis metanol
Oksidasi langsung metana, oksidasi parsial gas alam, gasifikasi batubara, dan sintesis karbon dioksida dan hidrogen semuanya mensintesis metanol.
Salah satu metode paling umum untuk mensintesis metanol adalah dengan mengubah syngas secara katalitik, yang merupakan campuran karbon monoksida, karbon dioksida, dan hidrogen. Proses ini melibatkan penggunaan katalis, biasanya berbahan dasar tembaga, untuk memfasilitasi reaksi. Syngas dimasukkan ke dalam reaktor yang mengandung katalis pada suhu dan tekanan tinggi, menghasilkan produksi metanol.
Metode lain untuk mensintesis metanol melibatkan oksidasi metana secara langsung, yang melibatkan penggunaan suhu dan tekanan tinggi dengan adanya katalis seperti platina atau paladium. Cara ini lebih sulit dan mahal dibandingkan dengan metode syngas, namun lebih efisien dan dapat menghasilkan rendemen yang lebih tinggi.
Oksidasi parsial gas alam adalah metode lain sintesis metanol, yang melibatkan penggunaan oksigen atau udara untuk mengoksidasi sebagian gas alam, menghasilkan campuran karbon monoksida dan hidrogen. Campuran tersebut kemudian dimasukkan ke dalam reaktor yang mengandung katalis, sehingga menghasilkan produksi metanol.
Gasifikasi batubara adalah metode sintesis metanol lainnya, yang melibatkan konversi batubara menjadi syngas, diikuti dengan proses konversi katalitik yang sama seperti dijelaskan di atas.
Penangkapan dan pemanfaatan karbon mengubah emisi karbon dioksida dari proses industri menjadi metanol, menggunakan hidrogen sebagai zat pereduksi.
Kegunaan metanol
Metanol memiliki kegunaan yang luas di berbagai industri, antara lain:
- Bahan Bakar: Kendaraan, generator dan peralatan industri lainnya dapat menggunakan metanol sebagai bahan bakar.
- Pelarut: Metanol adalah pelarut yang sangat baik untuk banyak zat, termasuk resin, pewarna dan minyak. Produsen menggunakan metanol untuk memproduksi cat, pernis dan pelapis lainnya.
- Bahan antara kimia: digunakan sebagai bahan baku produksi formaldehida, asam asetat dan bahan kimia lainnya.
- Antibeku: Digunakan sebagai agen antibeku dalam sistem pendingin mobil.
- Agen penghilang lapisan es: Digunakan sebagai bahan penghilang lapisan es pada sayap pesawat dan landasan pacu bandara.
- Pembersih: Digunakan sebagai bahan pembersih dalam berbagai proses industri.
- Farmasi: Digunakan sebagai pelarut dalam produksi banyak produk farmasi.
- Energi alternatif: dipelajari sebagai bahan bakar alternatif untuk sel bahan bakar dan sebagai media penyimpanan energi potensial.
- Metanol menjadi Olefin (MTO): Olefin seperti etilen dan propilena berasal dari konversi metanol.
- Metanol menjadi Bensin (MTG): Suatu proses yang disebut MTG mengubah metanol menjadi bensin.
Pertanyaan:
T: Apa itu metanol?
J: Metanol, juga dikenal sebagai alkohol kayu, adalah cairan tidak berwarna, mudah terbakar, dan berbau manis. Ini adalah alkohol paling sederhana dan rumus kimianya adalah CH3OH.
T: Apakah metanol bersifat polar atau non-polar?
Jawaban: Metanol adalah molekul polar. Ia mempunyai muatan parsial positif pada atom hidrogen dan muatan parsial negatif pada atom oksigen, sehingga menghasilkan momen dipol.
T: Untuk apa metanol digunakan?
J: Metanol memiliki kegunaan yang luas di berbagai industri, termasuk sebagai bahan bakar, pelarut, zat antara kimia, antibeku, bahan penghilang lapisan es, pembersih, pelarut farmasi, dan media penyimpanan energi potensial. Ini juga digunakan dalam produksi formaldehida, asam asetat dan bahan kimia lainnya. Selain itu, metanol diubah menjadi olefin seperti etilen dan propilena, yang digunakan sebagai bahan baku produksi plastik.
