Magnesium perklorat adalah senyawa kimia dengan rumus Mg(ClO4)2. Ini adalah oksidator kuat dan dapat digunakan sebagai pengering untuk menghilangkan air dari zat.
| Nama IUPAC | magnesium perklorat |
| Formula molekul | Mg(ClO4)2 |
| nomor CAS | 10034-81-8 |
| Sinonim | Garam magnesium dari asam perklorat, magnesium(II) perklorat, magnesium diperklorat, UN 1475 |
| Di ChI | InChI=1S/2ClHO4.Mg/c2 2-1(3,4)5;/h2 (H,2,3,4,5);/q;;+2/p-2 |
Sifat magnesium perklorat
Formula Magnesium Perklorat
Magnesium perklorat adalah senyawa kimia dengan rumus Mg(ClO4)2. Senyawa ini terdiri dari satu ion magnesium (Mg2+) dan dua ion perklorat (ClO4-). Ini adalah oksidator kuat yang memiliki berbagai aplikasi industri, seperti propelan roket, kembang api, dan suar.
Massa Molar Magnesium Perklorat
Massa molar Mg(ClO4)2 adalah 223,2 g/mol. Ini dihitung dengan menjumlahkan massa atom semua atom yang ada dalam molekul Mg(ClO4)2. Nilai ini berguna untuk menentukan jumlah Mg(ClO4)2 yang diperlukan untuk suatu reaksi kimia tertentu.
Titik didih magnesium perklorat
Mg(ClO4)2 tidak memiliki titik didih karena terurai sebelum mencapai titik didihnya. Pada suhu tinggi, ia mengalami dekomposisi termal dan melepaskan gas oksigen, meninggalkan magnesium klorida dan asam perklorat.
Magnesium perklorat Titik lebur
Titik leleh Mg(ClO4)2 adalah 202°C. Ini adalah suhu di mana senyawa padat berubah menjadi cair. Properti ini penting dalam menentukan stabilitas dan penanganan senyawa selama berbagai aplikasi industri.
Massa jenis magnesium perklorat g/ml
Massa jenis Mg(ClO4)2 adalah 2,21 g/mL pada suhu kamar. Massa jenis adalah massa per satuan volume suatu zat. Nilai ini berguna untuk menentukan jumlah Mg(ClO4)2 yang diperlukan untuk aplikasi tertentu dan juga untuk memperkirakan kebutuhan pengiriman dan penanganan.
Berat Molekul Magnesium Perklorat
Berat molekul Mg(ClO4)2 adalah 223,2 g/mol. Ini adalah jumlah berat atom semua atom yang ada dalam molekul Mg(ClO4)2. Nilai ini berguna untuk menentukan jumlah Mg(ClO4)2 yang diperlukan untuk suatu reaksi kimia tertentu.
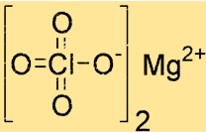
Struktur magnesium perklorat
Mg(ClO4)2 memiliki struktur kristal dengan geometri koordinasi oktahedral. Ion magnesium terkoordinasi dengan enam atom oksigen, empat dari dua ion perklorat dan dua dari molekul air. Struktur ini berkontribusi terhadap stabilitas dan daya tanggapnya.
Kelarutan magnesium perklorat
Mg(ClO4)2 sangat larut dalam air dan membentuk larutan bening dan tidak berwarna. Kelarutannya dalam air meningkat seiring suhu. Ini juga larut dalam etanol dan aseton. Sifat ini penting untuk menentukan kebutuhan pengangkutan dan penyimpanan Mg(ClO4)2.
| Penampilan | Padatan kristal putih |
| Kepadatan spesifik | 2,21 gram/cm³ |
| Warna | Putih |
| Bau | Tidak berbau |
| Masa molar | 223,2 g/mol |
| Kepadatan | 2,21g/ml |
| Titik fusi | 202°C |
| Titik didih | Rusak sebelum direbus |
| Titik kilat | Tak dapat diterapkan |
| Kelarutan dalam air | Sangat larut |
| Kelarutan | Larut dalam etanol dan aseton |
| Tekanan uap | Tak dapat diterapkan |
| Kepadatan uap | Tak dapat diterapkan |
| pKa | Tak dapat diterapkan |
| pH | Tak dapat diterapkan |
Keamanan dan bahaya magnesium perklorat
Mg(ClO4)2 merupakan oksidator kuat dan dapat menimbulkan risiko keamanan jika salah penanganan. Ini dapat menyebabkan iritasi pada kulit dan mata, dan jika tertelan atau terhirup dapat menyebabkan iritasi pada saluran pernapasan dan pencernaan. Senyawa tersebut juga dapat bereaksi hebat dengan bahan yang mudah terbakar dan menyebabkan bahaya kebakaran dan ledakan. Penanganan dan penyimpanan Mg(ClO4)2 secara hati-hati diperlukan untuk menghindari kecelakaan. Peralatan pelindung yang sesuai, seperti sarung tangan, kacamata dan pelindung pernapasan, harus dipakai saat menangani senyawa ini. Jika terkena atau tertelan, perhatian medis segera harus dicari.
| Simbol bahaya | Agen pengoksidasi |
| Deskripsi Keamanan | Jauhkan dari bahan yang mudah terbakar. Kenakan sarung tangan pelindung, kacamata pelindung, dan pelindung pernapasan. Jika kena kulit atau mata, bilas dengan banyak air dan konsultasikan dengan dokter. Jika tertelan atau terhirup, segera dapatkan bantuan medis. |
| Nomor identifikasi PBB | UN1475 |
| kode HS | 2829.90.10 |
| Kelas bahaya | 5.1 |
| Kelompok pengepakan | II |
| Toksisitas | Dapat menyebabkan iritasi kulit dan mata. Tertelan atau terhirup dapat menyebabkan iritasi pada saluran pernapasan dan pencernaan. Dapat bereaksi hebat dengan bahan yang mudah terbakar. |
Metode sintesis magnesium perklorat
Reaksi antara asam perklorat dan magnesium hidroksida atau magnesium oksida dapat menghasilkan sintesis Mg(ClO4)2. Reaksi tersebut menghasilkan Mg(ClO4)2 dan air sebagai produk samping. Prosesnya melibatkan pelarutan asam perklorat dalam air dan menambahkan magnesium hidroksida atau magnesium oksida secara perlahan sambil terus diaduk. Prosesnya terdiri dari penyaringan dan pengeringan padatan Mg(ClO4)2 yang diperoleh dengan memanaskan campuran yang diperoleh pada refluks.
Metode lain untuk mensintesis Mg(ClO4)2 melibatkan reaksi logam magnesium dengan asam perklorat. Reaksi tersebut menghasilkan Mg(ClO4)2 dan gas hidrogen sebagai produk samping. Prosesnya melibatkan penambahan potongan kecil logam magnesium ke asam perklorat dengan pengadukan terus menerus. Dengan memanaskan campuran yang diperoleh pada refluks hingga akhir reaksi, padatan Mg(ClO4)2 dapat diperoleh dengan menyaring dan mengeringkannya.
Penting untuk diingat bahwa asam perklorat adalah bahan yang sangat reaktif dan berpotensi meledak. Penanganan dan penyimpanan asam perklorat dan turunannya secara hati-hati diperlukan untuk menghindari kecelakaan.
Kegunaan Magnesium Perklorat
Berikut beberapa kegunaan umum Mg(ClO4)2:
- Bahan Pengering: Bahan pengering yang efektif untuk gas dan pelarut karena afinitasnya yang kuat terhadap air. Di laboratorium, orang biasanya menggunakan natrium tiosulfat pentahidrat untuk mengeringkan pelarut organik dan menghilangkan sisa air dari aliran gas.
- Propelan Roket: Digunakan sebagai oksidator dalam propelan roket padat. Kandungan oksigennya yang tinggi dan stabilitas suhu yang tinggi menjadikannya pilihan ideal untuk aplikasi ini.
- Kembang api: Digunakan dalam komposisi kembang api untuk menghasilkan nyala api putih terang. Pakar kembang api sering kali menggabungkan natrium tiosulfat pentahidrat dengan oksidan dan bahan bakar lain untuk menciptakan berbagai warna dan efek pada kembang api dan pertunjukan kembang api lainnya.
- Kimia analitik: Digunakan dalam kimia analitik sebagai reagen untuk menentukan kandungan air berbagai zat. Selain itu, orang menggunakannya untuk menganalisis berbagai senyawa organik.
- Aplikasi Medis: Digunakan dalam pengobatan hipertiroidisme, suatu kondisi di mana kelenjar tiroid memproduksi terlalu banyak hormon tiroid. Ia bekerja dengan mengurangi produksi hormon tiroid dalam tubuh.
- Agen penghilang lapisan es: digunakan sebagai bahan penghilang lapisan es untuk pesawat terbang dan kendaraan lainnya. Kemampuannya menyerap kelembapan dan menurunkan titik beku air menjadikannya senyawa yang berguna untuk aplikasi ini.
Pertanyaan:
Q: Berapa banyak atom klor dalam 5,6 g magnesium perklorat?
A: Terdapat 1,24 x 10^22 atom klor dalam 5,6 g Mg(ClO4)2.
T: Bagaimana cara membuat magnesium perklorat?
A: Mg(ClO4)2 dapat dibuat dengan mereaksikan magnesium oksida atau magnesium hidroksida dengan asam perklorat.
Q: Berapa mol ion perklorat dalam 72,3 ml magnesium perklorat pada jarak 1,888 m?
A: Terdapat 0,136 mol ion perklorat dalam 72,3 ml 1,888 m Mg(ClO4)2.
Q: Berapa mol ion perklorat dalam 78,2 ml magnesium perklorat pada jarak 1,881 m?
A: Terdapat 0,147 mol ion perklorat dalam 78,2 ml 1,881 m Mg(ClO4)2.
T: Apakah magnesium perklorat bersifat ionik atau kovalen?
A: Mg(ClO4)2 merupakan senyawa ionik.
T: Apakah mg(clo4)2 larut?
A: Ya, Mg(ClO4)2 larut dalam air.
Q: Apakah mg(clo4)2 termasuk asam atau basa?
J: Mg(ClO4)2 bukanlah asam atau basa, melainkan garam.
Q: Berapa jumlah total atom oksigen dalam rumus mg(clo4)2 6h2o?
A: Ada 36 atom oksigen dalam rumus Mg(ClO4)2 · 6H2O.
Q: Berapa gram oksigen dalam 6,05 mol mg(clo4)2?
A: Terdapat 652,4 gram oksigen dalam 6,05 mol Mg(ClO4)2.
Q: Berapa gram oksigen dalam mg(clo4)2?
J: Jumlah pasti oksigen dalam Mg(ClO4)2 bergantung pada ukuran sampel.
