Magnesium bromida (MgBr2) merupakan senyawa yang tersusun dari Mg dan Br yang biasa digunakan sebagai katalis dalam reaksi sintesis organik dan sebagai obat penenang dalam pengobatan.
| Nama IUPAC | magnesium bromida |
| Formula molekul | MgBr2 |
| nomor CAS | 7789-48-2 |
| Sinonim | Magnesium dibromida, UN1913, Bromomagnesite, Magnesium bromatum, Magnesiumbromid, Magnesium bromida |
| Di ChI | InChI=1S/2BrH.Mg/h2*1H;/q;;+2/p-2 |
Sifat magnesium bromida
Formula Magnesium Bromida
Rumus kimia magnesium bromida adalah MgBr2. Hal ini menunjukkan bahwa MgBr2 tersusun atas satu ion Mg+2 dan dua ion Br-. Rumusnya mewakili rasio atom dalam suatu molekul dan memainkan peran penting dalam menentukan sifat suatu senyawa. Rumus magnesium bromida menunjukkan bahwa ia merupakan senyawa ionik dengan titik leleh dan titik didih tinggi serta ikatan ionik yang kuat antara ion Mg+2 dan Bri-.
Massa Molar Magnesium Bromida
Massa molar MgBr2 adalah 184,113 g/mol. Ini adalah jumlah massa atom magnesium dan dua atom bromin. Massa molar merupakan parameter penting dalam perhitungan kimia karena membantu menentukan jumlah mol suatu zat dalam jumlah sampel tertentu. Massa molar MgBr2 memainkan peran penting dalam menentukan jumlah senyawa yang dibutuhkan untuk reaksi kimia.
Titik didih magnesium bromida
MgBr2 memiliki titik didih 1.204 derajat Celcius atau 2.199 derajat Fahrenheit. Titik didih suatu senyawa adalah suhu dimana tekanan uapnya sama dengan tekanan atmosfer. Titik didih MgBr2 yang tinggi menunjukkan bahwa MgBr2 merupakan senyawa stabil yang mampu menahan suhu tinggi tanpa terurai. Karakteristik ini membuatnya berguna dalam aplikasi suhu tinggi seperti metalurgi dan reaksi sintesis organik.
Titik leleh magnesium bromida
MgBr2 memiliki titik leleh 714 derajat Celsius atau 1.317 derajat Fahrenheit. Titik leleh suatu senyawa adalah suhu perubahan wujud padat menjadi cair. Titik leleh MgBr2 yang tinggi menunjukkan bahwa MgBr2 merupakan senyawa stabil dengan gaya antarmolekul yang kuat. Sifat ini membuatnya berguna sebagai reagen dalam reaksi kimia pada suhu tinggi.
Massa jenis magnesium bromida g/mL
Massa jenis MgBr2 adalah 3,72 g/mL. Massa jenis adalah ukuran jumlah massa per satuan volume suatu zat. Tingginya massa jenis MgBr2 menunjukkan bahwa MgBr2 merupakan senyawa berat yang dapat tenggelam dalam air. Karakteristik ini membuatnya berguna dalam berbagai aplikasi seperti sintesis anorganik dan sebagai obat penenang dalam pengobatan.
Berat Molekul Magnesium Bromida
Berat molekul MgBr2 adalah 184,113 g/mol. Ini adalah jumlah massa atom magnesium dan dua atom brom. Berat molekul memainkan peran penting dalam menentukan sifat kimia dan fisik suatu senyawa. Berat molekul MgBr2 mempengaruhi reaktivitas dan kelarutannya dalam berbagai pelarut.
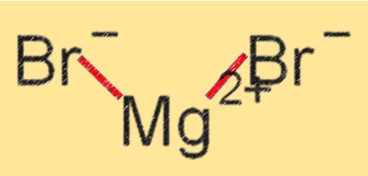
Struktur magnesium bromida
MgBr2 mempunyai struktur kisi kristal dengan ion Mg+2 dan Br- disatukan melalui ikatan ionik. Ini adalah padatan kristal putih yang sangat larut dalam air dan pelarut polar lainnya. Struktur kisi kristal MgBr2 berkontribusi terhadap titik leleh dan titik didih yang tinggi, serta stabilitasnya dalam berbagai reaksi kimia.
| Penampilan | Padatan kristal putih |
| Berat jenis | 3,72 gram/ml |
| Warna | Putih |
| Bau | Tidak berbau |
| Masa molar | 184,113 g/mol |
| Kepadatan | 3,72 gram/ml |
| Titik fusi | 714°C (1.317°F) |
| Titik didih | 1204°C (2199°F) |
| Titik kilat | Tak dapat diterapkan |
| Kelarutan dalam air | Sangat larut |
| Kelarutan | Larut dalam air, etanol, aseton dan eter |
| Tekanan uap | Tak dapat diterapkan |
| Kepadatan uap | Tak dapat diterapkan |
| pKa | Tak dapat diterapkan |
| pH | Netral |
Keamanan dan bahaya magnesium bromida
MgBr2 umumnya dianggap aman bila ditangani dengan benar. Namun, seperti senyawa kimia lainnya, bahan ini dapat menimbulkan bahaya jika tidak ditangani dengan hati-hati. MgBr2 bersifat korosif dan dapat menyebabkan iritasi parah pada kulit dan mata. Menghirup debu atau asap MgBr2 dapat menyebabkan iritasi pernafasan. Penting untuk mengenakan pakaian pelindung dan peralatan pernapasan saat menangani MgBr2. MgBr2 juga dapat bereaksi hebat dengan bahan kimia tertentu, seperti air atau asam, menghasilkan gas hidrogen bromida. Oleh karena itu, sangat penting untuk menyimpan dan menangani MgBr2 jauh dari bahan yang tidak kompatibel dan di tempat yang berventilasi baik.
| Simbol bahaya | Korosif |
| Deskripsi Keamanan | Hindari kontak dengan kulit dan mata. Kenakan pakaian pelindung dan peralatan pernapasan. Tangani dan simpan jauh dari bahan yang tidak kompatibel. |
| Nomor identifikasi PBB | UN2920 |
| kode HS | 2827.59.90 |
| Kelas bahaya | 8 |
| Kelompok pengepakan | II |
| Toksisitas | Toksisitas rendah jika ditangani dengan benar. Dapat menyebabkan iritasi kulit dan mata. Menghirup debu atau asap dapat menyebabkan iritasi pernafasan. |
Metode sintesis magnesium bromida
MgBr2 dapat disintesis dengan beberapa metode.
Metode yang umum adalah reaksi antara logam magnesium dan gas hidrogen bromida . Proses ini melibatkan pengaliran gas hidrogen bromida ke logam Mg, menghasilkan MgBr2 dan gas hidrogen.
Metode lain adalah reaksi antara magnesium oksida atau magnesium hidroksida dan asam hidrobromat . Proses ini menghasilkan MgBr2 dan air sebagai produknya.
Selain itu, MgBr2 dapat disintesis melalui reaksi antara magnesium karbonat dan asam hidrobromat , atau melalui reaksi antara magnesium sulfat dan NaBr.
Metode ini melibatkan pencampuran reagen dan membiarkan reaksi berlangsung, sehingga menghasilkan pembentukan MgBr2.
Kegunaan Magnesium Bromida
MgBr2 memiliki kegunaan yang beragam di berbagai industri. Berikut beberapa penerapan umumnya:
- Dalam sintesis organik: Digunakan sebagai katalis asam Lewis dalam reaksi sintesis organik, seperti reaksi Grignard, yang melibatkan pembentukan ikatan karbon-karbon.
- Dalam produksi bahan tahan api: Bahan tahan api, yang membuat bahan tidak mudah terbakar, mengandalkan bahan ini sebagai komponen penting dalam produksinya.
- Dalam industri minyak dan gas: Digunakan sebagai cairan penyelesaian di sumur minyak dan gas, yang membantu menjaga tekanan dan mencegah keruntuhan sumur.
- Dalam bidang farmasi: digunakan sebagai bahan aktif dalam beberapa produk farmasi, seperti obat penenang dan antikonvulsan.
- Dalam elektrokimia: Digunakan sebagai elektrolit dalam baterai dan perangkat elektrokimia lainnya.
- Dalam produksi logam: digunakan sebagai fluks dalam produksi logam tertentu, seperti aluminium dan titanium.
- Dalam kimia analitik: Digunakan sebagai reagen dalam kimia analitik untuk penentuan berbagai unsur, seperti boron dan fluorida.
Pertanyaan:
T: Apa rumus kimia magnesium bromida?
A: Rumus kimia magnesium bromida adalah MgBr2.
T: Apakah magnesium bromida bersifat ionik atau kovalen?
J: MgBr2 adalah senyawa ionik.
T: Apa rumus magnesium bromida?
A: Rumus magnesium bromida adalah MgBr2.
T: Apakah magnesium bromida larut dalam air?
A: Ya, MgBr2 larut dalam air. Ini sangat larut dalam air dan dapat larut membentuk larutan bening dan tidak berwarna.
T: Apa rumus magnesium bromida?
A: Rumus magnesium bromida adalah MgBr2.
