Kromium trioksida, juga dikenal sebagai asam kromat, adalah senyawa anorganik dengan rumus CrO3. Ini adalah asam anhidrida dari asam kromat dan kadang-kadang dipasarkan dengan nama yang sama.
| Nama IUPAC | Kromium(VI)oksida |
| Formula molekul | CrO3 |
| nomor CAS | 1333-82-0 |
| Sinonim | Anhidrida kromat, kromium oksida anhidrida, trioxochrome Chromium (VI) oksida |
| Di ChI | InChI=1S/Cr.3O |
Sifat kromium trioksida
Rumus kromium trioksida
Rumus kromat anhidrida adalah CrO3. Ini terdiri dari satu atom kromium yang terikat pada tiga atom oksigen.
Massa Molar Kromium Trioksida
Massa molar kromat anhidrida dihitung dengan menjumlahkan massa atom unsur penyusunnya, yaitu kromium (Cr) dan oksigen (O). Massa molarnya kira-kira 99,994 g/mol.
Titik didih kromium trioksida
Anhidrida kromat tidak memiliki titik didih yang jelas. Ketika dipanaskan, ia terurai menjadi kromium oksida dan gas oksigen tanpa melewati fase cair.
Titik leleh kromium trioksida
Titik leleh kromat anhidrida kira-kira 196°C. Pada suhu ini, wujudnya berubah dari padat menjadi cair.
Massa jenis kromium trioksida g/mL
Kepadatan kromat anhidrida kira-kira 2,7 g/mL. Nilai ini mewakili massa senyawa per satuan volume.
Berat Molekul Kromium Trioksida
Berat molekul kromat anhidrida, juga disebut massa molar, kira-kira 99,994 g/mol. Ini adalah jumlah massa atom atom kromium dan oksigen dalam senyawa.
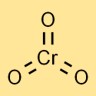
Struktur kromium trioksida
Anhidrida kromat memiliki struktur molekul di mana satu atom kromium terikat secara terpusat pada tiga atom oksigen. Ia mengadopsi geometri tetrahedral, dengan atom kromium di tengah dan atom oksigen di sudut.
Kelarutan kromium trioksida
Anhidrida kromat sangat larut dalam air. Ini mudah larut, membentuk larutan asam kromat. Kelarutan kromat anhidrida dalam air memungkinkannya digunakan dalam berbagai proses dan aplikasi kimia.
| Penampilan | Kristal merah tua |
| Berat jenis | 2,7 gram/ml |
| Warna | Merah gelap |
| Bau | Tidak berbau |
| Masa molar | 99,994 g/mol |
| Kepadatan | 2,7 gram/ml |
| Titik fusi | 196°C |
| Titik didih | Terurai |
| Titik kilat | Tak dapat diterapkan |
| Kelarutan dalam air | Sangat larut |
| Kelarutan | Larut dalam berbagai pelarut seperti etanol, eter, dll. |
| Tekanan uap | Tak dapat diterapkan |
| Kepadatan uap | Tak dapat diterapkan |
| pKa | Tak dapat diterapkan |
| pH | Asam (dalam larutan) |
Keamanan dan bahaya kromium trioksida
Anhidrida kromat menimbulkan risiko keamanan yang signifikan dan harus ditangani dengan hati-hati. Ini adalah zat yang sangat korosif dan mengoksidasi, mampu menyebabkan luka bakar parah pada kulit, mata dan sistem pernafasan. Menghirup atau menelan kromat anhidrida dapat menyebabkan gangguan pernapasan, masalah pencernaan, dan bahkan kerusakan organ.
Alat pelindung diri (APD) yang sesuai harus dipakai saat bekerja dengan kromat anhidrida, termasuk sarung tangan, kacamata dan respirator. Itu harus disimpan di tempat sejuk dan kering, jauh dari bahan yang tidak kompatibel dan sumber api.
Pembuangan kromat anhidrida harus dilakukan sesuai dengan peraturan setempat, karena dianggap sebagai limbah berbahaya. Ini tidak boleh dilepaskan ke lingkungan.
| Simbol bahaya | Korosif, Pengoksidasi |
| Deskripsi Keamanan | Hindari kontak dengan kulit, mata dan inhalasi. Gunakan peralatan pelindung yang sesuai. |
| Nomor identifikasi PBB | PBB 1463 |
| kode HS | 2819.90.90 |
| Kelas bahaya | 5.1 (Agen pengoksidasi) |
| Kelompok pengepakan | II |
| Toksisitas | Sangat beracun |
Metode sintesis kromium trioksida
Ada beberapa metode untuk mensintesis kromat anhidrida.
Metode yang umum melibatkan reaksi antara natrium dikromat dan asam sulfat . Dalam lingkungan terkendali, seseorang mencampurkan natrium dikromat (Na2Cr2O7) dengan asam sulfat pekat (H2SO4) . Reaksi tersebut menghasilkan pembentukan larutan kromat anhidrida (CrO3) berwarna merah tua dan natrium sulfat (Na2SO4) sebagai produk sampingan.
Metode lain melibatkan oksidasi senyawa kromium(III) menggunakan zat pengoksidasi kuat seperti hidrogen peroksida (H2O2) atau asam nitrat (HNO3) . Dalam proses ini, campurkan senyawa kromium(III) dengan zat pengoksidasi pada kondisi tertentu untuk mengubah kromium(III) menjadi kromat anhidrida.
Pembuatan kromat anhidrida dilakukan dengan mereaksikan senyawa logam kromium atau kromium(II) dengan zat pengoksidasi kuat seperti kalium permanganat (KMnO4) atau kalium dikromat (K2Cr2O7). Reaksi mengarah pada pembentukan kromat anhidrida.
Penting untuk dicatat bahwa sintesis kromat anhidrida harus dilakukan dengan langkah-langkah keamanan yang tepat dan sesuai dengan peraturan yang sesuai. Individu yang berpengalaman harus melakukan proses sintesis di laboratorium yang lengkap untuk memastikan keselamatan mereka dan meminimalkan dampak lingkungan.
Kegunaan Kromium Trioksida
Anhidrida kromat digunakan sebagai zat pengoksidasi dalam berbagai proses kimia, termasuk produksi senyawa organik.
- Produsen menggunakannya untuk memproduksi pewarna dan pigmen, seperti kuning krom dan hijau krom.
- Industri pelapisan listrik menggunakannya untuk menyimpan krom pada permukaan logam, memberikan ketahanan terhadap korosi dan hasil akhir yang menarik.
- Ini digunakan dalam pembuatan katalis kromium untuk reaksi polimerisasi dalam produksi plastik dan bahan sintetis.
- Ini berperan dalam sintesis obat-obatan dan zat antara organik.
- Perawatan pengawet kayu menggunakannya sebagai fungisida dan insektisida untuk melindungi dari pembusukan dan hama.
- Laboratorium menggunakannya sebagai reagen untuk berbagai pengujian dan analisis kimia.
- Penggunaannya dalam produksi gelas dan keramik khusus meningkatkan warna dan sifat tertentu.
- Industri penyamakan kulit menggunakannya untuk mengolah kulit, membantu menstabilkan dan mewarnai kulit.
- Ini adalah komponen dalam formulasi bahan pembersih dan perawatan permukaan untuk permukaan logam.
Penting untuk menangani kromat anhidrida dengan hati-hati karena sifatnya yang beracun dan korosif. Kepatuhan terhadap protokol keselamatan yang tepat menjamin perlindungan manusia dan lingkungan selama penggunaan dan pembuangannya.
Pertanyaan:
T: Apa itu CrO3?
A: CrO3 adalah kromat anhidrida, senyawa yang terdiri dari satu atom kromium yang terikat pada tiga atom oksigen.
Q: Apakah CrO3 merupakan oksidator kuat?
J: Ya, CrO3 adalah zat pengoksidasi kuat yang biasa digunakan dalam reaksi kimia untuk memfasilitasi oksidasi berbagai senyawa.
T: Apa pengaruh CrO3 terhadap alkohol?
A: CrO3 dapat mengoksidasi alkohol dan mengubahnya menjadi senyawa karbonil yang sesuai, seperti aldehida atau keton.
Q: Produk organik apa yang Anda peroleh dari reaksi 1-pentanol dengan CrO3, H2O dan H2SO4?
A: Reaksi tersebut akan menghasilkan produk organik 1-pentanon, yang merupakan keton.
Q: Reagen mana yang terbaik untuk melakukan transformasi berikut: PCC, HIO4, CrO3, NaOH?
J: Pilihan reagen terbaik untuk transformasi ini adalah PCC (pyridinium chlorochromate).
T: Apakah CrO3 bersifat amfoter?
J: Tidak, CrO3 tidak bersifat amfoter. Ini adalah senyawa yang sangat asam tetapi tidak mampu menunjukkan sifat basa.
Q: Bagaimana cara mencari bilangan oksidasi Cr dalam CrO3?
A: Bilangan oksidasi Cr dalam CrO3 adalah +6.
T: Apa nama CrO3?
J: Nama CrO3 adalah kromat anhidrida.
T: Apa pengaruh CrO3 terhadap alkohol non-anonik?
J: CrO3 dapat mengoksidasi alkohol non-anonik, mengubahnya menjadi senyawa karbonil yang sesuai, seperti keton non-anonik.
Q: Berapa muatan kation logam transisi pada CrO3?
A: Kation logam transisi pada CrO3 yaitu kromium mempunyai muatan +6.
