Karbon disulfida adalah senyawa kimia mudah menguap yang dibentuk dengan menggabungkan karbon dan belerang. Ini digunakan dalam proses industri, pelarut dan pembuatan serat rayon.
| Nama IUPAC | Karbon disulfida |
| Formula molekul | CS2 |
| nomor CAS | 75-15-0 |
| Sinonim | Karbon disulfida, ditiokarb, karbon disulfida |
| Di ChI | InChI=1S/CS2/c2-1-3 |
Sifat karbon disulfida
Rumus karbon disulfida
Rumus kimia karbon disulfida adalah CS2. Ia terdiri dari satu atom karbon dan dua atom belerang, terikat bersama dalam susunan linier. Rumus sederhana ini penting untuk memahami komposisi dasar senyawa.
Massa Molar Karbon Disulfida
Massa molar karbon disulfida kira-kira 76,14 g/mol. Untuk menghitungnya, kita tambahkan massa atom dari satu atom karbon (12,01 g/mol) dan dua atom belerang (masing-masing 32,06 g/mol). Mengetahui massa molar membantu berbagai perhitungan kimia.
Titik didih karbon disulfida
Karbon disulfida memiliki titik didih yang relatif rendah, sekitar 46,3°C (115,3°F). Sifat ini membuatnya mudah menguap dan mudah menguap. Titik didihnya yang rendah penting dalam proses dan aplikasi industri yang memerlukan penguapan cepat.
Titik lebur karbon disulfida
Titik leleh karbon disulfida kira-kira -110,8°C (-187,4°F). Ia tetap dalam keadaan padat pada suhu di bawah titik ini dan berubah menjadi cair ketika dipanaskan. Memahami titik lelehnya sangat penting untuk penanganan dan penyimpanan.
Massa jenis karbon disulfida g/mL
Kepadatan karbon disulfida kira-kira 1,26 g/mL pada suhu kamar. Nilai ini berarti massa per satuan volume. Karena lebih padat dari air, ia akan tenggelam ketika dicampur dan kepadatannya akan mempengaruhi kelarutannya dalam berbagai pelarut.
Berat Molekul Karbon disulfida
Berat molekul karbon disulfida kira-kira 76,14 g/mol, dihitung dari rumus kimianya. Nilai ini berperan penting dalam stoikiometri dan dalam menentukan jumlah senyawa dalam reaksi kimia.
Struktur karbon disulfida
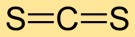
Karbon disulfida memiliki struktur molekul linier, dengan atom karbon di tengah dan atom belerang di kedua sisinya. Susunan sederhana ini sangat penting untuk memahami perilaku kimianya dan interaksinya dengan zat lain.
Kelarutan karbon disulfida
Karbon disulfida sulit larut dalam air, hanya sekitar 0,2 g per 100 ml air pada suhu kamar. Namun, sangat larut dalam pelarut organik seperti benzena dan etanol. Perilaku kelarutan ini penting untuk berbagai aplikasi dalam kimia dan industri.
| Penampilan | Cairan tidak berwarna |
| Berat jenis | 1.26 |
| Warna | Tanpa warna |
| Bau | Aromanya menyengat dan manis |
| Masa molar | 76,14 g/mol |
| Kepadatan | 1,26 gram/ml |
| Titik fusi | -110,8°C (-187,4°F) |
| Titik didih | 46,3°C (115,3°F) |
| Titik kilat | -30°C (-22°F) |
| Kelarutan dalam air | 0,2g/100ml (20°C) |
| Kelarutan | Larut dalam pelarut organik seperti benzena dan etanol |
| Tekanan uap | 318 mmHg (20°C) |
| Kepadatan uap | 2,62 (udara = 1) |
| pKa | ~ -2 |
| pH | Netral (pH 7) |
Keamanan dan bahaya karbon disulfida
Karbon disulfida menimbulkan risiko keamanan yang signifikan. Bahan ini sangat mudah terbakar dan uapnya dapat membentuk campuran yang mudah meledak di udara. Paparan yang terlalu lama dapat menyebabkan pusing, sakit kepala, dan bahkan kehilangan kesadaran. Hal ini juga berbahaya bagi kehidupan akuatik dan lingkungan. Ventilasi yang memadai, peralatan pelindung diri, dan penyimpanan tahan api sangat penting untuk meminimalkan risiko. Hindari kontak dengan kulit dan mata, karena dapat menyebabkan iritasi dan kerusakan. Penanganan harus dilakukan di lingkungan yang terkendali dengan baik dan tumpahan harus diatasi dengan cepat. Memahami dan mengikuti petunjuk keselamatan sangat penting untuk mencegah kecelakaan dan memastikan lingkungan kerja yang aman saat menangani karbon disulfida.
| Simbol bahaya | Mudah terbakar, berbahaya |
| Deskripsi Keamanan | Cairan dan uap yang sangat mudah terbakar. Berbahaya jika terhirup atau tertelan. Menyebabkan iritasi kulit dan mata. |
| Nomor identifikasi PBB | UN1131 |
| kode HS | 2813.10.1000 |
| Kelas bahaya | 3 (Cairan mudah terbakar) |
| Kelompok pengepakan | II (Bahaya sedang) |
| Toksisitas | Toksisitas sedang |
Metode sintesis karbon disulfida
Beberapa metode aktif memungkinkan sintesis karbon disulfida.
Metode umum melibatkan mereaksikan belerang dengan metana atau gas alam pada suhu tinggi, menghasilkan produk CS2.
Pendekatan lain adalah dengan mereaksikan uap belerang dengan batu bara panas. Selain itu, kombinasi karbon monoksida dan uap belerang di atas katalis juga dapat menghasilkan karbon disulfida.
Selain itu, sintesis langsung CS2 dapat terjadi ketika karbon bereaksi dengan uap belerang pada suhu tinggi. Di laboratorium, ahli kimia menggunakan reaksi antara kalium xantat dan asam sulfat untuk produksi karbon disulfida dalam skala kecil.
Setiap metode memerlukan tindakan pencegahan keselamatan yang tepat karena sifat karbon disulfida yang sangat mudah terbakar dan beracun. Keserbagunaan metode sintesis ini memungkinkan berbagai aplikasi industri, termasuk penggunaannya sebagai pelarut, sebagai bahan mentah dalam proses kimia, dan dalam pembuatan serat rayon.
Kegunaan karbon disulfida
Karbon disulfida menemukan berbagai aplikasi karena sifat serbagunanya. Berikut beberapa kegunaannya:
- Aplikasi penelitian dan laboratorium: Laboratorium menggunakan karbon disulfida sebagai reagen untuk berbagai reaksi kimia, termasuk sintesis senyawa organologam.
- Ekstraksi minyak atsiri: Karbon disulfida digunakan dalam ekstraksi minyak atsiri dari tanaman, memfasilitasi pemisahan senyawa aromatik yang diinginkan.
- Ekstraksi Minyak: Industri menggunakan karbon disulfida untuk mengekstraksi minyak dari biji-bijian dan sayuran karena kelarutannya dan titik didihnya yang rendah.
- Pembuatan serat rayon: Karbon disulfida memainkan peran penting dalam produksi serat rayon karena membantu melarutkan selulosa, yang kemudian diekstrusi oleh produsen untuk membentuk serat sintetis yang digunakan dalam tekstil.
- Aplikasi industri: Karbon disulfida berkontribusi pada produksi pestisida, fumigan, dan bahan kimia karet. Selain itu, ia bertindak sebagai katalis dalam pembuatan asam sulfat dan karbon tetraklorida.
- Pelarut: Karbon disulfida berfungsi sebagai pelarut untuk berbagai zat, termasuk minyak, gemuk, karet, resin, dan belerang. Oleh karena itu, bahan ini biasa digunakan dalam produksi produk berbasis selulosa.
- Proses Kimia: Berfungsi sebagai bahan baku dalam sintesis senyawa organik seperti karbon tetraklorida, tiokarbamat dan ditiokarbamat. Senyawa ini dapat diterapkan dalam industri pertanian dan farmasi.
- Vulkanisasi karet: Karbon disulfida berpartisipasi dalam proses vulkanisasi karet, meningkatkan kekuatan, elastisitas, dan ketahanan ausnya.
Penerapan yang beragam ini menyoroti pentingnya karbon disulfida di berbagai industri, mulai dari tekstil dan pertanian hingga penelitian dan manufaktur.
Pertanyaan:
Q: Manakah dari molekul berikut yang bersifat polar? A. amonia B. oktan c. air d. karbon disulfida
J: a, Air (H2O) bersifat polar karena bentuk molekulnya yang melengkung dan pembagian elektron yang tidak merata.
Q: Berapakah sudut antara ikatan karbon-sulfur pada molekul karbon disulfida (CS2)?
A: Sudut antara ikatan karbon-belerang di CS2 adalah 180 derajat, membentuk geometri linier.
Q: Berapa jumlah total atom dalam 1 mol karbon disulfida?
J: Satu mol karbon disulfida mengandung 6,02 x 10^23 molekul, dan setiap molekul memiliki 3 atom (1 karbon dan 2 belerang).
T: Menurut Anda, unsur manakah yang dapat larut dalam pelarut nonpolar, karbon disulfida, CS2?
A: Zat nonpolar seperti oktan (b) harus larut dalam karbon disulfida (CS2).
T: Berapa titik didih normal karbon disulfida?
J: Titik didih normal karbon disulfida adalah sekitar 46,3°C (115,3°F).
T: Apakah karbon disulfida bersifat polar atau non-polar?
J: Karbon disulfida (CS2) adalah molekul non-polar karena bentuknya yang linier dan pembagian elektron yang sama.
Q: Apa rumus karbon disulfida?
A: Rumus karbon disulfida adalah CS2.
T: Apa itu karbon disulfida?
A: Karbon disulfida (CS2) adalah senyawa kimia mudah menguap yang terdiri dari satu atom karbon dan dua atom belerang, yang digunakan dalam berbagai aplikasi industri.
T: Seberapa pentingkah fakta bahwa karbon disulfida lebih padat daripada air?
J: Kepadatan karbon disulfida yang lebih tinggi dibandingkan dengan air berarti karbon tersebut tidak mudah bercampur dan akan membentuk lapisan yang berbeda jika digabungkan.
T: Bagaimana manusia bisa menemukan karbon disulfida?
J: Manusia dapat bersentuhan dengan karbon disulfida melalui proses industri, aplikasi kimia, atau penanganan produk tertentu.
T: Apa yang terjadi jika Anda menelan karbon disulfida?
J: Menelan karbon disulfida dapat menyebabkan gangguan kesehatan termasuk mual, sakit kepala, dan berdampak pada sistem saraf sehingga berbahaya bagi kesehatan manusia.
T: Apakah karbon disulfida lebih padat daripada air?
J: Ya, karbon disulfida lebih padat daripada air, dengan massa jenis sekitar 1,26 g/mL dibandingkan dengan massa jenis air yang 1 g/mL.
