Kalsium bisulfit (Ca(HSO3)2) merupakan senyawa yang tersusun dari kalsium, belerang, dan oksigen. Ini umumnya digunakan sebagai pengawet makanan dan antioksidan dalam industri makanan.
| Nama IUPAC | Kalsium hidrogen sulfit |
| Formula molekul | Ca(HSO3)2 |
| nomor CAS | 13780-03-5 |
| Sinonim | Kalsium bisulfit, Kalsium hidrogen sulfit, Kalsium asam sulfat, Kapur bisulfit |
| Di ChI | InChI=1S/Ca.2H2O3S/c;2*1-4(2)3/jam;(H2,1,2,3)/q+2;;/p-2 |
Sifat kalsium bisulfit
Formula Kalsium Bisulfit
Rumus kimia kalsium bisulfit adalah Ca(HSO3)2. Ini menunjukkan jumlah dan jenis atom dalam suatu molekul atau unit rumus. Rumusnya penting dalam menentukan berat molekul, massa molar, dan sifat-sifat senyawa lainnya. Ca(HSO3)2 merupakan senyawa penting yang digunakan dalam industri pangan sebagai pengawet dan antioksidan.
Massa Molar Kalsium Bisulfit
Ca(HSO3)2 memiliki massa molar 202,2 g/mol. Ini adalah senyawa ionik yang terdiri dari kalsium, hidrogen sulfit, dan sulfur dioksida. Massa molar penting untuk menghitung jumlah Ca(HSO3)2 yang dibutuhkan dalam suatu reaksi atau untuk menyiapkan larutan dengan konsentrasi yang diinginkan.
Titik didih kalsium bisulfit
Titik didih Ca(HSO3)2 bukanlah nilai yang pasti karena terurai sebelum mencapai titik didihnya. Ca(HSO3)2 terurai melepaskan sulfur dioksida. Oleh karena itu, tidak digunakan dalam proses yang memerlukan aplikasi suhu tinggi.
Titik lebur kalsium bisulfit
Titik leleh Ca(HSO3)2 adalah 203°C. Pada suhu ini, ia terurai membentuk kalsium sulfat dan sulfur dioksida. Penguraian Ca(HSO3)2 merupakan reaksi eksotermik dan menghasilkan panas dalam jumlah besar. Oleh karena itu, harus ditangani dengan hati-hati saat dipanaskan.
Massa jenis kalsium bisulfit g/mL
Kepadatan Ca(HSO3)2 bervariasi tergantung pada bentuk dimana ia ditemukan. Bentuk Ca(HSO3)2 anhidrat memiliki massa jenis 2,68 g/mL, sedangkan bentuk dihidrat memiliki massa jenis 1,98 g/mL. Massa jenis suatu zat penting dalam menentukan berapa banyak zat yang dibutuhkan untuk mengisi volume tertentu.
Berat Molekul Kalsium Bisulfit
Berat molekul Ca(HSO3)2 adalah 202,2 g/mol. Dihitung dengan menjumlahkan berat atom unsur penyusunnya: kalsium (40,08 g/mol), hidrogen (1,008 g/mol), belerang (32,06 g/mol) dan oksigen (15,99 g/mol). Berat molekul penting dalam menentukan jumlah zat yang dibutuhkan untuk suatu reaksi.
Struktur kalsium bisulfit
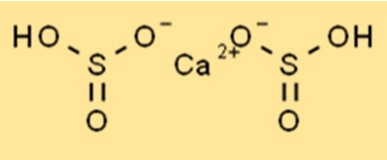
Struktur Ca(HSO3)2 merupakan senyawa ionik dengan rumus kimia Ca(HSO3)2. Ia memiliki bentuk tetrahedral dengan atom kalsium pusat dikelilingi oleh empat atom oksigen. Ion hidrogen sulfit dihubungkan ke atom kalsium melalui ikatan ionik. Struktur Ca(HSO3)2 penting untuk memahami sifat kimianya.
Kelarutan kalsium bisulfit
Ca(HSO3)2 cukup larut dalam air, dengan kelarutan sekitar 60 gram per 100 mililiter air pada suhu kamar. Kelarutannya meningkat seiring suhu dan juga larut dalam etanol dan gliserol.
| Penampilan | Bubuk kristal putih |
| Berat jenis | 2,68 (anhidrat), 1,98 (dihidrat) |
| Warna | Putih |
| Bau | Tidak berbau |
| Masa molar | 202,2 g/mol |
| Kepadatan | 2,68 g/mL (anhidrat), 1,98 g/mL (dihidrat) |
| Titik fusi | 203°C |
| Titik didih | Terurai |
| Titik kilat | Tak dapat diterapkan |
| Kelarutan dalam air | Larut |
| Kelarutan | Larut dalam air, tidak larut dalam pelarut organik |
| Tekanan uap | Tak dapat diterapkan |
| Kepadatan uap | Tak dapat diterapkan |
| pKa | 1.92 |
| pH | 4.5-6.0 |
Keamanan dan Bahaya Kalsium Bisulfit
Ca(HSO3)2 umumnya dianggap aman bila digunakan dalam jumlah kecil dalam produk makanan. Namun, hal ini bisa berbahaya jika tidak ditangani dengan benar. Dapat menyebabkan iritasi kulit, iritasi mata dan masalah pernapasan jika terhirup. Penelanan dalam jumlah besar dapat menyebabkan gangguan pencernaan, termasuk mual dan muntah. Ca(HSO3)2 harus ditangani dengan hati-hati dan peralatan pelindung, seperti sarung tangan dan respirator, harus dipakai saat menanganinya. Itu harus disimpan di tempat sejuk dan kering, jauh dari panas dan bahan yang tidak kompatibel. Tumpahan harus segera dibersihkan untuk menghindari paparan terhadap bahan tersebut.
| Simbol bahaya | Tidak ada |
| Deskripsi Keamanan | Hindari menghirup, menelan dan kontak kulit/mata. Kenakan peralatan pelindung. |
| Nomor identifikasi PBB | Tidak diatur |
| kode HS | 28321000 |
| Kelas bahaya | Tidak diklasifikasikan |
| Kelompok pengepakan | Tak dapat diterapkan |
| Toksisitas | Toksisitasnya rendah, namun dapat menyebabkan iritasi kulit dan mata, masalah pernafasan, dan gangguan pencernaan jika tertelan dalam jumlah banyak. |
Metode sintesis kalsium bisulfit
Beberapa metode dapat digunakan untuk mensintesis Ca(HSO3)2.
Salah satu metodenya adalah dengan mereaksikan gas sulfur dioksida dengan kalsium hidroksida , menghasilkan Ca(HSO3)2 dan air.
Prosesnya melibatkan reaksi kalsium oksida dengan gas sulfur dioksida, menghasilkan kalsium sulfit. Kemudian, reaksi gas sulfur dioksida dengan kalsium sulfit menghasilkan Ca(HSO3)2.
Reaksi gas sulfur dioksida dengan air dan kalsium karbonat menghasilkan Ca(HSO3)2, gas karbon dioksida, dan air.
Untuk mensintesis Ca(HSO3)2 di laboratorium, gas sulfur dioksida dapat ditambahkan ke dalam larutan kalsium hidroksida atau kalsium oksida hingga pH yang diinginkan tercapai. Larutan yang dihasilkan akan mengandung Ca(HSO3)2, yang dapat dimurnikan dengan metode filtrasi atau pengendapan.
Kegunaan Kalsium Bisulfit
Ca(HSO3)2 memiliki beberapa kegunaan di berbagai industri karena sifatnya yang unik. Berikut beberapa kegunaan Ca(HSO3)2 yang paling umum:
- Industri makanan: Digunakan sebagai pengawet makanan untuk mencegah pertumbuhan bakteri dan mikroorganisme lainnya pada produk makanan, terutama pada buah-buahan dan sayuran.
- Pengolahan Air: Digunakan dalam pengolahan air untuk menghilangkan kelebihan klorin dan bahan kimia lainnya dari air dan untuk mencegah pertumbuhan bakteri dan ganggang dalam sistem air.
- Industri Tekstil: Digunakan dalam industri tekstil untuk menghilangkan kelebihan pewarna dari kain dan mencegah pemudaran selama proses pewarnaan.
- Industri kertas: Digunakan dalam industri kertas untuk memutihkan pulp dan mencegah perubahan warna pada produk kertas.
- Industri kimia: Digunakan dalam industri kimia sebagai zat pereduksi dan sebagai sumber gas sulfur dioksida.
- Industri farmasi: Digunakan dalam industri farmasi sebagai antioksidan dan pengawet pada obat-obatan tertentu.
Pertanyaan:
T: Apakah Otoritas Keamanan Pangan Eropa menyetujui kalsium bisulfit?
J: Ya, Otoritas Keamanan Pangan Eropa (EFSA) telah menyetujui penggunaan Ca(HSO3)2 sebagai bahan tambahan makanan. Ini terdaftar sebagai pengawet makanan yang disetujui di Uni Eropa.
T: Berapa peringkat E untuk kalsium bisulfit?
A: Bilangan E Ca(HSO3)2 adalah E227. Nomor E adalah kode yang ditetapkan untuk bahan tambahan makanan oleh Uni Eropa.
T: Apakah kalsium bisulfit aman?
A: Ca(HSO3)2 umumnya dianggap aman dikonsumsi dalam jumlah kecil. Namun, dapat menyebabkan iritasi kulit dan mata, masalah pernafasan, dan gangguan pencernaan jika tertelan dalam jumlah banyak. Penting untuk menangani dan menyimpan Ca(HSO3)2 dengan benar untuk memastikan keamanannya.
Q: Berapa kelarutan kalsium bisulfit dalam air?
A: Ca(HSO3)2 cukup larut dalam air, dengan kelarutan sekitar 60 gram per 100 mililiter air pada suhu kamar.
T: Apa sifat termodinamika kalsium bisulfit?
A: Sifat termodinamika Ca(HSO3)2 meliputi titik leleh sekitar 150°C dan titik didih sekitar 160°C. Kapasitas panas dan entalpi pembentukannya juga telah diselidiki dalam berbagai penelitian.
