Kalium fosfat (K3PO4) merupakan senyawa yang mengandung unsur kalium dan fosfor. Ini umumnya digunakan sebagai bahan tambahan makanan dan pupuk karena kelarutannya yang tinggi dan kemampuannya menyediakan nutrisi penting untuk pertumbuhan tanaman.
| Nama IUPAC | Kalium fosfat |
| Formula molekul | K3PO4 |
| nomor CAS | 7778-53-2 |
| Sinonim | Tripotassium fosfat, kalium ortofosfat, kalium fosfat tersier, tripotassium monofosfat, kalium fosfat tribasa |
| Di ChI | InChI=1S/3K.H3O4P/c;;;1-5(2,3)4/jam;;;(H3,1,2,3,4)/q3*+1;/p-3 |
Sifat kalium fosfat
Formula Kalium Fosfat
Rumus kimia kalium fosfat adalah K3PO4. Hal ini menunjukkan bahwa senyawa tersebut mengandung tiga ion K+ dan satu ion PO43- pada setiap satuan rumus. Rumus kalium fosfat berguna untuk menentukan stoikiometri reaksi yang melibatkan senyawa, serta mengidentifikasi jumlah setiap unsur yang ada dalam massa senyawa tertentu.
Massa Molar Kalium Fosfat
Massa molar K3PO4 adalah 212,27 g/mol. Ini dihitung dengan menambahkan massa atom kalium, fosfor dan oksigen ke dalam senyawa. Massa molar merupakan parameter penting untuk menentukan jumlah zat yang ada dalam suatu massa suatu senyawa. Hal ini juga berguna untuk menghitung stoikiometri reaksi yang melibatkan K3PO4.
Titik didih kalium fosfat
Titik didih K3PO4 adalah 1660°C. Titik didih yang tinggi ini disebabkan oleh kuatnya ikatan ion antara ion K+ dan ion PO43- dalam senyawa tersebut. Ini juga merupakan indikasi stabilitas senyawa pada suhu tinggi. Titik didih K3PO4 berguna dalam berbagai aplikasi industri, seperti produksi keramik dan kaca.
Titik Leleh Kalium Fosfat
Titik leleh K3PO4 adalah 1340°C. Ini adalah suhu di mana senyawa padat berubah menjadi cair. Tingginya titik leleh K3PO4 disebabkan oleh sifat senyawa yang bersifat ionik sehingga memerlukan energi yang besar untuk mengatasi gaya tarik menarik antar ion. Titik leleh K3PO4 berguna untuk menentukan kesesuaiannya untuk berbagai aplikasi, seperti produksi pupuk dan bahan tambahan pangan.
Massa jenis kalium fosfat g/mL
Massa jenis K3PO4 adalah 2,564 g/mL pada suhu kamar. Kepadatan senyawa yang tinggi disebabkan oleh adanya tiga ion K+ dan satu ion PO43- dalam setiap satuan rumus. Kepadatan K3PO4 berguna dalam menentukan kelarutan dan perilakunya dalam berbagai proses industri, seperti dalam produksi pupuk dan bahan tambahan pangan.
Berat Molekul Kalium Fosfat
Berat molekul K3PO4 adalah 212,27 g/mol. Ini adalah jumlah berat atom seluruh atom dalam senyawa. Berat molekul berguna untuk menghitung jumlah zat yang ada dalam suatu massa suatu senyawa, serta menentukan stoikiometri reaksi yang melibatkan K3PO4.
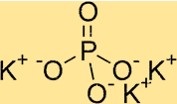
Struktur kalium fosfat
K3PO4 memiliki struktur kristal ortorombik. Ini terdiri dari satu set PO4 tetrahedra, dengan masing-masing ion fosfat berbagi dua atom oksigen dengan ion fosfat tetangga. Ion kalium terletak di antara tetrahedra fosfat, dikelilingi oleh atom oksigen. Struktur K3PO4 berguna untuk memahami sifat-sifatnya, seperti kelarutan dan stabilitas termal.
| Penampilan | Bubuk kristal putih |
| Kepadatan spesifik | 2,564 gram/mL |
| Warna | Putih |
| Bau | Tidak berbau |
| Masa molar | 212,27 g/mol |
| Kepadatan | 2,564 gram/mL |
| Titik fusi | 1340°C |
| Titik didih | 1660°C |
| Titik kilat | Tak dapat diterapkan |
| Kelarutan dalam air | 100 g/l (20°C) |
| Kelarutan | Larut dalam etanol dan aseton, tidak larut dalam eter |
| Tekanan uap | Dapat diabaikan |
| Kepadatan uap | Tak dapat diterapkan |
| pKa | pKa1 = 2,16, pKa2 = 7,21, pKa3 = 12,32 |
| pH | PH larutan 1% adalah 11,5 |
Keamanan dan Bahaya Kalium Fosfat
K3PO4 umumnya dianggap aman digunakan bila ditangani dengan benar. Namun, seperti bahan kimia lainnya, bahan ini dapat menimbulkan bahaya jika salah ditangani atau tertelan dalam jumlah banyak. Senyawa ini diklasifikasikan sebagai iritasi pada kulit, mata, dan pernapasan dan dapat menyebabkan luka bakar parah atau gangguan pernapasan jika terhirup atau tertelan dalam konsentrasi tinggi. Bahan ini juga tidak cocok dengan asam dan zat pengoksidasi dan dapat menyebabkan kebakaran atau ledakan jika terkena bahan-bahan tersebut. Oleh karena itu, penting untuk menangani K3PO4 dengan hati-hati, memakai peralatan pelindung yang sesuai, dan menyimpannya di tempat yang sejuk, kering, dan berventilasi baik, jauh dari bahan yang tidak kompatibel.
| Simbol bahaya | Xi (Menjengkelkan) |
| Deskripsi Keamanan | Hindari kontak dengan kulit dan mata. |
| Nomor identifikasi PBB | UN 2833 (untuk anhidrat), UN 2423 (untuk trihidrat) |
| kode HS | 28352400 |
| Kelas bahaya | 6.1 (beracun) |
| Kelompok pengepakan | AKU AKU AKU |
| Toksisitas | LD50 (oral, tikus): 2,340 mg/kg; LC50 (inhalasi, tikus): 50 mg/L |
Metode sintesis kalium fosfat (K3PO4)
Ada beberapa metode untuk mensintesis K3PO4, termasuk reaksi asam fosfat (H3PO4) dengan kalium hidroksida (KOH) atau dekomposisi termal KH2PO4.
Salah satu metodenya adalah dengan mereaksikan KOH dan H3PO4 dalam jumlah yang sama dalam air pada suhu sekitar 60 hingga 80°C. Prosedurnya melibatkan penguapan campuran yang dihasilkan dan memanaskan residu padat hingga sekitar 300°C untuk menghasilkan K3PO4.
Cara lainnya adalah dengan mereaksikan KH2PO4 dengan KOH pada suhu tinggi (di atas 400°C) menghasilkan K3PO4 dan air. Oven khusus dapat melakukan proses yang disebut dekomposisi termal.
Reaksi asam fosfat dengan kalium karbonat (K2CO3) dan reaksi kalium oksida (K2O) dengan fosfor pentoksida (P2O5) merupakan metode tambahan untuk memproduksi K3PO4.
Kegunaan Kalium Fosfat
K3PO4 memiliki beberapa kegunaan praktis di berbagai industri, antara lain:
- Pupuk: Biasa digunakan sebagai pupuk karena kandungan fosfornya yang tinggi. Petani sering menambahkannya ke tanah untuk menyediakan nutrisi penting bagi tanaman.
- Industri Makanan: Digunakan sebagai bahan tambahan makanan untuk mengatur tingkat keasaman, mencegah perubahan warna dan memperbaiki tekstur.
- Zat penyangga: Berbagai aplikasi laboratorium menggunakannya sebagai zat penyangga yang efektif, termasuk larutan penyangga kalibrasi pH dan penelitian biologi.
- Deterjen: Digunakan dalam produksi deterjen dan produk pembersih karena kemampuannya melunakkan air dan mencegah penumpukan endapan mineral.
- Obat: Digunakan sebagai suplemen makanan untuk mengobati kondisi medis tertentu, seperti kadar fosfat darah rendah.
- Pengolahan Air: Digunakan dalam pengolahan air untuk mencegah pembentukan kerak dan korosi pada pipa dan peralatan.
- Flame Retardant: Digunakan sebagai penghambat api pada berbagai bahan, termasuk tekstil dan plastik, karena kemampuannya melepaskan uap air dan mencegah penyebaran api.
Pertanyaan:
T: Apakah kalium fosfat larut dalam air?
A: Ya, K3PO4 larut dalam air.
Q: Berapa banyak ion kalium yang dibutuhkan untuk berikatan dengan ion fosfat?
A: Diperlukan tiga ion kalium untuk berikatan dengan ion fosfat, membentuk K3PO4.
Q: Endapan apa yang terbentuk ketika larutan kalsium bromida dan kalium fosfat dicampur?
A: Ketika larutan kalsium bromida dan K3PO4 dicampur, terbentuk endapan kalsium fosfat (Ca3(PO4)2).
Q: Apakah k3po4 larut dalam air?
A: Ya, K3PO4 larut dalam air.
Q: Apakah k3po4 dapat larut?
A: Ya, K3PO4 larut dalam air.
Q: Produk apa yang dihasilkan dari pencampuran larutan Ni(C2H3O2)2 (aq) dan K3PO4 (aq) dalam air?
A: Ketika larutan berair Ni(C2H3O2)2 dan K3PO4 dicampur, akan terbentuk endapan nikel(II) fosfat (Ni3(PO4)2), begitu pula larutan berair kalium asetat (KCH3COO) dan asam asetat (CH3COOH).
Q: Unsur manakah yang meningkatkan bilangan oksidasinya pada reaksi ini? 3KOH + H3PO4 → K3PO4 + 3H2O
A: Unsur fosfor meningkatkan bilangan oksidasinya dari +5 pada H3PO4 menjadi +5 pada K3PO4.
T: Apa itu K3PO4?
A: K3PO4 adalah formula kimia kalium fosfat, senyawa yang digunakan dalam berbagai aplikasi, seperti pupuk, bahan tambahan makanan, dan produk pembersih.
