Oktan adalah bahan bakar beroktan tinggi yang digunakan pada mesin pembakaran. Ini meningkatkan kinerja mesin, mengurangi ketukan dan meningkatkan keluaran tenaga. Ini biasanya digunakan pada kendaraan berperforma tinggi dan mobil balap.
| Nama IUPAC | Oktan |
| Formula molekul | C8H18 |
| nomor CAS | 111-65-9 |
| Sinonim | n-Oktan, Oktan Normal, Oktan |
| Di ChI | InciChI=1S/C8H18/c1-3-5-7-8-6-4-2/h3-8H2.1-2H3 |
Sifat oktan
Rumus Oktan
Rumus oktan adalah C8H18. Ini terdiri dari delapan atom karbon dan delapan belas atom hidrogen. Rumus molekul ini mewakili susunan atom dalam molekul oktan tunggal.
Massa Oktan Molar
Massa molar oktan dihitung dengan menjumlahkan massa atom semua atom dalam rumus kimianya. Massa molar oktan kira-kira 114,22 gram per mol. Hal ini penting dalam berbagai perhitungan yang melibatkan jumlah oktan dalam sampel tertentu.
Titik didih angka oktan
Oktan memiliki titik didih sekitar 125,5 derajat Celcius (257,9 derajat Fahrenheit). Ini adalah suhu di mana oktan berubah dari fase cair menjadi fase gas. Titik didih oktan dipengaruhi oleh struktur molekul dan gaya antarmolekulnya.
Titik lebur oktan
Oktan memiliki titik leleh sekitar -57 derajat Celcius (-70,6 derajat Fahrenheit). Ini adalah suhu di mana oktan berubah dari padat menjadi cair. Titik leleh oktan bergantung pada faktor-faktor seperti struktur molekul dan gaya antarmolekul.
Kepadatan oktan g/mL
Massa jenis oktan kira-kira 0,703 gram per mililiter (g/mL). Massa jenis adalah ukuran massa per satuan volume suatu zat. Massa jenis oktan yang lebih rendah dibandingkan dengan air yang memiliki massa jenis 1 g/mL, menunjukkan bahwa oktan lebih rendah massa jenisnya dibandingkan air.
Berat Molekul Oktan
Berat molekul oktan kira-kira 114,22 gram per mol. Ini adalah jumlah berat atom semua atom dalam molekul oktan. Berat molekul sangat penting dalam berbagai perhitungan, seperti menentukan jumlah oktan yang dibutuhkan dalam suatu reaksi.
Struktur oktan
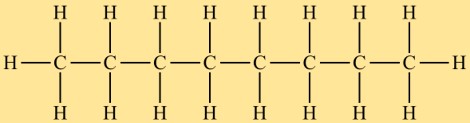
Oktan termasuk dalam golongan alkana dan mempunyai struktur linier. Ini terdiri dari rantai delapan atom karbon dengan atom hidrogen melekat padanya. Susunan atom pada oktan sedemikian rupa sehingga tidak ada struktur bercabang atau siklik.
kelarutan bilangan oktan
Oktan dianggap tidak larut dalam air. Ia menunjukkan kelarutan yang rendah dalam pelarut polar karena sifatnya yang nonpolar. Namun, oktan sangat larut dalam pelarut non-polar, seperti hidrokarbon lain, minyak, dan pelarut organik.
| Penampilan | Cairan tidak berwarna |
| Berat jenis | 0,703 gram/ml |
| Warna | Tanpa warna |
| Bau | Tidak berbau |
| Masa molar | 114,22 g/mol |
| Kepadatan | 0,703 gram/ml |
| Titik fusi | -57°C (-70,6°F) |
| Titik didih | 125,5°C (257,9°F) |
| Titik kilat | -18°C (0°F) |
| Kelarutan dalam air | Tidak larut |
| Kelarutan | Larut dalam pelarut non-polar |
| Tekanan uap | 12,9 mmHg pada 20°C |
| Kepadatan uap | 3,47 (udara = 1) |
| pKa | ~45 |
| pH | Netral |
Keamanan dan Bahaya Oktan
Octan menimbulkan risiko keamanan tertentu yang perlu dipertimbangkan. Bahan ini sangat mudah terbakar dan mudah terbakar, sehingga menimbulkan bahaya kebakaran. Uap oktan dapat membentuk campuran yang mudah meledak dengan udara, sehingga meningkatkan risiko kebakaran dan ledakan. Penting untuk menangani oktan dengan hati-hati, memastikan ventilasi yang memadai dan menghindari sumber api. Kontak kulit dengan oktan dapat menyebabkan iritasi dan kekeringan. Menelan atau menghirup oktan dapat menyebabkan risiko kesehatan termasuk iritasi pernafasan dan efek sistem saraf pusat. Penting untuk mengikuti tindakan pencegahan keselamatan, menggunakan alat pelindung diri yang sesuai, dan menjauhkan oktan dari zat yang tidak kompatibel.
| Simbol bahaya | Mudah terbakar (F), Iritan (Xi) |
| Deskripsi Keamanan | Jauhkan dari panas/percikan/api terbuka. Gunakan di area yang berventilasi baik. Hindari kontak dengan kulit dan mata. |
| Nomor identifikasi PBB | PBB 1262 |
| kode HS | 2901.10.10 |
| Kelas bahaya | 3 – Cairan yang mudah terbakar |
| Kelompok pengepakan | AKU AKU AKU |
| Toksisitas | Lemah |
Metode sintesis oktan
Berbagai metode dapat mensintesis oktan. Metode yang umum dilakukan adalah dengan mereformasi fraksi minyak bumi seperti nafta secara katalitik. Proses ini memanaskan nafta dan melewatkannya ke katalis, biasanya platina atau renium, sehingga mendorong penataan ulang molekul hidrokarbon. Penataan ulang ini menghasilkan senyawa oktan yang lebih tinggi, terutama oktan.
Metode lain adalah dengan mengalkilasi isobutana dengan butena. Asam sulfat atau asam fluorida , bertindak sebagai katalis asam, memfasilitasi reaksi isobutana, hidrokarbon bercabang, dengan hidrokarbon tak jenuh (butena). Reaksi ini membentuk molekul oktan rantai cabang.
Isomerisasi adalah pendekatan tambahan untuk menghasilkan oktan. Ini mengubah hidrokarbon rantai lurus seperti heksana atau heptana menjadi isomer rantai bercabang. Berbagai katalis, termasuk katalis zeolit atau platina, dapat mengkatalisis proses ini.
Selain itu, oktan dapat diperoleh dengan menghidrogenasi hidrokarbon aromatik seperti toluena atau xilena menggunakan gas hidrogen dan katalis yang sesuai. Reaksi ini mengubah senyawa aromatik menjadi sikloheksana, yang selanjutnya dapat didehidrogenasi untuk menghasilkan oktan.
Metode sintesis ini memainkan peran penting dalam produksi oktan, yang banyak digunakan sebagai komponen bahan bakar pada bensin. Dengan menggunakan teknik ini, oktan dengan angka oktan yang diinginkan dapat diperoleh, sehingga memastikan performa dan efisiensi optimal pada mesin pembakaran.
Kegunaan oktan
Octan menemukan berbagai kegunaan di berbagai industri karena khasiatnya yang bermanfaat. Berikut adalah beberapa aplikasi utama oktan:
- Bahan Bakar: Oktan terutama digunakan sebagai komponen bahan bakar dalam bensin. Ini meningkatkan nilai oktan bahan bakar, yang meningkatkan kinerja mesin, mengurangi ketukan dan mencegah kerusakan mesin. Hal ini sangat penting terutama pada kendaraan berperforma tinggi dan mobil balap.
- Mesin Pembakaran: Oktan sangat penting untuk mesin pembakaran internal, termasuk pada mobil, sepeda motor, dan mesin kecil. Ini menyediakan sumber energi yang diperlukan untuk pengoperasian dan penggerak kendaraan dan mesin.
- Sintesis Kimia: Oktan berfungsi sebagai prekursor untuk produksi berbagai bahan kimia. Ini digunakan sebagai bahan mentah untuk sintesis senyawa hidrokarbon lainnya, seperti alkohol, aldehida dan asam.
- Pelarut Laboratorium: Oktan digunakan sebagai pelarut non-polar di laboratorium. Polaritasnya yang rendah membuatnya cocok untuk melarutkan senyawa nonpolar, sehingga memungkinkan peneliti melakukan eksperimen dan ekstraksi tertentu.
- Referensi Standar: Untuk menentukan angka oktan dan membandingkan kinerja berbagai bahan bakar, para peneliti dan ahli secara aktif menggunakan oktan sebagai acuan dan senyawa acuan. Ini membantu menetapkan standar kualitas dan efisiensi bensin dan bahan bakar hidrokarbon lainnya.
- Kalibrasi: Oktan digunakan dalam kalibrasi peralatan, seperti kromatografi gas, untuk memastikan pengukuran yang akurat dan tepat. Sifatnya yang diketahui dan perilakunya yang terkarakterisasi dengan baik menjadikannya standar kalibrasi yang andal.
- Penelitian dan Pengembangan: Oktan sangat penting untuk tujuan penelitian dan pengembangan di industri otomotif dan bahan bakar. Para ilmuwan dan insinyur secara aktif mempelajari sifat, karakteristik pembakaran, dan dampak oktan terhadap lingkungan untuk meningkatkan efisiensi bahan bakar, mengurangi emisi, dan berinovasi pada bahan bakar alternatif.
Octan secara aktif menggerakkan transportasi, memungkinkan sintesis kimia, memfasilitasi pekerjaan laboratorium, dan mendorong kemajuan dalam industri otomotif dan energi.
Pertanyaan:
Q: Senyawa manakah yang memiliki titik leleh tertinggi?
J: Al2(CO3)3.
Q: Berapa entalpi pembentukan standar isomer C8H18(g) ini?
J: Entalpi pembentukan standar isomer C8H18(g) spesifik untuk isomer tertentu dan memerlukan identifikasi untuk menentukan nilainya.
Q: Berapa massa dalam gram 5,90 mol C8H18?
A: Massa 5,90 mol C8H18 kira-kira 789,26 gram.
Q: Pernyataan manakah yang paling tepat membandingkan titik leleh butana (C4H10) dengan titik leleh oktan (C8H18)?
A: Oktan (C8H18) memiliki titik leleh lebih tinggi dibandingkan butana (C4H10).
T: Apa nama C8H18?
A: Nama C8H18 adalah oktan.
T: Apa itu oktan?
A: Oktan adalah hidrokarbon alkana dengan rumus molekul C8H18. Ini biasanya digunakan sebagai komponen yang mudah terbakar dalam bensin.
Q: Berapa nilai oktan bensin?
J: Angka oktan bensin mengacu pada kemampuannya menahan ketukan selama pembakaran. Ini menunjukkan sifat anti-ketukan bahan bakar dan kesesuaiannya untuk mesin kompresi tinggi.
Q: Berapakah bilangan oktan dan bilangan setana?
A: Angka oktan mengukur sifat anti-ketukan bensin, sedangkan angka setana mengukur kualitas penyalaan bahan bakar solar.
T: Apa itu oktan?
A: Nilai Oktan adalah nilai numerik yang mewakili kinerja suatu bahan bakar dalam menahan ketukan selama pembakaran. Ini menunjukkan kemampuan bahan bakar untuk menahan kompresi sebelum penyalaan.
Q: Apa nama hidrokarbon CH3(CH2)6CH3?
A: Nama hidrokarbon CH3(CH2)6CH3 adalah oktan.
