Hidrogen peroksida atau H2O2 adalah cairan berwarna biru pucat dengan sifat pengoksidasi yang kuat. Ini biasanya digunakan sebagai desinfektan, pemutih dan roket sebagai propelan. Dalam konsentrasi tinggi bisa berbahaya.
| Nama IUPAC | Dihidrogen dioksida |
| Formula molekul | H2O2 |
| nomor CAS | 7722-84-1 |
| Sinonim | Hidrogen Dioksida, Peroksida, Oxydol, Superoxol, Hidronium Dioksida, Peroxaan, Asepticper, dll. |
| Di ChI | InChI=1S/H2O2/c1-2/h1-2H |
Sifat hidrogen peroksida
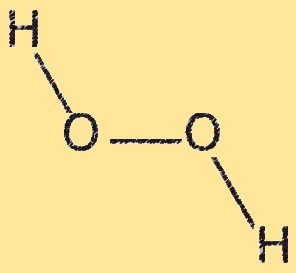
struktur H2O2
Hidrogen peroksida memiliki struktur molekul melengkung, dengan sudut kira-kira 104,5 derajat antara dua atom oksigen. Molekul tersebut memiliki dua ikatan OH dan satu ikatan OO. Ikatan OO lemah dan mudah putus, menjadikan hidrogen peroksida sebagai zat pengoksidasi kuat. Struktur melengkung hidrogen peroksida dihasilkan dari tolakan antara pasangan elektron bebas pada atom oksigen.
Rumus Hidrogen Peroksida
Rumus kimia hidrogen peroksida adalah H2O2, yang menunjukkan bahwa setiap molekul hidrogen peroksida mengandung dua atom hidrogen dan dua atom oksigen. Rumusnya adalah cara ringkas untuk merepresentasikan komposisi molekul suatu zat. Rumus kimia hidrogen peroksida penting untuk memahami sifat-sifatnya dan reaksinya dengan zat lain.
Massa Molar Hidrogen Peroksida
Hidrogen peroksida memiliki massa molar sekitar 34,01 g/mol. Massa molar adalah jumlah massa atom seluruh atom dalam suatu molekul senyawa. Hidrogen peroksida memiliki dua atom hidrogen dan dua atom oksigen dalam setiap molekulnya, sehingga massa molarnya dihitung dengan menjumlahkan massa atom masing-masing atom. Massa molar merupakan sifat penting suatu zat karena digunakan dalam perhitungan stoikiometri untuk menentukan jumlah zat yang ada dalam sampel tertentu.
Titik didih hidrogen peroksida
Titik didih hidrogen peroksida adalah 150,2°C (302,4°F). Suhu ini merupakan titik dimana tekanan uap zat cair sama dengan tekanan atmosfer. Di atas suhu ini, cairan berubah menjadi gas, dan di bawah suhu ini, ia tetap berbentuk cair. Titik didih hidrogen peroksida lebih tinggi dibandingkan air, yang mendidih pada suhu 100°C, karena adanya ikatan hidrogen antarmolekul dalam hidrogen peroksida.
Titik Leleh Hidrogen Peroksida
Titik leleh hidrogen peroksida adalah -0,43°C (31,23°F). Suhu ini merupakan titik di mana wujud padat dan cair suatu zat berada dalam kesetimbangan. Pada suhu ini, bentuk padat hidrogen peroksida melebur menjadi cairan. Titik leleh hidrogen peroksida lebih rendah dibandingkan air, yang meleleh pada suhu 0°C, karena sifat molekul hidrogen peroksida yang tidak stabil.
Massa jenis hidrogen peroksida g/mL
Massa jenis hidrogen peroksida adalah 1,11 g/mL pada suhu dan tekanan standar (STP). Artinya satu mililiter hidrogen peroksida memiliki berat 1,11 gram. Massa jenis hidrogen peroksida lebih besar dibandingkan dengan air yang memiliki massa jenis 1 g/mL, karena adanya atom oksigen yang lebih berat dalam hidrogen peroksida.
Berat Molekul Hidrogen Peroksida
Berat molekul hidrogen peroksida adalah 34,01 g/mol. Nilai ini dihitung dengan menjumlahkan massa atom setiap atom dalam molekul hidrogen peroksida. Berat molekul merupakan sifat penting suatu zat karena digunakan dalam berbagai perhitungan, termasuk menentukan konsentrasi hidrogen peroksida dalam suatu larutan.
| Penampilan | Cairan bening dan tidak berwarna |
| Berat jenis | 1,11 g/cm3 pada 20°C |
| Warna | Biru pucat (bentuk murni) |
| Bau | Hampir tidak berbau (bentuk murni) |
| Masa molar | 34,01 g/mol |
| Kepadatan | 1,11 g/mL pada 20°C |
| Titik fusi | -0,43°C |
| Titik didih | 150,2°C |
| Titik kilat | Tak dapat diterapkan |
| Kelarutan dalam air | Benar-benar dapat larut dengan air |
| Kelarutan | Larut dalam alkohol, eter dan pelarut organik lainnya |
| Tekanan uap | 23,3 mmHg pada 20°C |
| Kepadatan uap | 1.1 (udara = 1) |
| pKa | 11.6 (pada 25°C) |
| pH | 4.5 – 6.0 (larutan 10%) |
Catatan: Nilai-nilai ini adalah nilai tipikal dan dapat bervariasi tergantung pada kemurnian, konsentrasi, dan faktor lainnya.
Keamanan dan Bahaya Hidrogen Peroksida
Hidrogen peroksida bisa berbahaya jika tidak ditangani dengan benar. Ini adalah zat pengoksidasi kuat yang dapat bereaksi hebat dengan zat organik dan anorganik, yang berpotensi menyebabkan kebakaran atau ledakan. Bentuk pekat hidrogen peroksida juga bersifat korosif dan dapat menyebabkan luka bakar parah atau kerusakan jaringan jika terkena kulit atau mata. Menghirup uap hidrogen peroksida dapat mengiritasi saluran pernafasan dan jika tertelan dapat menyebabkan kerusakan internal yang serius atau kematian. Oleh karena itu, tindakan pencegahan keselamatan yang tepat, seperti mengenakan pakaian pelindung dan sarung tangan, menghindari kontak dengan bahan yang tidak kompatibel, dan menggunakan di area yang berventilasi baik, harus dilakukan saat menangani hidrogen peroksida.
| Simbol bahaya | HAI,C |
| Deskripsi Keamanan | Jauhkan dari panas, percikan api dan nyala api. Kenakan pakaian pelindung dan sarung tangan. Hindari kontak dengan kulit, mata dan pakaian. Jangan menghirup uapnya. Jika terjadi kebakaran, gunakan semprotan air, busa, bahan kimia kering, atau karbon dioksida. |
| Nomor identifikasi PBB | PBB 2015 |
| kode HS | 2847.00.00 |
| Kelas bahaya | 5.1 |
| Kelompok pengepakan | II |
| Toksisitas | Beracun jika tertelan atau terhirup. Menyebabkan luka bakar kulit yang parah dan kerusakan mata. Dapat menyebabkan iritasi pernafasan. Dapat menyebabkan kebakaran atau ledakan. |
Metode sintesis hidrogen peroksida
Hidrogen peroksida dapat disintesis dengan berbagai metode, termasuk proses antrakuinon, autoksidasi 2-etilantrahidrokuinon, dan elektrolisis asam sulfat encer. Metode yang paling umum untuk produksi hidrogen peroksida secara komersial adalah proses antrakuinon.
Dalam proses antrakuinon, antrakuinon terlebih dahulu dihidrogenasi menjadi antrahidrokuinon, yang kemudian dioksidasi dengan udara dengan adanya katalis menghasilkan hidrogen peroksida. Hidrogen peroksida kemudian diekstraksi dan dimurnikan menggunakan berbagai teknik, seperti distilasi dan filtrasi.
Metode lain untuk mensintesis hidrogen peroksida adalah autoksidasi 2-etilantrahidrokuinon. Dalam metode ini, 2-ethylanthrahydroquinone diekspos ke udara dengan adanya katalis basa, yang mendorong autoksidasi senyawa untuk menghasilkan hidrogen peroksida.
Elektrolisis asam sulfat encer adalah metode lain untuk mensintesis hidrogen peroksida. Dalam metode ini, asam sulfat encer dielektrolisis menggunakan sel elektrolitik khusus, yang menghasilkan hidrogen peroksida di salah satu elektroda.
Hidrogen peroksida juga dapat disintesis dengan metode lain, seperti sintesis langsung dari hidrogen dan oksigen atau reduksi peroksida dengan zat pereduksi. Namun, metode ini tidak umum digunakan untuk produksi hidrogen peroksida komersial karena rendahnya efisiensi dan keamanannya.
Kegunaan Hidrogen Peroksida
Hidrogen peroksida merupakan senyawa kimia serbaguna dengan berbagai aplikasi di berbagai industri. Berikut beberapa kegunaan umum hidrogen peroksida:
- Industri tekstil, kertas dan pulp umumnya menggunakan H2O2 sebagai bahan pemutih untuk menghilangkan warna dari kain dan pulp.
- Fasilitas layanan kesehatan menggunakan H2O2 sebagai disinfektan yang efektif untuk membunuh bakteri, virus, dan jamur serta untuk mensterilkan peralatan dan permukaan medis.
- Instalasi pengolahan air menggunakan H2O2 untuk menghilangkan kotoran seperti besi dan mangan serta untuk mendisinfeksi air.
- Produk pewarna rambut dan pemutih gigi menggunakan H2O2 untuk mencerahkan warna rambut dan gigi.
- Industri dirgantara menggunakan H2O2 sebagai bahan bakar roket.
- Produksi berbagai polimer, seperti polipropilen, polietilen, dan polistiren, melibatkan penggunaan H2O2.
- H2O2 merupakan bahan pembersih yang berguna untuk menghilangkan noda dan kotoran dari permukaan serta membersihkan lensa kontak.
- H2O2 digunakan dalam industri makanan sebagai bahan pemutih dan pengawet produk makanan.
Secara keseluruhan, keserbagunaan H2O2 menjadikannya senyawa kimia berharga yang memiliki banyak aplikasi di berbagai industri.
Pertanyaan:
Harga hidrogen peroksida
Harga hidrogen peroksida dapat sangat bervariasi tergantung pada berbagai faktor seperti kemurnian, konsentrasi, dan jumlah yang dibeli. Secara umum, harga hidrogen peroksida dapat berkisar dari sen per pon untuk hidrogen peroksida tingkat teknis hingga beberapa dolar per pon untuk tingkat kemurnian tinggi yang digunakan dalam aplikasi khusus.
Pada Februari 2023, harga rata-rata 35% hidrogen peroksida food grade adalah sekitar $20 hingga $30 per galon atau $0,10 hingga $0,20 per ons cairan. Hidrogen peroksida tingkat industri dengan kemurnian dan konsentrasi lebih rendah mungkin lebih murah, biasanya antara $1 dan $5 per galon. Namun, harga dapat bervariasi tergantung pada penyedia, wilayah, dan faktor lainnya.
Di mana membeli hidrogen peroksida?
Hidrogen peroksida adalah senyawa kimia umum yang dapat dibeli dari berbagai pemasok, baik online maupun di toko fisik. Berikut beberapa tempat Anda dapat membeli hidrogen peroksida:
- Pemasok Bahan Kimia: Pemasok bahan kimia, seperti Sigma-Aldrich, Fisher Scientific, dan VWR International, menawarkan berbagai kadar dan konsentrasi hidrogen peroksida untuk berbagai aplikasi.
- Pasar Online: Pasar online, seperti Amazon, eBay, dan Alibaba, menawarkan hidrogen peroksida dari berbagai pemasok, dengan kualitas dan konsentrasi berbeda.
- Toko kelontong dan apotek: Banyak toko kelontong dan apotek menjual hidrogen peroksida konsentrasi rendah (3% hingga 6%) sebagai antiseptik untuk pembersihan luka dan pertolongan pertama.
- Toko Perlengkapan Kolam Renang: Hidrogen peroksida dapat digunakan sebagai pengoksidasi kolam dan spa untuk menjaga kejernihan air dan desinfeksi. Toko perlengkapan kolam renang, seperti Leslie’s Pool Supplies, mungkin menjual produk hidrogen peroksida untuk tujuan ini.
