Fenol (C6H5OH) merupakan senyawa kimia yang digunakan dalam berbagai industri. Ia memiliki sifat antiseptik dan juga digunakan dalam produksi plastik, pewarna dan obat-obatan.
| Nama IUPAC | Fenol |
| Formula molekul | C6H6O |
| nomor CAS | 108-95-2 |
| Sinonim | Asam karbol, hidroksibenzena, monohidroksibenzena |
| Di ChI | InChI=1S/C6H6O/c7-6-4-2-1-3-5-6/h1-5.7H |
Sifat fenol
rumus fenol
Rumus fenol adalah C6H6O. Ini terdiri dari enam atom karbon, enam atom hidrogen dan satu atom oksigen. Susunan atom-atom ini memberi fenol sifat kimia yang unik.
Massa Molar Fenol
Massa molar C6H5OH dihitung dengan menjumlahkan massa atom unsur-unsur penyusunnya. C6H5OH memiliki massa molar sekitar 94,11 gram per mol (g/mol). Nilai ini berguna untuk menentukan jumlah C6H5OH dalam sampel tertentu.
Titik didih fenol
C6H5OH memiliki titik didih sekitar 181,7 derajat Celsius (358,1 derajat Fahrenheit). Titik didih yang relatif tinggi ini menunjukkan bahwa C6H5OH berada dalam bentuk cair pada suhu kamar dan memerlukan panas yang signifikan untuk berubah menjadi gas.
Titik Leleh Fenol
Titik leleh C6H5OH kira-kira 40,5 derajat Celcius (104,9 derajat Fahrenheit). Suhu ini menandai transisi C6H5OH dari wujud padat ke wujud cair. Titik leleh yang rendah memungkinkan C6H5OH mudah larut dalam berbagai pelarut.
Kepadatan fenol g/mL
C6H5OH memiliki kepadatan sekitar 1,07 gram per mililiter (g/mL). Nilai massa jenis ini menunjukkan bahwa C6H5OH lebih padat dibandingkan air yang mempunyai massa jenis 1 g/mL. Artinya C6H5OH mengalir dalam air.
Berat Molekul Fenol
Berat molekul C6H5OH dihitung dengan menjumlahkan berat atom atom penyusunnya. C6H5OH memiliki berat molekul sekitar 94,11 gram per mol (g/mol). Nilai ini sangat penting untuk menentukan stoikiometri dan reaksi yang melibatkan C6H5OH.
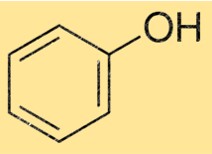
Struktur fenol
Struktur C6H5OH terdiri dari cincin benzena dengan gugus hidroksil (-OH) yang terikat pada salah satu atom karbon. Gugus hidroksil inilah yang memberikan sifat khas pada C6H5OH, menjadikannya senyawa penting dalam berbagai aplikasi industri.
Kelarutan fenol
C6H5OH memiliki kelarutan sedang dalam air. Dapat larut dalam air membentuk larutan bening karena terbentuknya ikatan hidrogen antara molekul C6H5OH dan molekul air. Namun kelarutan C6H5OH menurun dengan adanya senyawa organik nonpolar lainnya.
| Penampilan | Cairan bening dan tidak berwarna |
| Berat jenis | 1,07g/ml |
| Warna | Tanpa warna |
| Bau | Bau khas |
| Masa molar | 94,11 g/mol |
| Kepadatan | 1,07g/ml |
| Titik fusi | 40,5°C (104,9°F) |
| Titik didih | 181,7°C (358,1°F) |
| Titik kilat | 79°C (174°F) |
| Kelarutan dalam air | Larut |
| Kelarutan | Larut dalam pelarut organik |
| Tekanan uap | 0,7 mmHg (20°C) |
| Kepadatan uap | 3.2 (udara = 1) |
| pKa | 9.95 |
| pH | Sekitar 6 |
Keamanan dan bahaya fenol
C6H5OH berpotensi menimbulkan bahaya keselamatan dan harus ditangani dengan hati-hati. Ini bersifat korosif dan dapat menyebabkan luka bakar parah pada kulit dan kerusakan mata jika bersentuhan. Menghirup uap C6H5OH dapat mengiritasi sistem pernapasan dan menyebabkan gangguan pernapasan. Paparan pada konsentrasi tinggi dapat membahayakan organ dalam, termasuk hati, ginjal, dan sistem saraf. C6H5OH juga mudah terbakar dan dapat menyala jika terkena api terbuka atau sumber panas. Penting untuk menggunakan tindakan perlindungan yang tepat seperti sarung tangan, kacamata dan pelindung pernafasan saat bekerja dengan C6H5OH untuk meminimalkan risiko yang terkait dengan penanganan dan penggunaannya.
| Simbol bahaya | Tengkorak dan tulang bersilang, bersifat korosif |
| Deskripsi Keamanan | Menyebabkan luka bakar parah, beracun jika terhirup |
| Nomor identifikasi PBB | UN 1671 (cair), UN 2312 (padat) |
| kode HS | 2907.11.00 |
| Kelas bahaya | Kelas 6.1 (Zat beracun) |
| Kelompok pengepakan | PG II (untuk cairan), PG III (untuk padat) |
| Toksisitas | Sangat beracun dan korosif |
Metode sintesis fenol
C6H5OH dapat disintesis dengan berbagai metode. Metode yang umum adalah proses cumene. Dalam proses ini, benzena dan propilena bereaksi dengan adanya katalis asam, biasanya asam fosfat, menghasilkan kumena. Udara atau oksigen mengoksidasi kumena untuk menghasilkan kumena hidroperoksida, yang mengalami pembelahan untuk menghasilkan C6H5OH dan aseton sebagai produk sampingan.
Metode lainnya adalah proses Dow, yang melibatkan oksidasi langsung benzena menggunakan udara dan katalis oksida logam, seperti tembaga atau mangan. Proses ini menghasilkan C6H5OH dan air sebagai produk utama.
Proses Raschig-Hooker adalah jalur lain untuk sintesis C6H5OH. Ini melibatkan reaksi klorobenzena dengan natrium hidroksida pada suhu dan tekanan tinggi. Proses ini menghasilkan C6H5OH dan natrium klorida.
Hidrolisis garam diazonium yang berasal dari anilin memungkinkan diperolehnya C6H5OH. Proses ini melibatkan reaksi anilin dengan asam nitrat membentuk garam diazonium, yang kemudian mengalami hidrolisis menghasilkan C6H5OH.
Selain itu, terdapat metode alternatif, antara lain oksidasi toluena atau benzena dengan asam nitrat, serta hidrolisis klorobenzena menggunakan uap.
Metode sintesis yang berbeda ini menawarkan jalur berbeda untuk memproduksi C6H5OH, sehingga memungkinkan ketersediaannya di industri dan penerapannya di banyak sektor seperti obat-obatan, plastik, dan pewarna.
Kegunaan fenol
C6H5OH menemukan berbagai aplikasi di beberapa sektor karena sifatnya yang unik. Berikut adalah beberapa kegunaan umum:
- Ini digunakan sebagai antiseptik dalam berbagai produk kesehatan dan desinfektan untuk mencegah infeksi dan mempercepat penyembuhan luka.
- Perusahaan ini menjadi pionir dalam produksi berbagai plastik, termasuk polikarbonat, resin epoksi, dan resin fenolik, yang banyak digunakan dalam industri konstruksi, otomotif, dan kelistrikan.
- C6H5OH berperan penting dalam sintesis obat-obatan farmasi, seperti analgesik, antipiretik, dan antiseptik, sehingga berkontribusi pada bidang medis.
- Produsen menggunakannya dalam pembuatan pewarna sintetis, pigmen dan pewangi untuk menambah warna dan wewangian pada berbagai produk konsumen.
- Turunan C6H5OH digunakan sebagai herbisida untuk mengendalikan pertumbuhan gulma dalam praktik pertanian dan hortikultura.
- Resin fenolik yang berasal dari C6H5OH digunakan dalam produksi perekat, memberikan sifat ikatan yang kuat dalam berbagai aplikasi termasuk pengerjaan kayu dan laminasi.
- Produk kosmetik seperti krim, lotion dan pewarna rambut mengandung C6H5OH karena sifat pengawet dan antioksidannya.
- Dalam industri seperti pengolahan makanan dan manufaktur farmasi, C6H5OH bertindak sebagai pelarut untuk mengekstrak berbagai senyawa termasuk lemak, minyak, dan alkaloid.
- Ini berfungsi sebagai zat antara serbaguna dalam sintesis banyak bahan kimia, termasuk bisphenol-A, kaprolaktam, dan nilon.
- Peneliti menggunakan fenol sebagai reagen laboratorium dalam eksperimen, khususnya dalam studi biokimia dan biologi molekuler.
Beragamnya aplikasi menyoroti pentingnya fenol di berbagai sektor, menjadikannya senyawa berharga dalam berbagai proses industri dan produk konsumen.
Pertanyaan
T: Apa itu fenol?
A: C6H5OH adalah senyawa kimia yang terdiri dari gugus hidroksil (-OH) yang terikat pada cincin benzena.
Q: Apa gugus fungsi alkohol dan fenol?
J: Gugus fungsi alkohol adalah gugus hidroksil (-OH), sedangkan pada C6H5OH gugus hidroksil secara khusus terikat pada cincin benzena.
T: Untuk apa fenol digunakan?
A: C6H5OH digunakan di berbagai industri untuk aplikasi seperti antiseptik, produksi plastik, sintesis farmasi, pewarna, parfum dan sebagai pelarut.
T: Apa itu fenol pKa?
J: PKa C6H5OH kira-kira 9,95, yang menunjukkan sifat asam lemahnya.
T: Apakah fenol termasuk alkohol?
J: Ya, C6H5OH dianggap sebagai alkohol karena adanya gugus fungsi hidroksil (-OH).
Q: Apa itu senyawa fenolik?
A: Senyawa fenolik adalah sekelompok senyawa kimia yang mengandung satu atau lebih cincin fenol dan menunjukkan beragam aktivitas biologis dan sifat antioksidan.
T: Bagaimana cara menghitung total kandungan fenolik?
A: Kandungan total fenolik dapat ditentukan dengan menggunakan berbagai metode spektrofotometri, seperti uji Folin-Ciocalteu, dengan mengukur serapan senyawa fenolik pada panjang gelombang tertentu.
Q: Apakah fenol larut dalam air?
A: Ya, C6H5OH cukup larut dalam air, membentuk larutan bening karena pembentukan ikatan hidrogen dengan molekul air.
Q: Mana yang lebih asam, fenol atau alkohol?
J: C6H5OH lebih asam dibandingkan alkohol karena adanya ion fenoks yang lebih stabil akibat stabilisasi resonansi pada molekul C6H5OH.
