Dimethylamine (DMA) adalah senyawa kimia dengan bau amis. Ini digunakan dalam berbagai proses industri, seperti produksi bahan kimia pertanian, obat-obatan dan surfaktan.
| Nama IUPAC | N-metilmetanamina |
| Formula molekul | C2H7N |
| nomor CAS | 124-40-3 |
| Sinonim | DMA, N-metilmetanamina, dimetilammonia, metilamin, N-metilmetanamina, N-metilmetanamina, N-metilmetanamina hidroklorida |
| Di ChI | InciChI=1S/C2H7N/c1-3-2/h3H,1-2H3 |
Sifat dimetilamin
Rumus dimetilamin
Dimetilamina adalah senyawa organik dengan rumus kimia C2H7N. Ini adalah turunan dari amonia, di mana dua dari tiga atom hidrogen telah digantikan oleh gugus metil. Rumusnya mewakili komposisi molekul dimetilamina, yang mengandung dua atom karbon, tujuh atom hidrogen, dan satu atom nitrogen.
Massa Molar Dimetilamin
Massa molar DMA adalah 45,09 g/mol. Ini adalah molekul yang relatif kecil, yang berkontribusi terhadap titik didih rendah dan tekanan uap tinggi. Massa molar adalah massa satu mol DMA dan dihitung dengan menjumlahkan massa atom semua atom dalam molekul.
Titik didih dimetilamina
Titik didih DMA adalah -6,3°C. Titik didih yang rendah ini membuat DMA menjadi cairan yang mudah menguap dan mudah terbakar. Ia mendidih pada suhu yang lebih rendah dari air, yang berarti mudah menguap jika terkena udara. Titik didih suatu zat adalah suhu saat zat berubah wujud dari cair menjadi gas.
Titik Leleh Dimetilamin
Titik leleh DMA adalah -92°C. Ini adalah cairan tidak berwarna pada suhu kamar tetapi dapat membeku membentuk padatan kristal putih di bawah titik lelehnya. Titik leleh suatu zat adalah suhu perubahan wujud padat menjadi cair.
Kepadatan Dimetilamin g/mL
Kepadatan DMA adalah 0,67 g/mL. Massa jenisnya lebih kecil dibandingkan air, yang massa jenisnya 1 g/mL. Artinya DMA akan mengapung di atas air. Massa jenis suatu zat adalah massa per satuan volume zat tersebut.
Berat Molekul Dimetilamina
Berat molekul DMA adalah 45,09 g/mol. Ini adalah jumlah berat atom semua atom dalam molekul DMA. Berat molekul berguna untuk menentukan berapa banyak suatu zat yang dibutuhkan untuk menghasilkan volume atau konsentrasi tertentu suatu larutan.
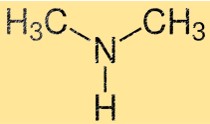
Struktur dimetilamina
Struktur DMA terdiri dari atom nitrogen yang terikat pada dua gugus metil dan satu atom hidrogen. Ini adalah amina primer sederhana dengan bentuk piramidal. Atom nitrogen memiliki sepasang elektron bebas, yang menjadikan DMA sebagai basa lemah.
Kelarutan dimetilamina
DMA larut dalam air, etanol, dan dietil eter. Ini membentuk ikatan hidrogen dengan molekul air, sehingga mudah larut dalam air. Kelarutannya dalam pelarut organik seperti etanol dan dietil eter disebabkan oleh kemampuannya membentuk ikatan hidrogen antarmolekul dengan molekul pelarut.
| Penampilan | Cairan tidak berwarna |
| Berat jenis | 0,666 g/ml pada 25°C |
| Warna | Tanpa warna |
| Bau | Ikan, amonia |
| Masa molar | 45,09 g/mol |
| Kepadatan | 0,666 g/ml pada 25°C |
| Titik fusi | -92°C |
| Titik didih | -6,3°C |
| Titik kilat | -32°C |
| Kelarutan dalam air | Larut dalam air |
| Kelarutan | Larut dalam etanol dan dietil eter |
| Tekanan uap | 522 mmHg pada 20°C |
| Kepadatan uap | 1,53 (udara = 1) |
| pKa | 10.73 |
| pH | 11.1 |
Keamanan dan bahaya dimetilamina
DMA bisa berbahaya jika tidak ditangani dengan benar. Bahan ini sangat mudah terbakar dan mudah terbakar jika terkena panas, percikan api, atau nyala api. Ini juga beracun dan dapat menyebabkan iritasi pada mata, kulit dan sistem pernafasan. Paparan langsung DMA dapat menyebabkan sakit kepala, pusing, dan mual. Penting untuk menggunakan peralatan pelindung seperti sarung tangan, kacamata dan respirator saat menangani DMA. Itu harus disimpan di tempat sejuk dan kering, jauh dari panas dan sumber api. Jika terjadi tumpahan atau paparan, hal tersebut harus ditangani sesuai dengan protokol keselamatan yang sesuai.
| Simbol bahaya | F,T |
| Deskripsi Keamanan | Sangat mudah terbakar, beracun, korosif |
| Nomor identifikasi PBB | PBB 1032 |
| kode HS | 2921.19.00 |
| Kelas bahaya | 2.1 (Gas yang mudah terbakar) |
| Kelompok pengepakan | II |
| Toksisitas | LD50 (oral, tikus) 230 mg/kg; LC50 (inhalasi, tikus) 1660 ppm/4 jam |
Metode sintesis dimetilamina
Ada beberapa metode untuk mensintesis DMA.
Metode yang umum melibatkan mereaksikan metanol dan amonia dengan adanya katalis. Ahli kimia dapat menyaring dan memurnikan produk yang dihasilkan untuk mendapatkan DMA murni.
Metode lain melibatkan reaksi formaldehida dan amonium klorida dengan adanya basa, seperti natrium hidroksida. Reaksi tersebut menghasilkan metilamin, yang kemudian dapat direaksikan dengan formaldehida menghasilkan DMA.
Untuk mensintesis DMA, seseorang dapat bereaksi dengan dimetil sulfat dan amonia . Reaksi ini bersifat eksotermik dan menghasilkan DMA dan amonium sulfat sebagai produk sampingan. Namun, ahli kimia jarang menggunakan metode ini karena sifat dimetil sulfat yang berbahaya.
Untuk mendapatkan DMA, metil klorida dapat direaksikan dengan amonia . Reaksi ini juga menghasilkan amonium klorida sebagai produk sampingan.
Secara keseluruhan, sintesis DMA memerlukan penanganan yang hati-hati dan penggunaan peralatan serta alat pelindung yang tepat karena sifat berbahaya dari bahan mentah dan kondisi reaksi.
Kegunaan Dimetilamina
DMA memiliki beragam aplikasi di berbagai industri karena sifat kimianya yang unik. Berikut beberapa kegunaan umum DMA:
- Industri pertanian: Berbagai herbisida, insektisida dan fungisida menggunakan DEA sebagai perantara dalam produksinya.
- Farmasi: Digunakan sebagai bahan baku sintesis berbagai obat-obatan, termasuk anestesi lokal, antibiotik, dan antihistamin.
- Industri karet: digunakan sebagai akselerator vulkanisasi pada industri karet, yang meningkatkan sifat fisik produk karet.
- Industri Perminyakan: Digunakan sebagai penghambat korosi dan zat penetral dalam penyulingan minyak bumi.
- Pengolahan Air: Digunakan sebagai flokulan dalam pengolahan air untuk menghilangkan padatan tersuspensi dan kotoran lainnya.
- Pelarut: Digunakan sebagai pelarut dalam produksi berbagai bahan kimia, termasuk resin, pewarna dan plastik.
- Industri tekstil: Digunakan sebagai bahan perantara pencelupan dan bahan finishing dalam industri tekstil.
- Perawatan Pribadi: Juga digunakan sebagai bahan dalam berbagai produk perawatan pribadi, termasuk sampo dan kondisioner, karena berfungsi sebagai pengatur pH.
Pertanyaan:
T: Manakah dari berikut ini yang mewakili netralisasi dimetilamina secara menyeluruh?
J: Netralisasi sempurna DMA terjadi ketika ia bereaksi dengan asam klorida membentuk dimetilamonium klorida dan air.
T: Jenis produk apa yang terjadi jika 3-pentanon bereaksi dengan dimetilamina?
A: Ketika 3-pentanon bereaksi dengan DMA, produk yang dihasilkan adalah imina.
T: Apakah dimetilamina aman untuk rambut?
A: DMA umumnya digunakan dalam produk perawatan rambut sebagai pengatur pH dan dianggap aman digunakan pada konsentrasi rendah.
T: Apakah dimetilamina baik untuk rambut?
J: DMA dapat memberikan manfaat bagi rambut bila digunakan dalam produk perawatan rambut dengan konsentrasi yang sesuai, karena dapat membantu meningkatkan efektivitas bahan lainnya.
T: Apa itu dimetilamina?
A: DMA adalah senyawa organik dengan rumus kimia (CH3)2NH. Merupakan gas tidak berwarna dengan bau yang menyengat dan biasa digunakan dalam berbagai proses industri.
T: Apakah berbahan dasar dimetilamina?
A: DMA merupakan basa lemah karena dapat menerima proton dari molekul air untuk membentuk ion hidroksida dan ion metilammonium.
Q: Apakah cetearyl dimethylamine itu cewek keriting?
J: Cetearyl DMA tidak dianggap disetujui oleh gadis keriting, karena merupakan bahan sintetis yang biasa digunakan dalam produk perawatan rambut dan mungkin tidak cocok untuk mereka yang mengikuti metode gadis keriting.
T: Bagaimana cara mengetahui pka dimetilamina?
J: PKa DMA dapat ditemukan secara eksperimental dengan mengukur pH larutan yang konsentrasi DMA dan asam konjugatnya diketahui, dan menggunakan persamaan Henderson-Hasselbalch untuk menghitung nilai pKa.
T: Bagaimana cara menyiapkan 100 ml buffer dengan pH 11,0 dari dimetilamina?
A: Untuk menyiapkan buffer dengan pH 11,0 dari DMA, seseorang perlu mencampurkan sejumlah DMA dengan asam konjugatnya, dimetilamonium klorida, dalam perbandingan tertentu untuk mencapai pH yang diinginkan. Jumlah pastinya bergantung pada kapasitas buffer yang diinginkan dan pKa asam konjugat.
