Bromotimol biru (BTB) adalah indikator pH yang berubah warna dari kuning menjadi biru dengan adanya larutan basa. Ini biasanya digunakan dalam eksperimen ilmiah dan sebagai alat diagnostik medis.
| Nama IUPAC | 3′,3”-dibromotimolsulfonftalein |
| Formula molekul | C27H28Br2O5S |
| nomor CAS | 76-59-5 |
| Sinonim | bromotimol sulfonftalein; 4,4′-(1,1-dioksida-3H-2,1-benzoxathiole-3,3-diil)bis(2-bromo-3-metil-6-(1-metiletil)fenol) |
| Di ChI | InChI=1S/C27H28Br2O5S/c1-13(2)17-11-20(15(5)23(28)18(17)7-9-19(24(20)29)8-10-21(27) 22(30)12-25(31)32)37(33,34)36-26-14(3)6-4-16(35-26)24-7-9-29-11-10-23( 24)28/jam4-7.9-12.31-32H.8H2.1-3H3 |
Massa Molar Biru Bromotimol
BTB memiliki massa molar 624,38 g/mol. Massa molar adalah massa satu mol suatu zat dan biasanya digunakan dalam perhitungan yang melibatkan reaksi kimia. Massa molar BTB dihitung dengan menjumlahkan berat atom seluruh atom dalam rumus kimianya, yaitu C27H28Br2O5S. Mengetahui massa molar suatu zat penting untuk menentukan jumlah zat yang diperlukan untuk suatu reaksi tertentu, serta menentukan jumlah produk yang dihasilkan dalam suatu reaksi.
Titik didih bromotimol biru
BTB memiliki titik didih 636,3°C pada 760 mmHg. Titik didih adalah suhu di mana suatu zat berubah dari wujud cair menjadi gas pada tekanan tertentu. Titik didih BTB yang tinggi menunjukkan bahwa BTB merupakan senyawa stabil yang tidak mudah menguap atau terurai dalam kondisi normal. Titik didih suatu zat dapat digunakan untuk menentukan kemurniannya, karena pengotor dapat mengubah titik didihnya.
Bromotimol biru Titik lebur
BTB memiliki titik leleh 165-170°C. Titik leleh adalah suhu di mana zat padat berubah dari wujud padat menjadi cair. Titik leleh suatu zat digunakan untuk mengidentifikasi dan mengkarakterisasinya, karena zat yang berbeda memiliki titik leleh yang berbeda pula. Titik leleh BTB yang relatif tinggi menunjukkan bahwa BTB merupakan senyawa stabil yang tidak mudah terurai.
Bromotimol biru Massa jenis g/ml
BTB memiliki kepadatan 1,36 g/mL. Massa jenis adalah massa suatu zat per satuan volume dan mengukur seberapa padat molekul-molekul dalam suatu zat. Massa jenis BTB menunjukkan bahwa ia merupakan senyawa yang relatif padat dan biasa digunakan sebagai standar dalam pengukuran massa jenis.
Berat Molekul Biru Bromotimol
Berat molekul BTB adalah 624,38 g/mol. Berat molekul adalah jumlah berat atom seluruh atom dalam suatu molekul dan merupakan faktor penting dalam reaksi kimia. Berat molekul BTB digunakan untuk menentukan jumlah zat yang dibutuhkan untuk suatu reaksi tertentu, serta untuk menentukan jumlah produk yang dihasilkan dalam suatu reaksi.
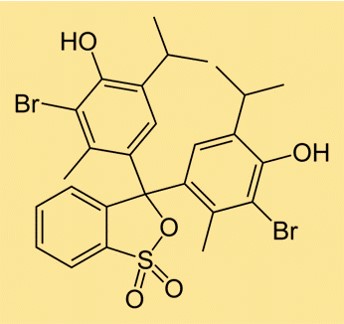
Struktur bromotimol biru
Struktur BTB terdiri dari dua cincin aromatik yang masing-masing memiliki atom brom yang terikat. Ada juga gugus sulfonat yang menempel pada salah satu cincin, yang membuat molekulnya larut dalam air. Struktur BTB mirip dengan indikator pH lainnya, digunakan untuk menentukan keasaman atau kebasaan suatu larutan.
Formula Bromotimol Biru
Rumus kimia BTB adalah C27H28Br2O5S. Rumusnya menunjukkan jumlah dan jenis atom dalam molekul dan digunakan dalam reaksi kimia untuk menentukan jumlah zat yang dibutuhkan untuk suatu reaksi tertentu. Rumus BTB menunjukkan bahwa ia mengandung dua atom bromin, yang memberikan warna khas kuning-hijau dalam larutan asam, dan gugus sulfonat, yang membuatnya larut dalam air.
| Penampilan | Bubuk hijau tua |
| Berat jenis | 1.36 |
| Warna | hijau kekuningan |
| Bau | Tidak berbau |
| Masa molar | 624,38 g/mol |
| Kepadatan | 1,36g/ml |
| Titik fusi | 165-170°C |
| Titik didih | 636,3°C pada 760 mmHg |
| Titik kilat | Tak dapat diterapkan |
| Kelarutan dalam air | Larut |
| Kelarutan | Larut dalam etanol, sedikit larut dalam eter dan kloroform |
| Tekanan uap | Tak dapat diterapkan |
| Kepadatan uap | Tak dapat diterapkan |
| pKa | 6.3 |
| pH | Kuning pada pH 6,0, hijau pada pH 7,6, biru pada pH 7,9 |
Keamanan dan bahaya bromotimol biru
BTB bisa berbahaya jika tertelan, terhirup, atau terserap melalui kulit. Hal ini dapat menyebabkan iritasi pada mata, kulit, dan sistem pernapasan. Penelanan dapat menyebabkan iritasi gastrointestinal, mual, muntah dan sakit perut. Menghirup debu atau uap BTB dapat menyebabkan iritasi pernafasan, batuk dan kesulitan bernafas. Zat tersebut juga mungkin berbahaya bagi kehidupan akuatik dan tidak boleh dibuang ke sumber air. Alat pelindung diri yang sesuai, seperti sarung tangan dan pelindung mata, harus dipakai saat menangani BTB, dan harus digunakan serta dibuang sesuai dengan prosedur dan peraturan laboratorium yang sesuai.
| Simbol bahaya | Tidak ada |
| Deskripsi Keamanan | S22: Jangan menghirup debu. S24/25: Hindari kontak dengan kulit dan mata. S36/37/39: Kenakan pakaian pelindung, sarung tangan, dan pelindung mata/wajah yang sesuai. |
| Sebuah pengidentifikasi | Tidak diatur |
| kode HS | 2921.59.90 |
| Kelas bahaya | Tidak diklasifikasikan |
| Kelompok pengepakan | Tak dapat diterapkan |
| Toksisitas | LD50 (oral, tikus) = 4,500 mg/kg |
Metode sintesis bromotimol biru
Ada berbagai metode untuk mensintesis BTB.
Metode yang umum adalah reaksi antara timol biru dan bromin dengan adanya katalis asam kuat, seperti asam klorida. Reaksi berlangsung dengan adisi elektrofilik brom ke molekul timol biru, diikuti dengan substitusi atom hidrogen dengan atom brom. Senyawa yang dihasilkan adalah BTB.
Metode lain melibatkan reaksi antara 2,6-dibromoindofenol dan kresol merah dengan adanya katalis asam kuat. Reaksi terjadi melalui substitusi elektrofilik atom hidrogen pada molekul merah kresol dengan atom brom pada molekul 2,6-dibromoindofenol. Senyawa yang dihasilkan adalah BTB.
Metode ketiga melibatkan reaksi antara timol biru dan natrium bromida dengan adanya natrium hidroksida. Reaksi terjadi dengan mensubstitusi atom hidrogen dalam molekul timol biru dengan atom brom dari molekul natrium bromida. Senyawa yang dihasilkan adalah BTB.
Apapun metode yang digunakan, produk yang dihasilkan harus dimurnikan dengan rekristalisasi atau kromatografi kolom untuk mendapatkan BTB murni.
Kegunaan Bromotimol Biru
BTB memiliki beberapa aplikasi di berbagai bidang. Beberapa kegunaan BTB antara lain:
- Indikator: Digunakan sebagai indikator asam basa, dengan kisaran pH 6,0 hingga 7,6. Pada pH 6,0 berwarna kuning, pada pH 7,6 berwarna hijau, dan pada pH 7,9 berwarna biru.
- Eksperimen Laboratorium: Digunakan dalam berbagai eksperimen laboratorium untuk menguji keberadaan karbon dioksida dan gas lainnya dan untuk menentukan hasil bagi pernapasan.
- Budidaya Perairan: Digunakan dalam budidaya perairan untuk memantau tingkat pH air di akuarium dan kolam.
- Bidang Medis: Digunakan untuk menguji keberadaan empedu dalam sampel urin dan untuk mendeteksi adanya infeksi jamur.
- Pendidikan: Digunakan dalam pendidikan sebagai alat bantu visual untuk menunjukkan prinsip-prinsip reaksi asam-basa dan untuk mengajar siswa tentang tingkat pH.
- Industri Pertanian: Digunakan untuk mengukur tingkat pH tanah, merupakan faktor penting dalam menentukan kesehatan dan pertumbuhan tanaman.
- Pengujian Lingkungan: Digunakan dalam pengujian lingkungan untuk mengukur tingkat pH sumber air, seperti danau dan sungai, untuk memastikan kesesuaiannya untuk kehidupan akuatik.
Secara keseluruhan, BTB merupakan senyawa serbaguna dengan banyak aplikasi di berbagai bidang.
Pertanyaan:
T: Apa itu bromotimol biru?
A: BTB adalah indikator pH yang biasa digunakan dalam percobaan laboratorium dan berbagai aplikasi lainnya. Ini adalah senyawa kimia yang berubah warna tergantung pada keasaman atau alkalinitas suatu larutan.
T: Berapa kisaran pH bromotimol biru?
J: Kisaran pH BTB adalah antara 6,0 dan 7,6. Pada pH 6,0 berwarna kuning, pada pH 7,6 berwarna hijau, dan pada pH 7,9 berwarna biru.
T: Apa perubahan warna biru bromotimol?
A: Perubahan warna BTB tergantung pada pH larutan. Pada pH 6,0 berwarna kuning, pada pH 7,6 berwarna hijau, dan pada pH 7,9 berwarna biru.
Q: Apakah bromotimol biru termasuk asam atau basa? Jawaban: BTB bukanlah asam atau basa. Ini adalah indikator yang berubah warna tergantung pada keasaman atau alkalinitas suatu larutan.
