Asetil klorida atau C2H3ClO adalah cairan tidak berwarna dan berasap dengan bau yang menyengat. Hal ini terutama digunakan sebagai reagen dalam sintesis organik dan sebagai agen asetilasi dalam produksi obat-obatan dan pewarna.
| Nama UPAC | Asetil klorida |
| Formula molekul | C2H3ClO |
| nomor CAS | 75-36-5 |
| Sinonim | Etanoil klorida, asam asetat klorida, asetat klorida, kloroasetil klorida, AcCl |
| Di ChI | InChI=1S/C2H3ClO/c1-2(3)4/h1H3 |
Sifat Asetil Klorida
Massa Molar Asetil Klorida
Asetil klorida, dengan rumus kimia C2H3ClO, memiliki massa molar sekitar 78,50 g/mol. Ini dihitung dengan menjumlahkan massa atom setiap atom dalam molekul, yaitu karbon (12,01 g/mol), hidrogen (1,01 g/mol), klor (35,45 g/mol) dan oksigen (16,00 g/mol). Massa molar asetil klorida penting dalam perhitungan stoikiometri untuk menentukan jumlah reaktan dan produk dalam reaksi kimia.
Titik didih asetil klorida
Titik didih asetil klorida adalah 51,5°C (124,7°F) pada tekanan atmosfer standar. Titik didih yang rendah ini, ditambah dengan sifatnya yang sangat reaktif, berarti asetil klorida harus ditangani dengan hati-hati di laboratorium. Ini adalah cairan berasap tidak berwarna dengan bau menyengat yang sangat larut dalam pelarut polar seperti etanol dan aseton.
Titik Leleh Asetil Klorida
C2H3ClO memiliki titik leleh -112,1°C (-169,8°F) pada tekanan atmosfer standar. Hal ini menjadikannya senyawa yang sangat mudah menguap dan reaktif sehingga memerlukan penanganan dan penyimpanan yang hati-hati.
Massa jenis asetil klorida g/mL
Asetil klorida memiliki kepadatan 1,104 g/mL pada 25°C (77°F). Artinya C2H3ClO lebih padat dari air dan akan tenggelam di dalamnya. Kepadatan C2H3ClO penting dalam menentukan berapa banyak material yang dapat disimpan dalam volume tertentu, serta tindakan keselamatan yang diperlukan untuk menangani dan menyimpan material tersebut.
Berat Molekul Asetil Klorida
Berat molekul C2H3ClO adalah 78,50 g/mol. Nilai ini penting untuk menentukan jumlah C2H3ClO yang dibutuhkan dalam reaksi kimia dan untuk mengkonversi satuan pengukuran yang berbeda.
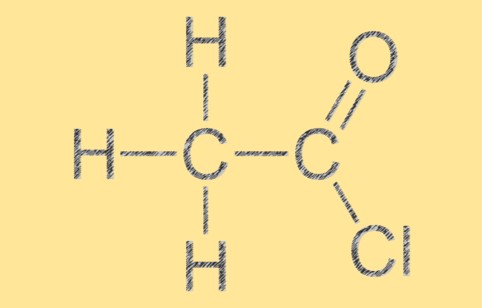
Struktur Asetil Klorida
Asetil klorida memiliki geometri molekul trigonal planar, dengan atom karbon di tengah dikelilingi oleh tiga atom lainnya dalam susunan segitiga datar. Molekul tersebut memiliki ikatan rangkap C=O antara atom karbon dan oksigen dan ikatan tunggal antara atom karbon dan klor. Struktur molekul C2H3ClO memberikan karakteristik reaktivitas dan sifat kimianya.
Rumus Asetil Klorida
Rumus kimia asetil klorida adalah C2H3ClO, yang mewakili jumlah dan jenis atom dalam molekul. Rumusnya penting untuk perhitungan stoikiometri dalam reaksi kimia dan untuk mengidentifikasi senyawa di laboratorium. C2H3ClO terutama digunakan sebagai reagen dalam sintesis organik dan sebagai agen asetilasi dalam produksi obat-obatan dan pewarna.
| Penampilan | Cairan tidak berwarna |
| Berat jenis | 1,104 g/ml pada 25°C |
| Warna | Tanpa warna |
| Bau | hektar |
| Masa molar | 78,50 g/mol |
| Kepadatan | 1,104 g/ml pada 25°C |
| Titik fusi | -112,1°C |
| Titik didih | 51,5°C |
| Titik kilat | -26°C |
| Kelarutan dalam air | Bereaksi hebat dengan air |
| Kelarutan | Larut dalam sebagian besar pelarut organik |
| Tekanan uap | 69,7 mmHg pada 25°C |
| Kepadatan uap | 2.7 (udara=1) |
| pKa | -6.3 |
| pH | Sangat asam |
Keamanan dan Bahaya Asetil Klorida
C2H3ClO adalah zat yang sangat reaktif dan berbahaya yang menimbulkan risiko signifikan terhadap kesehatan dan keselamatan manusia. Ini adalah zat korosif dan beracun yang dapat menyebabkan luka bakar parah pada kulit, kerusakan mata, dan iritasi pernafasan jika terpapar. Asetil klorida juga dapat bereaksi hebat dengan air, menghasilkan gas asam klorida, yang dapat mengiritasi saluran pernapasan. Penting untuk menangani C2H3ClO dengan sangat hati-hati, memakai alat pelindung diri yang sesuai dan hanya menggunakannya di area yang berventilasi baik. Penyimpanan, pelabelan, dan pengangkutan yang tepat juga penting untuk mencegah kecelakaan dan memastikan penanganan yang aman terhadap bahan ini.
| Simbol bahaya | Korosif, Beracun |
| Deskripsi Keamanan | Jangan menghirup uapnya. Kenakan sarung tangan pelindung dan pelindung mata/wajah. Jika terjadi kebakaran, gunakan alat pemadam CO2, bahan kimia kering, atau busa. |
| Sebuah pengidentifikasi | UN1717 |
| kode HS | 2915.90.9000 |
| Kelas bahaya | 8 |
| Kelompok pengepakan | II |
| Toksisitas | Sangat beracun dan korosif. Menyebabkan luka bakar parah pada kulit dan mata. Mungkin berakibat fatal jika terhirup atau tertelan. |
Metode sintesis asetil klorida
C2H3ClO dihasilkan dengan mereaksikan asam asetat dengan tionil klorida, fosfor triklorida, atau fosfor pentaklorida. Metode ini melibatkan penggunaan reagen yang sangat reaktif dan berbahaya dan harus digunakan dengan sangat hati-hati.
Metode sintesis C2H3ClO yang paling umum melibatkan reaksi asam asetat dengan tionil klorida. Metode ini biasanya melibatkan penambahan tionil klorida ke asam asetat secara terkendali, dengan kontrol suhu yang cermat untuk mencegah panas berlebih dan dekomposisi. Reaksi tersebut menghasilkan C2H3ClO dan gas sulfur dioksida sebagai produk sampingan.
Metode lain untuk mensintesis C2H3ClO melibatkan reaksi asam asetat dengan fosfor triklorida atau fosfor pentaklorida. Dalam metode ini, asam asetat dicampur dengan fosfor triklorida atau fosfor pentaklorida dan dipanaskan untuk memulai reaksi. Reaksi menghasilkan C2H3ClO dan asam fosfat sebagai produk sampingan.
Penting untuk dicatat bahwa metode ini melibatkan penggunaan bahan kimia yang sangat reaktif dan berbahaya dan harus dilakukan hanya oleh ahli kimia berpengalaman di area yang berventilasi baik dan dilengkapi dengan peralatan pelindung diri yang sesuai. Selain itu, sintesis C2H3ClO harus dilakukan di bawah lemari asam untuk meminimalkan paparan gas beracun dan korosif.
Kegunaan Asetil Klorida
Asetil klorida adalah senyawa kimia serbaguna yang banyak digunakan dalam industri dan penelitian. Beberapa kegunaan umum C2H3ClO adalah:
- Produksi obat-obatan: Berbagai produk farmasi, termasuk obat penghilang rasa sakit, antibiotik, dan anestesi, menggunakan C2H3ClO dalam sintesisnya.
- Produksi pewarna dan parfum: Produksi berbagai pewarna dan parfum, seperti kumarin yang digunakan dalam parfum dan sabun, melibatkan penggunaan C2H3ClO.
- Produksi Polimer: Produksi berbagai polimer seperti polikarbonat dan polivinil klorida yang dihubungkan pada C2H3ClO sebagai reaktan.
- Produksi turunan asetat: C2H3ClO memainkan peran penting dalam produksi senyawa turunan asetat seperti asam amino dan alkohol.
- Reaksi Kimia: C2H3ClO menunjukkan reaktivitas yang tinggi, menjadikannya reagen yang berharga dalam berbagai reaksi kimia, termasuk reaksi asetilasi dan reaksi Friedel-Crafts.
- Penelitian Laboratorium: C2H3ClO sering digunakan dalam penelitian laboratorium sebagai reagen untuk reaksi kimia dan sebagai pelarut untuk berbagai senyawa.
Penting untuk diingat bahwa C2H3ClO adalah zat berbahaya dan harus ditangani dengan sangat hati-hati. Protokol dan peraturan keselamatan yang tepat harus diikuti saat menggunakan C2H3ClO untuk meminimalkan risiko yang terkait dengan penanganan dan penggunaannya.
