Asam fluoroantimonat adalah salah satu asam super paling kuat yang diketahui, dengan fungsi keasaman Hammett -21. Ini adalah campuran hidrogen fluorida dan antimon pentafluorida.
| Nama IUPAC | Asam fluoroantimon (V) |
| Formula molekul | H[SbF6] |
| nomor CAS | 16950-06-4 |
| Sinonim | Hidrogen heksafluoroantimonat (V), Antimon heksafluorida terhidrasi, Antimon hidrogen fluorida, Asam hidrofluorat dengan pentafluoroantimon (1:1) |
| Di ChI | InChI=1S/F6Sb.H/h1H;/q+1;/p-1 |
pH asam fluoroantimonat
Asam fluoroantimonat adalah asam super dan memiliki pH di bawah -14. Hal ini karena skala pH mengukur konsentrasi ion hidrogen (H+) dalam larutan dan superasam memiliki konsentrasi ion H+ lebih tinggi daripada air murni.
Pengukur pH tradisional tidak dapat mengukur pH asam fluoroantimonat secara akurat karena tidak dirancang untuk menangani asam kuat tersebut. Sebaliknya, para ilmuwan menggunakan fungsi keasaman Hammett untuk mengukur keasaman asam fluoroantimonic. Fungsi keasaman Hammett membandingkan keasaman superasam menggunakan derajat protonasi senyawa referensi. Asam fluoroantimonat memiliki fungsi keasaman Hammett -21, yang merupakan nilai paling negatif dan menunjukkan bahwa ia adalah salah satu superasam paling kuat yang diketahui.
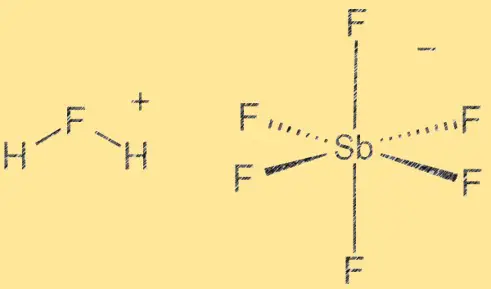
Struktur asam fluoroantimonat:
Asam fluoroantimonat memiliki struktur molekul yang terdiri dari ion hidrogen (H+) dan ion heksafluoroantimonat (V) ([SbF6]^-). Ion SbF6 berperan sebagai asam Lewis, sedangkan ion H+ berperan sebagai asam Bronsted. Senyawa ini sangat polar karena perbedaan keelektronegatifan antara atom hidrogen dan fluor. Ikatan antara antimon dan fluorida bersifat kovalen, sedangkan ikatan antara hidrogen dan fluorida bersifat kovalen polar.
Massa molar Asam Fluoroantimonic:
Asam fluoroantimonat memiliki massa molar 216,74 g/mol. Ini adalah superasam yang sangat reaktif dan korosif yang terdiri dari hidrogen fluorida (HF) dan antimon pentafluorida (SbF5). Massa molar asam fluoroantimonat yang tinggi dapat dikaitkan dengan adanya atom antimon yang berat dalam struktur molekulnya.
Titik didih asam fluoroantimonat:
HSbF6 adalah senyawa yang sangat reaktif dan tidak stabil sehingga tidak memiliki titik didih tertentu. Ia terurai pada suhu di atas -10°C, melepaskan asap beracun berupa gas hidrogen fluorida. Titik didihnya diperkirakan sekitar 20-30°C, tetapi ini bukan parameter yang berguna untuk menggambarkan sifat HSbF6.
Titik lebur asam fluoroantimonat:
HSbF6 tidak memiliki titik leleh yang jelas karena sifatnya yang sangat reaktif. Itu hanya bisa ada dalam keadaan cair dan terurai dengan cepat saat didinginkan ke suhu yang lebih rendah. Diperkirakan terurai sekitar -90°C, melepaskan asap beracun hidrogen fluorida dan antimon pentafluorida.
Massa jenis asam fluoroantimonat g/ml:
Massa jenis HSbF6 adalah 2,1 g/mL. Kepadatan tinggi ini dapat dikaitkan dengan adanya atom antimon berat dalam struktur molekulnya. Ini adalah senyawa yang sangat korosif dan reaktif dan harus ditangani dengan sangat hati-hati. Kepadatan HSbF6 juga menyulitkan penanganan di laboratorium.
Berat molekul asam fluoroantimonat:
Berat molekul asam fluoroantimonat adalah 236,76 g/mol. Ini terdiri dari satu ion hidrogen, satu ion antimon dan enam ion fluorida. Berat molekul asam fluoroantimonat yang tinggi dapat dikaitkan dengan adanya atom antimon yang berat dalam struktur molekulnya.
Rumus Asam Fluoroantimonat:
Rumus kimia asam fluoroantimonat adalah H[SbF6]. Ia terdiri dari ion hidrogen (H+) dan ion heksafluoroantimonat (V) ([SbF6]^-). Ion [SbF6]^- dibentuk oleh reaksi antimon pentafluorida (SbF5) dengan hidrogen fluorida (HF). Rumusnya mewakili rasio bilangan bulat paling sederhana dari atom-atom yang ada dalam senyawa.
| Penampilan | Cairan tidak berwarna sampai kuning pucat |
| Berat jenis | 2.1g/ml |
| Warna | Tidak berwarna sampai kuning pucat |
| Bau | Tidak berbau |
| Masa molar | 236,76 g/mol |
| Kepadatan | 2.1g/ml |
| Titik fusi | Terurai sekitar -90°C |
| Titik didih | Terurai di atas -10°C |
| Titik kilat | Tak dapat diterapkan |
| Kelarutan dalam air | Bereaksi hebat dengan air |
| Kelarutan | Larut dalam HF anhidrat, SbF5, SO2F2 dan SO2ClF |
| Tekanan uap | Tak dapat diterapkan |
| Kepadatan uap | Tak dapat diterapkan |
| PKa | -21 (fungsi keasaman Hammett) |
| pH | Kurang dari -14 |
Catatan: Asam fluoroantimonat adalah senyawa yang sangat reaktif dan korosif sehingga harus ditangani dengan sangat hati-hati. Sifat fisik dan kimianya sulit diukur secara akurat karena sifatnya yang tidak stabil dan terbatasnya metode manipulasi yang tersedia. Nilai yang tercantum dalam tabel ini merupakan perkiraan berdasarkan literatur yang tersedia dan mungkin tidak tepat.
Keamanan dan Bahaya Asam Fluoroantimonic
Asam fluoroantimonat adalah zat yang sangat berbahaya dan sangat korosif yang menimbulkan risiko kesehatan dan keselamatan yang signifikan. Ini adalah zat pengoksidasi kuat yang dapat bereaksi hebat dengan air, senyawa organik, dan bahkan beberapa logam. Bahan ini dapat menyebabkan luka bakar parah dan kerusakan jaringan jika terkena kulit atau mata, dan menghirup uapnya dapat menyebabkan gangguan pernapasan dan kerusakan paru-paru.
Personil yang terlatih harus menangani asam fluoroantimonic menggunakan peralatan khusus dan pakaian pelindung di laboratorium yang berventilasi baik dan dilengkapi dengan baik. Badan pengatur secara ketat mengatur dan membatasi penggunaan asam fluoroantimonic karena potensinya menyebabkan cedera serius dan kerusakan lingkungan.
| Simbol bahaya | Korosif |
| Deskripsi Keamanan | Jangan menghirup uapnya. Kenakan sarung tangan, pakaian dan pelindung mata/wajah. Hindari kontak dengan kulit, mata dan pakaian. Gunakan hanya di bawah tudung kimia. |
| Nomor identifikasi PBB | UN3264 |
| kode HS | 28111990 |
| Kelas bahaya | 8 (Zat korosif) |
| Kelompok pengepakan | AKU AKU AKU |
| Toksisitas | Sangat beracun dan korosif; dapat menyebabkan luka bakar parah dan kerusakan jaringan jika terkena kulit atau mata, dan menghirup uapnya dapat menyebabkan gangguan pernapasan dan kerusakan paru-paru. |
Metode sintesis asam fluoroantimonat
Asam fluoroantimonat (HSbF6) biasanya disintesis dengan mencampurkan hidrogen fluorida (HF) dan antimon pentafluorida (SbF5) dengan perbandingan molar 1:1. Reaksi berlangsung dalam kondisi anhidrat dan pada suhu rendah untuk mencegah dekomposisi asam super yang dihasilkan. Reaksi keseluruhan dapat direpresentasikan sebagai berikut:
HF + SbF5 → HSbF6
Reaksinya sangat eksotermis dan dapat melepaskan sejumlah besar panas. Oleh karena itu, biasanya dilakukan di lingkungan yang berventilasi baik dan terkendali, seperti lemari asam kimia, dengan menggunakan tindakan perlindungan yang tepat.
Untuk menyiapkan HSbF6, antimon trifluorida (SbF3) dapat direaksikan dengan HF dengan adanya zat pengoksidasi seperti SbF5 atau sulfur dioksida difluorida (SO2F2). Reaksi ini memerlukan kondisi anhidrat dan suhu rendah. Reaksinya dapat dinyatakan sebagai berikut:
SbF3 + 3HF + SO2F2 → HSbF6 + SO2
HSbF6 merupakan senyawa yang sangat reaktif dan tidak stabil sehingga memerlukan penanganan dan penyimpanan khusus. Biasanya disimpan dalam wadah tertutup rapat dan kedap udara dalam kondisi anhidrat dan pada suhu rendah untuk mencegah dekomposisi. Tindakan keselamatan dan peralatan pelindung yang tepat sangat penting saat bekerja dengan HSbF6 karena toksisitas dan korosifitasnya yang tinggi.
Kegunaan Asam Fluoroantimonic
Asam Fluoroantimonat (HSbF6) adalah salah satu superasam paling ampuh yang diketahui dan memiliki beragam aplikasi industri dan penelitian. Berikut beberapa kegunaan asam fluoroantimonic:
- HSbF6 berfungsi sebagai katalis dalam berbagai reaksi kimia, termasuk alkilasi, isomerisasi, dan polimerisasi.
- Industri petrokimia menggunakan HSbF6 dalam produksi bensin beroktan tinggi dan hidrokarbon lainnya.
- Para peneliti di industri farmasi menggunakan HSbF6 sebagai katalis dalam sintesis berbagai produk farmasi, termasuk obat antivirus dan antikanker.
- HSbF6 dapat diterapkan dalam pengetsaan dan pembersihan komponen elektronik, seperti microchip dan semikonduktor, yang digunakan dalam produksi komponen elektronik.
- Para ilmuwan menggunakan HSbF6 sebagai alat penelitian di berbagai bidang ilmu kimia dan material, termasuk sintesis material baru dan studi reaksi kimia.
HSbF6 adalah zat yang sangat reaktif dan berbahaya sehingga memerlukan penanganan khusus dan tindakan perlindungan. Obat ini diatur secara ketat dan hanya boleh digunakan oleh personel terlatih di laboratorium yang dilengkapi dengan baik. Potensi bahaya yang terkait dengan HSbF6 membatasi penggunaannya pada aplikasi khusus yang tidak tersedia alternatif lain.
Pertanyaan:
Bisakah asam fluoroantimonat melarutkan berlian?
HSbF6 dapat melarutkan intan karena sifat asamnya yang kuat. Para profesional terlatih di laboratorium yang lengkap dengan tindakan keselamatan dan peralatan pelindung yang tepat dapat melakukan reaksi yang sangat berbahaya antara berlian dan HSbF6. Namun, ini bukanlah metode yang praktis atau hemat biaya untuk pemrosesan atau pemotongan berlian. Pemotongan mekanis atau pemotongan laser lebih umum digunakan karena efisiensi dan keamanannya.
Di mana membeli asam fluoroantimonat?
Membeli HSbF6 sangat sulit karena sifatnya yang sangat berbahaya dan diatur. Hanya perusahaan atau lembaga yang disetujui dan diberi wewenang dengan izin dan peralatan yang diperlukan yang dapat menangani dan menyimpan asam dengan aman.
Konvensi Senjata Kimia (CWC) dan peraturan Standar Anti-Terorisme Fasilitas Kimia AS (CFATS) mengklasifikasikan HSbF6 sebagai zat berbahaya dan terkendali.
Instansi pemerintah seperti Badan Perlindungan Lingkungan (EPA), Departemen Keamanan Dalam Negeri (DHS), dan Biro Industri dan Keamanan (BIS) mengatur dan mengontrol secara ketat penjualan dan pembelian HSbF6.
Jika Anda memiliki kebutuhan yang sah untuk HSbF6, Anda dapat menghubungi pemasok bahan kimia atau lembaga penelitian yang disetujui dengan izin dan keahlian yang diperlukan.
Namun, Anda harus memberikan alasan rinci dan mendapatkan persetujuan dan izin yang diperlukan sebelum melakukan pembelian apa pun.
