Magnesium hipoklorit (Mg(ClO)2) adalah senyawa kimia yang tersusun dari magnesium, oksigen dan klorin. Ini digunakan sebagai bahan kimia desinfektan, pemutih dan pengolahan air.
| Nama IUPAC | Magnesium hipoklorit |
| Formula molekul | Mg(ClO)2 |
| nomor CAS | 10233-03-1 |
| Sinonim | Magnesium klorat, garam magnesium dari asam hipoklorit, magnesium oksiklorida, MagOCl |
| Di ChI | InChI=1S/Cl2O2.Mg/c1-3-2;/q-1;+2 |
Sifat magnesium hipoklorit
Formula Magnesium Hipoklorit
Magnesium hipoklorit memiliki rumus kimia Mg(ClO)2 yang berarti mengandung satu atom magnesium, dua atom klor, dan dua atom oksigen per molekul. Ini adalah padatan putih dengan sedikit bau klorin dan biasanya digunakan sebagai desinfektan dan bahan kimia pengolahan air.
Massa Molar Magnesium Hipoklorit
Massa molar Mg(ClO)2 adalah 127,21 g/mol. Nilai tersebut dihitung dengan menjumlahkan massa atom setiap unsur pada rumus kimianya, yaitu magnesium (24,31 g/mol), klor (35,45 g/mol), dan oksigen (15,99 g/mol). mol), dikalikan dengan indeksnya masing-masing.
Titik didih magnesium hipoklorit
Mg(ClO)2 tidak memiliki titik didih tertentu karena terurai sebelum mencapai titik didihnya. Ketika dipanaskan, Mg(ClO)2 melepaskan gas oksigen, meninggalkan magnesium klorida sebagai residu padat.
Titik lebur magnesium hipoklorit
Titik leleh Mg(ClO)2 adalah 100°C. Pada suhu ini, kristal Mg(ClO)2 padat berubah menjadi cair. Namun karena ketidakstabilannya pada suhu tinggi, disarankan untuk menanganinya dengan hati-hati.
Massa jenis magnesium hipoklorit g/mL
Massa jenis Mg(ClO)2 adalah 2,08 g/mL pada suhu kamar. Artinya satu mililiter Mg(ClO)2 mempunyai massa 2,08 gram.
Berat Molekul Magnesium Hipoklorit
Berat molekul Mg(ClO)2 adalah 127,21 g/mol. Ini adalah jumlah berat atom seluruh unsur dalam senyawa, yaitu magnesium, klor, dan oksigen.
Struktur magnesium hipoklorit
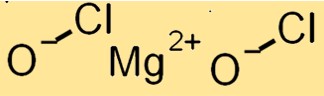
Mg(ClO)2 memiliki struktur kristal dengan sistem kristal monoklinik. Ini terdiri dari kation Mg+2 dan anion ClO, yang disatukan oleh ikatan ionik. Anion ClO berada dalam susunan tetrahedral yang terdistorsi di sekitar kation Mg+2.
Kelarutan magnesium hipoklorit
Mg(ClO)2 sedikit larut dalam air, dengan kelarutan 14,6 g/100 mL pada 20°C. Ini membentuk larutan sedikit basa dalam air karena hidrolisis ion hipoklorit. Namun tidak disarankan untuk melarutkan Mg(ClO)2 ke dalam air karena dapat menghasilkan gas klorin yang bersifat racun dan berbahaya bagi kesehatan manusia.
| Penampilan | Padatan putih |
| Berat jenis | 2,08 g/mL pada 20°C |
| Warna | Putih |
| Bau | Diklorinasi ringan |
| Masa molar | 127,21 g/mol |
| Kepadatan | 2,08 g/mL pada 20°C |
| Titik fusi | 100°C |
| Titik didih | Terurai sebelum mencapai titik didih |
| Titik kilat | Tak dapat diterapkan |
| Kelarutan dalam air | Sedikit larut (14,6 g/100 mL pada 20°C) |
| Kelarutan | Sedikit larut dalam air, larut dalam asam |
| Tekanan uap | Tak dapat diterapkan |
| Kepadatan uap | Tak dapat diterapkan |
| pKa | Tak dapat diterapkan |
| pH | Solusi yang sedikit mendasar |
Keamanan dan Bahaya Magnesium Hipoklorit
Mg(ClO)2 bisa berbahaya jika tidak ditangani dengan benar. Ini adalah zat pengoksidasi kuat yang dapat bereaksi hebat dengan bahan kimia tertentu. Kontak dengan kulit, mata dan selaput lendir dapat menyebabkan iritasi dan luka bakar. Menghirup debu atau kabut dapat menyebabkan masalah pernapasan. Penting juga untuk menghindari pencampuran Mg(ClO)2 dengan asam atau senyawa lain yang mengandung klor, karena dapat menghasilkan gas klor beracun. Disarankan untuk memakai peralatan pelindung seperti sarung tangan dan kacamata saat menangani Mg(ClO)2 dan menyimpannya di tempat sejuk dan kering, jauh dari bahan kimia yang tidak kompatibel.
| Simbol bahaya | Agen pengoksidasi, berbahaya |
| Deskripsi Keamanan | Jauhkan dari panas, percikan api, dan nyala api terbuka. Jangan menghirup debu atau kabut. Kenakan sarung tangan dan kacamata pelindung. |
| Nomor identifikasi PBB | tahun 1748 |
| kode HS | 2828.10.10 |
| Kelas bahaya | 5.1 (Agen pengoksidasi), 6.1 (Beracun) |
| Kelompok pengepakan | II |
| Toksisitas | LD50 (oral, tikus) – 290 mg/kg; LC50 (inhalasi, tikus) – 2,07 mg/L/4 jam; Iritasi kulit – Ringan; Iritasi mata – Parah |
Metode sintesis magnesium hipoklorit
Untuk mensintesis Mg(ClO)2, metode yang paling umum digunakan adalah dengan mereaksikan magnesium oksida dengan gas klor.
Dalam salah satu metode, untuk menghasilkan Mg(ClO)2, magnesium oksida harus dicampur dengan gas klor dengan adanya air. Pengendalian yang cermat diperlukan selama reaksi eksotermik untuk menghindari pembentukan produk sampingan yang tidak diinginkan.
Metode lain melibatkan reaksi antara magnesium hidroksida dan asam hipoklorit. Untuk menjaga pH, reaksi biasanya berlangsung dalam larutan natrium hidroksida. Larutan Mg(ClO)2 yang dihasilkan dapat dipisahkan dengan penyaringan dan kemudian dikeringkan setelah reaksi.
Metode ketiga melibatkan reaksi antara magnesium karbonat dan asam hipoklorit. Reaksi ini menghasilkan Mg(ClO)2 dan karbon dioksida. Untuk menghindari pembentukan produk sampingan yang tidak diinginkan, reaksi harus dipantau secara cermat.
Terlepas dari metode sintesis yang digunakan, penting untuk menangani Mg(ClO)2 dengan hati-hati karena sifat pengoksidasi dan potensi bahayanya.
Kegunaan Magnesium Hipoklorit
Mg(ClO)2 memiliki beberapa aplikasi praktis karena sifat pengoksidasi dan kemampuannya melepaskan gas klor. Berikut beberapa kegunaan umum Mg(ClO)2:
- Pengolahan Air: Biasa digunakan sebagai desinfektan di instalasi pengolahan air untuk membunuh bakteri dan virus berbahaya.
- Pemutih: Digunakan sebagai bahan pemutih untuk tekstil, kertas dan bahan lainnya.
- Kolam Renang: Digunakan sebagai bahan sanitasi di kolam renang untuk menjaga kandungan kimia air yang baik.
- Pengendalian Bau: Digunakan untuk mengendalikan bau tidak sedap di instalasi pengolahan limbah dan sistem saluran pembuangan.
- Zat pengoksidasi: digunakan sebagai zat pengoksidasi dalam produksi berbagai bahan kimia, seperti epoksida dan keton.
- Pertanian: Digunakan di bidang pertanian sebagai desinfektan dan pestisida untuk memerangi penyakit jamur dan bakteri.
- Sanitasi: Juga digunakan sebagai disinfektan pada permukaan dan peralatan di rumah sakit, pabrik pengolahan makanan, dan fasilitas lainnya.
Pertanyaan:
T: Apa rumus magnesium hipoklorit?
A: Rumus magnesium hipoklorit adalah Mg(ClO)2.
T: Berapa tingkat pH magnesium hipoklorit?
A: Tingkat pH Mg(ClO)2 bergantung pada konsentrasinya dan dapat bervariasi. Namun larutan Mg(ClO)2 umumnya memiliki pH antara 8 dan 10.
T: Apa rumus molekul magnesium hipoklorit?
A: Rumus molekul magnesium hipoklorit adalah Mg(ClO)2.
Q: Apa nama Mg(ClO)2?
A: Nama Mg(ClO)2 adalah magnesium hipoklorit.
Q: Apakah Mg(ClO)2 termasuk asam atau basa?
A: Mg(ClO)2 adalah garam basa dan dapat bertindak sebagai basa lemah dalam larutan air.
Q: Apakah Mg(ClO)2 termasuk garam?
A: Ya, Mg(ClO)2 adalah garam. Ini adalah senyawa kristal putih yang sangat larut dalam air dan mengandung logam (magnesium) dan non-logam (klorin).
