Kalsium nitrit (Ca(NO2)2) merupakan senyawa kimia yang biasa digunakan sebagai inhibitor korosi pada beton. Ini membantu mencegah korosi pada tulangan baja.
| Nama IUPAC | Kalsium dinirit |
| Formula molekul | Ca(NO2)2 |
| nomor CAS | 13780-06-8 |
| Sinonim | Kalsium nitrit dihidrat, asam nitrat, garam kalsium, asam nitrat, garam kalsium, dihidrat, dll. |
| Di ChI | InChI=1S/Ca.2HNO2/c;2 2-1-3/jam;2 (H,2,3) |
Sifat kalsium nitrit
Rumus kalsium nitrit
Rumus kimia kalsium nitrit adalah Ca(NO2)2. Rumus ini menunjukkan bahwa senyawa tersebut mengandung dua anion nitrit untuk setiap kation kalsium. Rumus tersebut penting dalam menentukan komposisi suatu senyawa dan dalam menentukan jumlah setiap unsur dalam suatu senyawa.
Massa Molar Kalsium Nitrit
Massa molar Ca(NO2)2, juga dikenal sebagai kalsium dinitrit, kira-kira 132,09 g/mol. Ini adalah senyawa ionik yang terdiri dari kation kalsium dan anion nitrit. Massa molar dihitung dengan menjumlahkan massa atom unsur penyusun senyawa, yang dalam hal ini adalah kalsium, nitrogen, dan oksigen.
Titik didih kalsium nitrit
Ca(NO2)2 memiliki titik didih yang tinggi sekitar 400°C (752°F). Titik didih yang tinggi ini disebabkan oleh kuatnya ikatan ion yang terdapat antara ion Ca2+ dan NO2- dalam senyawa tersebut. Ketika Ca(NO2)2 dipanaskan, ia mengalami dekomposisi termal, melepaskan nitrogen dioksida dan oksigen.
Titik leleh kalsium nitrit
Ca(NO2)2 memiliki titik leleh sekitar 132°C (270°F). Titik leleh ini relatif rendah dibandingkan senyawa ionik lainnya, seperti natrium klorida, yang memiliki titik leleh 801°C (1.474°F). Rendahnya titik leleh Ca(NO2)2 dapat disebabkan oleh relatif lemahnya ikatan ion antara ion Ca2+ dan NO2-.
Kepadatan kalsium nitrit g/mL
Massa jenis Ca(NO2)2 kira-kira 2,32 g/mL. Nilai tersebut menunjukkan bahwa Ca(NO2)2 merupakan senyawa yang relatif padat. Massa jenis dihitung dengan membagi massa senyawa dengan volumenya. Kepadatan Ca(NO2)2 yang tinggi dapat disebabkan oleh adanya kation kalsium yang relatif berat.
Berat Molekul Kalsium Nitrit
Berat molekul Ca(NO2)2 kira-kira 132,09 g/mol. Nilai ini dihitung dengan menjumlahkan berat atom unsur-unsur penyusun senyawa. Berat molekul penting dalam menentukan jumlah Ca(NO2)2 yang dibutuhkan untuk memperoleh jumlah mol senyawa tertentu.
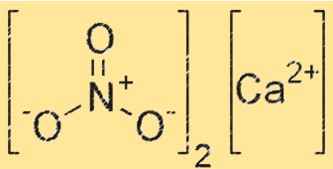
Struktur kalsium nitrit
Struktur Ca(NO2)2 terdiri dari Ca2+ dan NO2-. Ion Ca2+ terletak di tengah kisi kristal, sedangkan ion NO2- mengelilinginya. Kisi kristal disatukan oleh ikatan ionik yang kuat antara ion Ca2+ dan NO2-.
Kelarutan kalsium nitrit
Ca(NO2)2 larut dalam air dan alkohol. Kelarutan dalam air relatif tinggi, dengan kelarutan sekitar 61 g/100 ml air pada suhu kamar. Kelarutan dalam alkohol lebih rendah dibandingkan dalam air. Kelarutan Ca(NO2)2 penting dalam menentukan penggunaannya dalam berbagai aplikasi, seperti dalam produksi beton.
| Penampilan | Bubuk kristal putih sampai agak kuning atau padat |
| Berat jenis | 2.32 |
| Warna | Tidak berwarna sampai putih |
| Bau | Tidak berbau |
| Masa molar | 132,09 g/mol |
| Kepadatan | 2,32 gram/ml |
| Titik fusi | 132°C (270°F) |
| Titik didih | Terurai pada suhu sekitar 400°C (752°F) |
| Titik kilat | Tak dapat diterapkan |
| Kelarutan dalam air | Larut |
| Kelarutan | Larut dalam air dan alkohol |
| Tekanan uap | Tak dapat diterapkan |
| Kepadatan uap | Tak dapat diterapkan |
| pKa | Tak dapat diterapkan |
| pH | Netral |
Keamanan dan Bahaya Kalsium Nitrit
Ca(NO2)2 mungkin berbahaya jika tertelan, terhirup, atau terkena kulit atau mata. Hal ini dapat menyebabkan iritasi, luka bakar, dan masalah pernapasan. Senyawa tersebut juga merupakan zat pengoksidasi dan dapat bereaksi dengan bahan kimia lain, seperti asam dan logam, membentuk zat berbahaya. Ca(NO2)2 harus disimpan di tempat sejuk, kering, berventilasi baik, jauh dari bahan yang tidak kompatibel. Peralatan pelindung diri, seperti sarung tangan dan kacamata, harus dipakai saat menangani senyawa tersebut. Jika terpapar, pertolongan medis segera harus dicari dan pakaian yang terkontaminasi harus dilepas.
| Simbol bahaya | Xn |
| Deskripsi Keamanan | Hindari kontak dengan kulit dan mata; memakai alat pelindung diri (APD); Jika terpapar, segera dapatkan bantuan medis. |
| Nomor identifikasi PBB | PBB 1454 |
| kode HS | 2834.29.90 |
| Kelas bahaya | 5.1 |
| Kelompok pengepakan | AKU AKU AKU |
| Toksisitas | Berbahaya jika tertelan atau terhirup; dapat menyebabkan iritasi, luka bakar, dan masalah pernafasan |
Metode sintesis kalsium nitrit
Berbagai metode dapat mensintesis Ca(NO2)2, antara lain reaksi asam nitrat atau nitrogen oksida dengan kalsium karbonat , reaksi asam nitrat atau nitrogen oksida dengan karbon hidroksida. kalsium dan reaksi kalsium hidroksida atau amonium hidroksida dengan kalsium nitrat.
Metode yang umum adalah mereaksikan kalsium karbonat dengan asam nitrat untuk menghasilkan kalsium nitrat. Kemudian, reaksi kalsium nitrat dengan kalsium hidroksida menghasilkan pembentukan produk samping Ca(NO2)2 dan kalsium oksida.
Metode lain melibatkan reaksi nitrogen oksida dengan kalsium hidroksida untuk menghasilkan Ca(NO2)2 dan kalsium nitrat.
Dalam metode lain, seseorang dapat mereaksikan kalsium nitrat dengan kalsium hidroksida atau amonium hidroksida untuk menghasilkan Ca(NO2)2 sekaligus menghasilkan kalsium nitrat sebagai produk sampingannya.
Kegunaan Kalsium Nitrit
Ca(NO2)2 memiliki berbagai aplikasi di berbagai industri, antara lain:
- Industri Beton: Digunakan sebagai bahan tambahan beton untuk meningkatkan ketahanan dan kekuatan struktur beton. Ia bertindak sebagai penghambat korosi, melindungi baja tulangan dari korosi yang disebabkan oleh klorida dan ion agresif lainnya.
- Pertanian: Digunakan sebagai pupuk di bidang pertanian untuk menyediakan sumber nitrogen dan kalsium bagi tanaman. Juga digunakan sebagai bahan pembenah tanah untuk meningkatkan kualitas tanah dan meningkatkan pertumbuhan tanaman.
- Industri kimia: digunakan sebagai zat pereduksi dalam reaksi kimia, serta sebagai prekursor sintesis bahan kimia lain seperti kalsium nitrat dan kalsium amonium nitrat.
- Pengolahan Air Limbah: Digunakan sebagai bahan kimia pengolahan air limbah untuk menghilangkan kontaminan dan mengurangi konsentrasi zat berbahaya dalam air.
- Industri makanan: digunakan sebagai pengawet makanan untuk mencegah pertumbuhan bakteri dan mikroorganisme lain pada daging, ikan dan produk makanan lainnya.
Pertanyaan:
Q: Apa rumus kalsium nitrit?
A: Rumus kimia kalsium nitrit adalah Ca(NO2)2.
T: Berapa banyak kalsium nitrit yang digunakan dalam beton setiap tahunnya?
A: Jumlah Ca(NO2)2 yang digunakan dalam beton setiap tahun bervariasi tergantung pada aplikasi spesifik dan permintaan pasar. Namun, diperkirakan beberapa ribu ton Ca(NO2)2 digunakan di seluruh dunia sebagai bahan tambahan beton setiap tahunnya.
Q: Apakah kalsium nitrit larut dalam air?
A: Ya, Ca(NO2)2 larut dalam air. Ia memiliki kelarutan sekitar 167 g/L pada 20°C.
T: Apakah kalsium nitrit termasuk garam?
A: Ya, Ca(NO2)2 adalah garam. Senyawa ionik yang terdiri dari kation kalsium (Ca2+) dan anion nitrit (NO2-).
T: Bagaimana solusi berikut disiapkan? 1,25 l larutan Ca(NO2)2 sebanyak 0,775 m3
A: Untuk menyiapkan 1,25 L larutan Ca(NO2)2 0,775 M, Anda perlu melarutkan sekitar 187,5 g Ca(NO2)2 dalam air secukupnya hingga diperoleh volume akhir 1,25 L. Volume ini dapat dihitung dengan menggunakan rumus rumus: gram zat terlarut = Molaritas x volume (dalam liter) x massa molar zat terlarut.
Q: Apa rumus senyawa ionik kalsium nitrit?
A: Rumus senyawa ionik Ca(NO2)2 adalah Ca(NO2)2. Ini terdiri dari satu ion kalsium (Ca2+) dan dua ion nitrit (NO2-).
