Tetrabrometana adalah senyawa kimia dengan rumus CBr4. Ini adalah padatan kristal tidak berwarna dengan bau manis, digunakan sebagai pelarut dan tahan api. Ini beracun dan dapat membahayakan manusia dan lingkungan.
| Nama IUPAC | Tetrabrometana |
| Formula molekul | CBr4 |
| nomor CAS | 558-13-4 |
| Sinonim | Karbon tetrabromida, tetrabromoform, perbromometana, tetra-bromo-metana |
| Di ChI | InChI=1S/CBr4/c2-1(3,4)5 |
Sifat tetrabrometana
Massa molar CBr4
Tetrabrometana memiliki massa molar sekitar 331,63 g/mol. Ini adalah senyawa yang relatif berat dibandingkan dengan molekul organik lainnya. Massa molar tetrabromometana ditentukan dengan menjumlahkan massa atom semua atom dalam molekul. Dalam hal ini, ia terdiri dari satu atom karbon dan empat atom bromin.
Titik didih CBr4
Tetrabrometana memiliki titik didih 189°C (372°F). Ini adalah suhu di mana tekanan uap tetrabrometana cair sama dengan tekanan atmosfer. Pada suhu ini, cairan tetrabromometana akan mulai mendidih dan menguap menjadi gas.
Titik leleh CBr4
CBr4 memiliki titik leleh 90,5 °C (194,9 °F). Ini adalah suhu di mana CBr4 padat berubah menjadi cair. CBr4 memiliki titik leleh yang relatif tinggi untuk molekul organik, kemungkinan besar karena berat molekul dan gaya antarmolekulnya yang tinggi.
Kepadatan CBr4 g/ml
Massa jenis tetrabrometana adalah 3,42 g/mL pada suhu kamar. Artinya volume tertentu tetrabrometana memiliki berat 3,42 kali lebih banyak dari volume air yang sama. Kepadatan tinggi tetrabrometana disebabkan oleh berat molekulnya yang tinggi dan susunan atomnya yang rapat.
Berat molekul CBr4
Berat molekul tetrabrometana adalah 331,63 g/mol. Ini adalah berat gabungan semua atom dalam molekul. Berat molekul tetrabrometana penting untuk menghitung sifat fisiknya dan untuk memahami perilakunya dalam reaksi kimia.
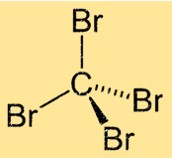
struktur CBr4
Tetrabromometana memiliki geometri molekul tetrahedral, dengan atom karbon di tengah dan empat atom bromin melekat padanya. Molekul ini memiliki struktur simetris dengan empat ikatan Br-C identik yang tersusun pada sudut yang sama di sekitar atom karbon pusat. Struktur ini memberi tetrabrometana sifat fisik dan kimia yang unik.
Rumus tetrabrometana
Rumus tetrabrometana adalah CBr4. Artinya ia terdiri dari satu atom karbon dan empat atom bromin. Rumus tetrabrometana penting untuk memahami struktur kimianya dan memprediksi reaktivitasnya dengan molekul lain.
| Penampilan | Padatan kristal tidak berwarna sampai kuning pucat |
| Berat jenis | 3,42 gram/ml |
| Warna | Tidak berwarna sampai kuning pucat |
| Bau | Lembut |
| Masa molar | 331,63 g/mol |
| Kepadatan | 3,42 gram/ml |
| Titik fusi | 90,5°C (194,9°F) |
| Titik didih | 189°C (372°F) |
| Titik kilat | Tidak mudah terbakar |
| Kelarutan dalam air | 0,0032 g/100 mL pada 20°C |
| Kelarutan | Tidak larut dalam air, larut dalam benzena, kloroform dan karbon disulfida |
| Tekanan uap | 0,006 mmHg pada 25°C |
| Kepadatan uap | 14.2 (melawan udara) |
| pKa | Tak dapat diterapkan |
| pH | Tak dapat diterapkan |
Keamanan dan bahaya tetrabrometana
Tetrabrometana dapat menimbulkan beberapa bahaya jika tidak ditangani dengan benar. Berbahaya jika tertelan, terhirup atau terkena kulit. Paparan tetrabrometana dapat menyebabkan iritasi, sakit kepala, pusing, dan mual. Paparan yang terlalu lama dapat menyebabkan kerusakan hati dan ginjal. Ini juga merupakan potensi bahaya lingkungan dan tidak boleh dilepaskan ke lingkungan. Tindakan pencegahan yang tepat, termasuk penggunaan pakaian dan peralatan pelindung, harus dilakukan saat menangani tetrabromometana. Jika terjadi paparan yang tidak disengaja, perhatian medis segera harus dicari. Tetrabromomethane harus disimpan dan ditangani di tempat yang berventilasi baik dan sesuai dengan protokol keselamatan yang sesuai.
| Simbol bahaya | T (beracun) |
| Deskripsi Keamanan | Jangan menelan, menghirup atau bersentuhan dengan kulit. Kenakan pakaian dan peralatan pelindung. Jika terjadi paparan yang tidak disengaja, konsultasikan dengan dokter. |
| Nomor identifikasi PBB | PBB 2515 |
| kode HS | 2903.90.9000 |
| Kelas bahaya | 6.1 |
| Kelompok pengepakan | II |
| Toksisitas | Beracun jika tertelan, terhirup atau terserap melalui kulit. Dapat menyebabkan iritasi, sakit kepala, pusing dan mual. Paparan yang terlalu lama dapat menyebabkan kerusakan hati dan ginjal. |
Metode sintesis tetrabromometana
Untuk mensintesis tetrabrometana, peneliti dapat mereaksikan brom metana , mereaksikan karbon tetrabromida dengan gas hidrogen, atau mereaksikan brom dengan natrium format.
Brominasi metana melibatkan reaksi metana dengan brom dengan adanya katalis, seperti besi atau aluminium bromida. Anda dapat memisahkan dan memurnikan campuran bromometana hasil proses untuk memperoleh Tetrabromometana.
Untuk mensintesis tetrabrometana, karbon tetrabromida dapat direaksikan dengan gas hidrogen dengan adanya katalis seperti nikel. Reaksi ini menghasilkan campuran bromometana, yang dapat dipisahkan dan dimurnikan oleh peneliti untuk mendapatkan tetrabromometana.
Metode lain untuk mensintesis tetrabrometana melibatkan reaksi brom dengan natrium format dengan adanya asam sulfat. Pemisahan dan pemurnian produk tetrabrometana dan natrium sulfat yang dihasilkan akan menghasilkan tetrabrometana.
Kegunaan Tetrabrometana
Tetrabrometana memiliki beberapa aplikasi di berbagai industri karena sifatnya yang unik. Berikut beberapa kegunaannya:
- Flame Retardant: Digunakan sebagai penghambat api pada plastik, tekstil, dan bahan lainnya. Ia bekerja dengan melepaskan brom saat terkena panas, yang menghambat proses pembakaran.
- Bahan Kimia Menengah: Digunakan sebagai zat antara kimia dalam produksi bahan kimia lainnya, seperti obat-obatan dan bahan kimia pertanian.
- Pelarut: Digunakan sebagai pelarut berbagai senyawa organik, khususnya dalam produksi pestisida.
- Agen uji: digunakan sebagai agen uji untuk mendeteksi kotoran pada bahan kimia lainnya.
- Agen pemurnian: digunakan sebagai agen pemurnian dalam produksi aluminium dan logam lainnya.
- Kedokteran hewan: Digunakan dalam kedokteran hewan sebagai obat cacing atau obat cacing untuk pengobatan infeksi parasit pada hewan.
Pertanyaan:
Q: Apakah CBR4 polar atau non polar?
A: Tetrabromomethane (cbr4) adalah molekul non-polar karena struktur tetrahedralnya yang simetris dan kurangnya ikatan polar.
Q: Manakah senyawa berikut yang bersifat polar: cbr4, xef2, scl4, brf3, ch3oh?
J: Di antara senyawa yang diberikan, hanya CH3OH (metanol) dan BRF3 (bromin trifluorida) yang merupakan molekul polar karena struktur molekulnya yang asimetris dan adanya ikatan polar.
Q: Apakah cbr4 larut dalam air?
A: Tetrabrometana tidak larut dalam air karena sifatnya yang non-polar, tidak sesuai dengan sifat polar air.
Q: Apa nama senyawa rumus cbr4? A: Senyawa rumus cbr4 disebut tetrabrometana atau karbon tetrabromida.
