Benzena atau C6H6 adalah cairan tidak berwarna, sangat mudah terbakar, dan berbau manis. Ini digunakan dalam produksi plastik, serat sintetis, karet, pestisida dan bahan kimia lainnya. Ini dikenal sebagai karsinogen dan dapat menyebabkan masalah kesehatan.
| Nama IUPAC | benzena |
| Formula molekul | C6H6 |
| nomor CAS | 71-43-2 |
| Sinonim | Benzol, Fena, Annulena, Sikloheksatriena, dll. |
| Di ChI | InChI=1S/C6H6/c1-2-4-6-5-3-1/h1-6H |
Sifat-sifat benzena
Massa molar Benzena
Benzena memiliki massa molar 78,11 g/mol. Ini adalah senyawa organik siklik yang terdiri dari enam atom karbon dan enam atom hidrogen. Massa molar benzena dihitung dengan menjumlahkan massa atom atom penyusunnya, yaitu 12,01 g/mol untuk karbon dan 1,01 g/mol untuk hidrogen. Benzena banyak digunakan dalam industri kimia sebagai bahan baku produksi banyak senyawa penting. Massa molar benzena penting dalam menentukan jumlah senyawa yang dibutuhkan untuk reaksi dan aplikasi lainnya.
rumus benzena
Benzena memiliki rumus kimia C6H6. Rumus ini mewakili jumlah dan jenis atom yang ada dalam molekul. Rumus benzena penting dalam menentukan sifat fisik dan kimianya, serta reaktivitasnya dalam reaksi kimia. Rumus benzena juga digunakan untuk memberi nama dan mengidentifikasi senyawa dalam berbagai konteks, seperti dalam literatur kimia dan dokumen peraturan.
Titik didih benzena
Benzena memiliki titik didih 80,1°C atau 176,2°F. Ini relatif rendah dibandingkan dengan senyawa organik lain dengan berat molekul serupa. Titik didih C6H6 disebabkan oleh gaya tarik menarik antarmolekulnya, terutama gaya Van der Waals. Ketika suhu meningkat, energi kinetik molekul juga meningkat, yang pada akhirnya menyebabkan pemecahan gaya antarmolekul dan transisi dari fase cair ke fase gas. Titik didih C6H6 yang rendah membuatnya berguna dalam aplikasi yang memerlukan penghilangan senyawa melalui penguapan.
Titik leleh benzena
C6H6 memiliki titik leleh 5,5°C atau 41,9°F. Ini relatif rendah dibandingkan dengan senyawa aromatik lain dengan berat molekul serupa. Titik leleh C6H6 disebabkan oleh struktur molekulnya, yang terdiri dari cincin datar atom karbon dengan ikatan rangkap bergantian. Susunan elektron dalam cincin memberikan stabilitas karakteristik pada C6H6 dan membuatnya tahan terhadap banyak reaksi kimia. Titik leleh C6H6 yang rendah membuatnya berguna dalam aplikasi yang memerlukan peleburan senyawa untuk diproses lebih lanjut.
Massa jenis benzena g/ml
Benzena memiliki kepadatan 0,879 g/mL pada suhu kamar (25°C atau 77°F). Massa jenis benzena adalah ukuran massa per satuan volume suatu senyawa. Kepadatan benzena yang rendah membuatnya berguna dalam aplikasi yang memerlukan pelarut dengan kepadatan rendah, seperti dalam pemisahan senyawa berdasarkan kepadatannya.
Berat molekul benzena
Benzena memiliki berat molekul 78,11 g/mol. Berat molekul benzena adalah jumlah berat atom atom-atom penyusunnya. Berat molekul benzena penting dalam menentukan stoikiometri reaksi dan menentukan konsentrasi benzena dalam larutan.
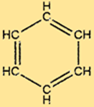
Struktur benzena
C6H6 memiliki struktur unik yang terdiri dari cincin atom karbon heksagonal, masing-masing terikat pada dua atom karbon lain dan satu atom hidrogen. Ikatan rangkap bergantian pada cincin memberikan stabilitas karakteristik pada C6H6 dan membuatnya tahan terhadap banyak reaksi kimia. Struktur C6H6 juga menjadikannya bahan mentah yang berguna untuk produksi banyak senyawa penting.
| Penampilan | Cairan tidak berwarna |
| Berat jenis | 0,879 gram/ml |
| Warna | Tanpa warna |
| Bau | Lembut |
| Masa molar | 78,11 g/mol |
| Kepadatan | 0,879 gram/ml |
| Titik fusi | 5,5°C (41,9°F) |
| Titik didih | 80,1°C (176,2°F) |
| Titik kilat | -11°C (12,2°F) |
| Kelarutan dalam air | 1,79g/L |
| Kelarutan | Tidak larut dalam air, larut dalam pelarut organik |
| Tekanan uap | 12,1 kPa pada 20°C |
| Kepadatan uap | 2.8 (udara=1) |
| pKa | 43.2 |
| pH | Netral |
Keamanan dan Bahaya Benzena
C6H6 adalah senyawa yang sangat mudah terbakar dan beracun yang menimbulkan risiko signifikan terhadap kesehatan manusia dan lingkungan. Ini dikenal sebagai karsinogen dan dapat menyebabkan leukemia, anemia aplastik dan kelainan darah lainnya pada manusia. Paparan C6H6 dapat terjadi melalui penghirupan, kontak dengan kulit, atau konsumsi dan dapat mengakibatkan efek kesehatan akut dan kronis. Penting untuk menangani C6H6 dengan tindakan pencegahan keselamatan yang tepat, termasuk ventilasi yang memadai, pakaian pelindung, dan pelindung pernapasan. C6H6 juga harus disimpan dan dibuang sesuai dengan peraturan setempat untuk meminimalkan kontaminasi lingkungan dan risiko kesehatan masyarakat.
| Simbol bahaya | Tengkorak dan Tulang Bersilang, Api |
| Deskripsi Keamanan | Amat mudah terbakar, Beracun, Karsinogenik, Berbahaya jika tertelan, Mengiritasi |
| Sebuah pengidentifikasi | UN 1114 (Benzene), UN 1992 (Cairan beracun dan mudah terbakar) |
| kode HS | 2902.20.00 |
| Kelas bahaya | 3 (Cairan mudah terbakar), 6.1 (Zat beracun), 8 (Zat korosif) |
| Kelompok pengepakan | II (Benzena), III (Cairan beracun dan mudah terbakar) |
| Toksisitas | Toksisitas akut: Sangat beracun (LD50: 2.5 g/kg per oral, 0.44 mg/L jika terhirup), Toksisitas kronis: Karsinogenik, Mutagenik, Toksisitas reproduksi |
Metode sintesis benzena
Ada beberapa metode untuk mensintesis benzena, bahan kimia industri penting yang digunakan dalam produksi plastik, karet, dan obat-obatan.
Salah satu metode yang umum adalah reformasi katalitik nafta minyak bumi, yang melibatkan pemanasan nafta hingga suhu tinggi dengan adanya katalis, seperti platina atau renium, untuk menghasilkan campuran hidrokarbon aromatik, termasuk benzena.
Metode lainnya adalah hidrodealkilasi toluena, yang melibatkan reaksi toluena dengan hidrogen dengan adanya katalis, seperti kromium oksida atau molibdenum oksida, untuk menghilangkan gugus metil dan membentuk benzena.
Pirolisis hidrokarbon, seperti batu bara atau minyak bumi, pada suhu tinggi tanpa adanya oksigen akan mensintesis benzena. Proses ini menghasilkan terbentuknya campuran hidrokarbon aromatik, termasuk benzena.
Metode lain untuk mensintesis benzena meliputi reaksi asetilena dengan dirinya sendiri dengan adanya katalis, seperti tembaga, untuk membentuk benzena, serta reaksi fenol dengan formaldehida dengan adanya katalis asam, seperti asam sulfat, untuk membentuk benzena. membentuk benzena. menghasilkan benzena.
Masing-masing metode ini mempunyai kelebihan dan kekurangannya masing-masing, tergantung pada faktor-faktor seperti biaya, efektivitas dan dampak terhadap lingkungan. Pilihan metode sintesis benzena akan bergantung pada aplikasi spesifik dan persyaratan proses produksi.
Kegunaan benzena
Benzena adalah bahan kimia industri serbaguna dan penting dengan beragam aplikasi di berbagai industri. Beberapa kegunaan utama benzena adalah:
- Produksi plastik: digunakan dalam produksi berbagai jenis plastik, termasuk polistiren, poliuretan, dan nilon.
- Produksi Karet: Produsen karet sintetis menggunakannya dalam produksi mereka. Produsen kemudian menggunakan karet sintetis ini untuk membuat ban, pipa, ikat pinggang, dan produk karet lainnya.
- Produksi farmasi: Digunakan sebagai bahan baku produksi berbagai produk farmasi, termasuk antibiotik, antihistamin, dan analgesik.
- Pelarut: Digunakan sebagai pelarut untuk berbagai senyawa organik, termasuk lemak, minyak, resin, dan lilin.
- Bahan Bakar: Digunakan sebagai aditif bahan bakar beroktan tinggi, meningkatkan kinerja mesin bensin.
- Ekstraksi Minyak: Digunakan dalam ekstraksi minyak, seperti minyak nabati dan minyak esensial, dari tumbuhan.
- Perekat: Digunakan dalam produksi perekat, seperti semen karet dan semen kontak.
- Pewarna: Digunakan dalam produksi berbagai jenis pewarna, termasuk pewarna sintetis yang digunakan dalam industri tekstil.
Pertanyaan:
T: Apakah benzena bersifat polar?
J: Tidak, benzena adalah molekul non-polar karena memiliki struktur simetris dan polaritas masing-masing ikatannya hilang.
T: Untuk apa benzena digunakan?
J: Benzena digunakan dalam produksi berbagai bahan, termasuk plastik, karet, obat-obatan, pelarut, bahan tambahan bahan bakar, perekat dan pewarna.
Q: Senyawa apa yang dapat menghantarkan listrik jika dilarutkan dalam air? CH4, CuSO4, C6H6 atau C6H12O6?
A: CuSO4 menghantarkan listrik ketika dilarutkan dalam air karena terdisosiasi menjadi ion-ion sehingga memungkinkan arus listrik mengalir.
T: Apakah C6H6 polar atau non-polar?
J: C6H6, juga dikenal sebagai benzena, adalah molekul nonpolar karena memiliki struktur simetris dan polaritas ikatan individunya hilang.
Q: Apakah C6H6 larut dalam air?
J: Tidak, C6H6 tidak larut dalam air karena merupakan molekul non-polar dan tidak berinteraksi dengan baik dengan pelarut polar seperti air.
