Natrium peroksida (Na2O2) adalah zat pengoksidasi yang kuat. Ia bereaksi hebat dengan air untuk melepaskan oksigen dan dapat menyulut bahan yang mudah terbakar jika bersentuhan. Ini digunakan dalam berbagai reaksi kimia dan sebagai desinfektan.
| Nama IUPAC | natrium oksida |
| Formula molekul | Na2O2 |
| nomor CAS | 1313-60-6 |
| Sinonim | Natrium peroksida, natrium superoksida, dinatrium dioksida, natrium binoksida, natrium dioksida, NaO2, UN 1507 |
| Di ChI | InChI=1S/2Na.O2/c;;1-2/q2*+1;-2 |
Sifat natrium peroksida
Rumus Natrium Peroksida
Rumus kimia natrium peroksida adalah Na2O2. Ini adalah senyawa ionik yang terdiri dari dua kation natrium (Na+) dan anion peroksida (O22-). Rumus natrium peroksida digunakan untuk mewakili komposisi kimia suatu senyawa dan penting dalam reaksi kimia yang melibatkan zat tersebut.
Massa molar natrium peroksida
Natrium peroksida, rumus kimia Na2O2, memiliki massa molar 77,98 g/mol. Ini adalah senyawa ionik yang terdiri dari dua kation natrium (Na+) dan anion peroksida (O22-). Massa molar natrium peroksida sangat penting untuk menghitung jumlah senyawa yang dibutuhkan untuk berbagai reaksi kimia.
Titik didih natrium peroksida
Natrium peroksida memiliki titik didih yang sangat tinggi yaitu 657°C (1215°F), membuatnya sangat stabil pada suhu tinggi. Senyawa tersebut terurai sebelum mencapai titik didihnya, melepaskan gas oksigen dan meninggalkan natrium oksida. Titik didih natrium peroksida yang tinggi membuatnya berguna dalam reaksi suhu tinggi dan proses industri yang memerlukan stabilitas termal yang tinggi.
Titik leleh natrium peroksida
Natrium peroksida memiliki titik leleh 675°C (1247°F), yang relatif tinggi dibandingkan zat umum lainnya. Ia meleleh membentuk cairan putih kekuningan dan terurai di atas titik lelehnya untuk melepaskan gas oksigen dan membentuk natrium oksida. Titik leleh natrium peroksida yang tinggi membuatnya berguna dalam reaksi kimia pada suhu tinggi.
Massa jenis natrium peroksida g/ml
Massa jenis natrium peroksida adalah 2,805 g/mL. Ini adalah bubuk putih sampai kekuningan dengan kepadatan lebih besar dari air. Kepadatan natrium peroksida yang tinggi membuatnya berguna dalam berbagai proses industri seperti pemutihan, desinfeksi dan produksi bahan kimia lainnya.
Berat molekul natrium peroksida
Natrium peroksida memiliki berat molekul 77,98 g/mol. Ini adalah senyawa ionik dengan dua kation natrium (Na+) dan satu anion peroksida (O22-). Berat molekul natrium peroksida penting dalam reaksi kimia yang melibatkan senyawa karena membantu menentukan jumlah reaktan dan produk.
Struktur natrium peroksida
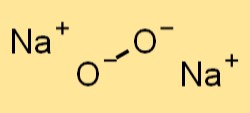
Natrium peroksida memiliki struktur kristal yang mirip dengan natrium klorida (NaCl). Ini membentuk kisi kubik berpusat muka, di mana ion natrium menempati sudut kubus dan anion peroksida terletak di tengah setiap muka. Anion peroksida dalam natrium peroksida diikat melalui ikatan kovalen, sedangkan ion natrium diikat melalui ikatan ionik.
| Penampilan: | Bubuk berwarna putih hingga kekuningan |
| Berat jenis: | 2,805 gram/cm3 |
| Warna: | Putih hingga kekuningan |
| Bau: | Tidak berbau |
| Masa molar: | 77,98 g/mol |
| Kepadatan: | 2,805 gram/cm3 |
| Titik fusi: | 675°C (1247°F) |
| Titik didih: | 657°C (1215°F) |
| Titik nyala: | Tak dapat diterapkan |
| Kelarutan dalam air: | Bereaksi hebat dengan air |
| Kelarutan: | Larut dalam alkohol, eter |
| Tekanan uap: | Tak dapat diterapkan |
| Kepadatan uap: | Tak dapat diterapkan |
| pKa: | Tak dapat diterapkan |
| nomor telepon: | Tak dapat diterapkan |
Keamanan dan Bahaya Natrium Peroksida
| Simbol bahaya: | Oksidasi, Korosif |
| Deskripsi Keamanan: | Jangan menghirup debu/asap/gas/kabut/uap. Hindari kontak dengan kulit/mata. Tangani dan simpan di bawah gas inert. Jika kena mata, segera bilas dengan banyak air dan bilas ke dokter. Jika terjadi kebakaran, gunakan media pemadam yang sesuai. |
| Nomor identifikasi PBB: | UN1503 |
| Kode HS: | 2829.11.00 |
| Kelas bahaya: | 5.1 |
| Kelompok pengepakan: | II |
| Toksisitas: | Korosif terhadap mata dan kulit, berbahaya jika tertelan atau terhirup. |
Metode sintesis natrium peroksida
Sintesis natrium peroksida (Na2O2) dapat dilakukan melalui beberapa metode, seperti kombinasi langsung, reaksi dengan oksigen, dan elektrolisis.
Salah satu metode sintesis Na2O2 adalah metode kombinasi langsung. Ini melibatkan pemanasan logam natrium dengan oksigen berlebih di dalam tungku. Reaksinya eksotermik dan penting untuk mengatur suhu untuk menghindari panas berlebih dan kemungkinan ledakan.
Metode lain melibatkan reaksi natrium hidroksida dengan hidrogen peroksida untuk menghasilkan Na2O2 dan air. Metode ini lebih aman dan terkontrol dibandingkan metode kombinasi langsung namun memerlukan suhu lebih tinggi dan waktu reaksi lebih lama.
Metode lain untuk mensintesis Na2O2 adalah melalui elektrolisis. Ini melibatkan elektrolisis larutan natrium hidroksida menggunakan anoda dan katoda yang sesuai. Pada proses elektrolisis, katoda menghasilkan Na2O2, sedangkan anoda menghasilkan gas oksigen.
Kegunaan natrium peroksida
Natrium peroksida banyak digunakan dalam industri dan laboratorium karena sifat pengoksidasi dan kemampuannya melepaskan oksigen.
Berikut beberapa kegunaan umum natrium peroksida:
- Pemutih: Digunakan sebagai bahan pemutih untuk pulp kertas, tekstil dan bahan lainnya.
- Agen Penghilang Bau: Digunakan sebagai agen penghilang bau di fasilitas pembuangan limbah dan pengolahan air limbah.
- Agen pengoksidasi: digunakan untuk mengoksidasi berbagai senyawa organik dan anorganik.
- Polimerisasi: Memulai polimerisasi monomer tertentu. Digunakan dalam produksi busa poliuretan dan polimer lainnya.
- Aplikasi farmasi: Digunakan sebagai reagen dalam sintesis senyawa farmasi.
- Reagen Laboratorium: Digunakan sebagai reagen laboratorium untuk berbagai keperluan analitis dan sintetik.
- Aplikasi Sel Bahan Bakar: Digunakan sebagai oksidator dalam sel bahan bakar untuk menghasilkan tenaga listrik.
Pertanyaan:
T: Apa reaksi kimia antara hidrogen peroksida dan natrium bisulfit?
J: Reaksi kimia antara hidrogen peroksida dan natrium bisulfit menghasilkan air dan natrium sulfat. Persamaan reaksi setimbangnya adalah: 2 NaHSO3 + H2O2 → Na2SO4 + 2 H2O.
T: Dimana bisa membeli bubuk natrium peroksida?
A: Bubuk natrium peroksida dapat dibeli dari berbagai pemasok dan distributor bahan kimia. Penting untuk memastikan bahwa pemasok memiliki reputasi baik dan mengikuti protokol keselamatan yang tepat dalam menangani dan mengirimkan bahan kimia berbahaya.
T: Dapatkah natrium oksida dibuat menjadi borohidrida dan hidrogen peroksida?
J: Natrium oksida tidak dapat dibuat langsung dari borohidrida dan hidrogen peroksida. Natrium oksida dapat disintesis melalui reaksi logam natrium dengan oksigen atau dengan memanaskan natrium hidroksida. Borohidrida dan hidrogen peroksida tidak umum digunakan dalam sintesis natrium oksida.
Q: Apa rumus natrium peroksida?
A: Rumus natrium peroksida adalah Na2O2.
Q: Berapakah bilangan oksidasi Na2O2?
A: Bilangan oksidasi natrium dalam Na2O2 adalah +1 dan bilangan oksidasi oksigen adalah -1.
Q: Berapakah bilangan oksidasi oksigen pada senyawa Na2O2?
A: Bilangan oksidasi oksigen dalam senyawa Na2O2 adalah -1.
