Magnesium nitrat adalah senyawa kristal putih dengan rumus kimia Mg(NO3)2. Ini digunakan dalam produksi pupuk, bahan peledak dan produk kembang api karena reaktivitasnya yang tinggi dan sifat pengoksidasi.
| Nama IUPAC | magnesium dinitrat |
| Formula molekul | mg(NO3)2 |
| nomor CAS | 10377-60-3 |
| Sinonim | Asam nitrat, garam magnesium; PBB 1474; Magnesium nitrat (II); Garam magnesium dari asam nitrat (2+) |
| Di ChI | InChI=1S/Mg.2NO3/c;22-1(3)4/q+2;2-1 |
Formula Magnesium Nitrat
Rumus kimia magnesium nitrat adalah Mg(NO3)2 yang menunjukkan bahwa senyawa tersebut mengandung satu kation magnesium (Mg²⁺) dan dua anion nitrat (NO₃⁻). Rumus ini digunakan untuk mewakili stoikiometri senyawa dalam persamaan kimia dan juga digunakan untuk menentukan berat molekul dan sifat magnesium nitrat lainnya.
Massa molar magnesium nitrat
Massa molar magnesium nitrat, yang dinyatakan dengan rumus kimia Mg(NO3)2, kira-kira 148,31 g/mol. Nilai ini dapat dihitung dengan menambahkan massa atom magnesium (24,31 g/mol), dua atom nitrogen (masing-masing 28,02 g/mol) dan enam atom oksigen (masing-masing 16,00 g/mol) yang ada dalam senyawa. Mengetahui massa molar sangat penting dalam menentukan jumlah magnesium nitrat yang dibutuhkan untuk reaksi kimia atau pembuatan larutan.
Titik didih magnesium nitrat
Mg(NO3)2 memiliki titik didih yang relatif tinggi sekitar 330°C (626°F) pada tekanan atmosfer. Nilai ini mungkin sedikit berbeda tergantung pada kemurnian dan konsentrasi senyawa. Titik didih Mg(NO3)2 penting dalam proses industri yang melibatkan produksi pupuk, bahan peledak dan kembang api, serta dalam percobaan laboratorium.
Titik lebur magnesium nitrat
Titik leleh Mg(NO3)2, yang merupakan suhu di mana senyawa padat berubah menjadi cair, kira-kira 89°C (192°F) untuk bentuk anhidrat dan 95°C (203°F) untuk bentuk bentuk anhidrat. bentuk heksahidrat. Bentuk heksahidrat Mg(NO3)2 lebih umum digunakan karena stabilitas dan kemudahan penanganannya. Titik lebur merupakan sifat fisik penting yang digunakan untuk menentukan kemurnian Mg(NO3)2 serta dalam berbagai proses industri.
Massa jenis magnesium nitrat g/ml
Massa jenis Mg(NO3)2 bervariasi tergantung pada bentuk senyawanya. Bentuk anhidrat memiliki kepadatan sekitar 2,3 g/cm³, sedangkan bentuk heksahidrat memiliki kepadatan sekitar 1,46 g/cm³. Kepadatan Mg(NO3)2 merupakan faktor penting dalam menentukan volume senyawa yang dibutuhkan dalam reaksi kimia, serta untuk penyimpanan dan pengangkutannya.
Berat Molekuler Magnesium Nitrat
Berat molekul Mg(NO3)2, yang merupakan jumlah berat atom seluruh unsur dalam senyawa, adalah sekitar 148,31 g/mol. Nilai ini penting dalam berbagai perhitungan kimia, terutama untuk menentukan jumlah Mg(NO3)2 yang diperlukan dalam reaksi atau dalam pembuatan larutan.
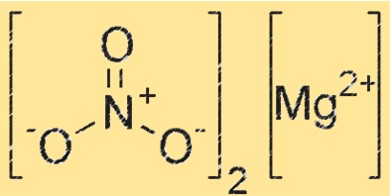
Struktur magnesium nitrat
Mg(NO3)2 memiliki struktur kristal yang termasuk dalam sistem kristal ortorombik. Senyawa tersebut terdiri dari kation magnesium (Mg²⁺) dan anion nitrat (NO₃⁻), dengan masing-masing kation magnesium dikelilingi oleh enam anion nitrat dalam susunan oktahedral. Struktur kristal Mg(NO3)2 memainkan peran penting dalam reaktivitas dan sifat-sifatnya.
| Penampilan | Padatan kristal putih |
| Berat jenis | 2,3 (anhidrat), 1,46 (heksahidrat) |
| Warna | Putih |
| Bau | Tidak berbau |
| Masa molar | 148,31 g/mol |
| Kepadatan | 2,3 g/cm³ (anhidrat), 1,46 g/cm³ (heksahidrat) |
| Titik fusi | 89°C (anhidrat), 95°C (heksahidrat) |
| Titik didih | 330°C |
| Titik kilat | Tak dapat diterapkan |
| Kelarutan dalam air | 234 g/L (anhidrat), 156 g/L (heksahidrat) pada 20°C |
| Kelarutan | Larut dalam air, etanol, metanol |
| Tekanan uap | 0,000009 mmHg pada 20°C |
| Kepadatan uap | Tak dapat diterapkan |
| pKa | 1.8 |
| pH | 4.5-6.0 (larutan 5%) |
Keamanan dan bahaya magnesium nitrat
Mg(NO3)2 dapat menimbulkan berbagai risiko keselamatan jika tidak ditangani dengan baik. Ini dapat menyebabkan iritasi dan luka bakar pada kulit, mata dan saluran pernapasan jika bersentuhan atau terhirup. Senyawa ini juga merupakan oksidator kuat dan dapat bereaksi hebat dengan bahan organik, termasuk zat yang mudah terbakar dan mudah terbakar. Menghirup debu Mg(NO3)2 dapat menyebabkan iritasi pernafasan bahkan kerusakan paru-paru. Simpan dan tangani Mg(NO3)2 di tempat sejuk, kering, berventilasi baik, jauh dari sumber api. Saat menangani senyawa ini, gunakan alat pelindung diri yang sesuai seperti sarung tangan dan kacamata pengaman.
| Simbol bahaya | Agen pengoksidasi |
| Deskripsi Keamanan | Hindari kontak dengan bahan yang mudah terbakar. Kenakan alat pelindung diri. Jauhkan dari sumber api. |
| Sebuah pengidentifikasi | PBB 1474 |
| kode HS | 283429 |
| Kelas bahaya | 5.1 (Agen pengoksidasi) |
| Kelompok pengepakan | II |
| Toksisitas | LD50 (oral, tikus): 3,500 mg/kg; LD50 (kulit, kelinci): > 2000 mg/kg. Magnesium nitrat tidak dianggap karsinogenik, mutagenik, atau teratogenik. |
Metode sintesis magnesium nitrat
Magnesium nitrat (Mg(NO3)2) dapat disintesis melalui beberapa metode, antara lain reaksi magnesium oksida atau magnesium hidroksida dengan asam nitrat.
Salah satu caranya adalah dengan menambahkan magnesium oksida ke dalam larutan asam nitrat dalam labu, lalu memanaskan campuran tersebut secara perlahan hingga larut. Untuk memperoleh kristal Mg(NO3)2, saring larutan untuk menghilangkan pengotor dan evaporasi pelarutnya.
Metode sintesis lain melibatkan mereaksikan logam magnesium dengan asam nitrat . Tambahkan strip magnesium ke dalam asam dan biarkan reaksi berlanjut hingga semua logam larut. Kemudian menguapkan larutan yang diperoleh sehingga diperoleh kristal Mg(NO3)2.
Larutkan magnesium karbonat dalam asam nitrat untuk membentuk Mg(NO3)2 dan karbon dioksida. Saring larutan yang dihasilkan dan evaporasi hingga diperoleh kristal Mg(NO3)2.
Cara lain adalah dengan mereaksikan magnesium hidroksida dengan asam nitrat menghasilkan Mg(NO3)2 dan air. Larutan yang diperoleh kemudian dimurnikan dengan cara filtrasi dan evaporasi hingga diperoleh kristal Mg(NO3)2.
Kegunaan Magnesium Nitrat
Magnesium nitrat memiliki banyak kegunaan di berbagai industri dan aplikasi. Beberapa kegunaan utama Mg(NO3)2 adalah:
- Pertanian: Digunakan sebagai pupuk, terutama pada tanaman yang membutuhkan magnesium tingkat tinggi, seperti tomat, paprika, dan buah jeruk. Ini membantu meningkatkan pertumbuhan tanaman dan meningkatkan kualitas dan hasil tanaman.
- Produk Kembang Api: Digunakan sebagai oksidator dalam kembang api dan aplikasi kembang api lainnya karena dapat menghasilkan nyala api yang terang dan intens serta membantu mengontrol laju pembakaran.
- Produksi Kaca: Digunakan sebagai fluks dalam produksi kaca untuk menurunkan titik leleh kaca dan meningkatkan sifat alirannya.
- Sintesis kimia: Digunakan sebagai reagen dalam berbagai reaksi sintesis kimia, seperti produksi senyawa magnesium lainnya, katalis, dan obat-obatan.
- Pengawetan: Digunakan sebagai pengawet makanan untuk menghambat pertumbuhan bakteri dan mikroorganisme lainnya.
- Aplikasi industri: Digunakan dalam produksi magnesium oksida dan magnesium hidroksida, yang digunakan sebagai penghambat api, dalam pengolahan air limbah dan sebagai zat penetral dalam tanah masam.
- Penelitian Laboratorium: Digunakan dalam berbagai eksperimen dan penelitian laboratorium, seperti menyiapkan larutan standar dan menguji prosedur analitis.
Pertanyaan:
Q: Apakah Mg(NO3)2 dapat larut?
A: Ya, magnesium nitrat sangat larut dalam air.
Q: Apa rumus magnesium nitrat?
A: Rumus magnesium nitrat adalah Mg(NO3)2.
Q: Berapa massa molar Mg(NO3)2?
A: Massa molar Mg(NO3)2 adalah 148,31 g/mol.
Q: Berapa rumus berat Mg(NO3)2?
A: Berat rumus Mg(NO3)2 adalah 148,31 g/mol.
Q: Apa nama sistematik dari Mg(NO3)2?
A: Nama sistematik untuk Mg(NO3)2 adalah magnesium dinitrat.
Q: Berapa konsentrasi ion nitrat dalam larutan Mg(NO3)2 0,125 M?
A: Konsentrasi ion nitrat dalam larutan Mg(NO3)2 0,125 M adalah 0,25 M, karena terdapat dua ion nitrat untuk setiap ion magnesium.
Q: Berapa rumus massa Mg(NO3)2?
A: Massa rumus Mg(NO3)2 adalah 148,31 g/mol.
