Kalsium karbonat adalah senyawa kimia dengan rumus CaCO3. Hal ini umumnya ditemukan di bebatuan dan kerang dan digunakan dalam produksi semen, cat dan suplemen makanan.
| Nama IUPAC | Kalsium karbonat |
| Formula molekul | CaCO3 |
| nomor CAS | 471-34-1 |
| Sinonim | Batu kapur, kapur, kalsit, aragonit, marmer, kalsium karbonat yang diendapkan, garam kalsium dari asam karbonat (1:1) |
| Di ChI | InChI=1S/CH2O3.Ca/c2-1(3)4;/h(H2,2,3,4);/q;+2/p-2 |
Massa molar CaCO3
Massa molar kalsium karbonat adalah 100,09 g/mol. Artinya satu mol kalsium karbonat mengandung 100,09 gram senyawa tersebut. Massa molar penting dalam perhitungan stoikiometri karena memungkinkan konversi dari mol ke gram atau sebaliknya.
Formula Kalsium Karbonat
Rumus kimia kalsium karbonat adalah CaCO₃. Artinya setiap molekul kalsium karbonat mengandung satu atom kalsium, satu atom karbon, dan tiga atom oksigen. Rumusnya penting untuk menentukan jumlah kalsium karbonat yang dibutuhkan untuk aplikasi spesifik dan untuk memahami sifat kimianya.
Titik didih kalsium karbonat
Kalsium karbonat tidak memiliki titik didih karena terurai sebelum mencapai titik didihnya. Pada tekanan atmosfer, kalsium karbonat terurai menjadi kalsium oksida dan karbon dioksida pada suhu di atas 825°C. Oleh karena itu, kalsium karbonat umumnya digunakan dalam aplikasi suhu tinggi, seperti produksi semen.
Titik Leleh Kalsium Karbonat
Titik leleh kalsium karbonat adalah 1339°C. Pada suhu ini, kalsium karbonat mengalami dekomposisi termal untuk membentuk kalsium oksida dan karbon dioksida. Titik leleh penting untuk memahami perilaku kalsium karbonat pada suhu tinggi.
Kepadatan Kalsium Karbonat g/ml
Massa jenis kalsium karbonat adalah 2,71 g/cm³. Artinya kalsium karbonat lebih padat dari air dan akan tenggelam jika dimasukkan ke dalam air. Kepadatan penting untuk memahami sifat fisik kalsium karbonat dan untuk menentukan kegunaannya dalam berbagai aplikasi.
Berat Molekul Kalsium Karbonat
Berat molekul kalsium karbonat adalah 100,09 g/mol. Artinya senyawa tersebut terdiri dari satu atom kalsium, satu atom karbon, dan tiga atom oksigen. Berat molekul penting untuk menentukan jumlah kalsium karbonat yang dibutuhkan untuk aplikasi tertentu dan untuk memahami sifat kimianya.
Struktur kalsium karbonat
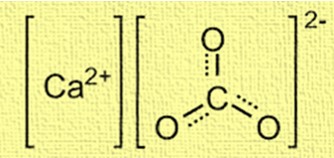
Struktur kalsium karbonat berbentuk kristal dan terdiri dari ion kalsium (Ca²⁺) dan ion karbonat (CO₃²⁻). Ion kalsium terletak di tengah struktur dan dikelilingi oleh enam ion karbonat. Ion karbonat tersusun dalam bentuk trigonal planar, dengan setiap atom oksigen terhubung ke atom karbon melalui ikatan rangkap. Struktur ini penting untuk memahami perilaku kalsium karbonat dalam berbagai aplikasi, seperti pembentukan cangkang dan terumbu karang.
| Penampilan | Bubuk putih atau kristal tidak berwarna |
| Berat jenis | 2.71 |
| Warna | Putih |
| Bau | Tidak berbau |
| Masa molar | 100,09 g/mol |
| Kepadatan | 2,71 gram/cm³ |
| Titik fusi | 1339°C |
| Titik didih | Rusak sebelum direbus |
| Titik kilat | Tak dapat diterapkan |
| Kelarutan dalam air | 0,0013 g/100 ml (25°C) |
| Kelarutan | Tidak larut dalam air dan sebagian besar pelarut organik |
| Tekanan uap | Dapat diabaikan |
| Kepadatan uap | Tak dapat diterapkan |
| pKa | 09.00 (pertama); 11,8 (detik) |
| pH | 9.3 – 9.7 (larutan berair 0,1 M) |
Keamanan dan Bahaya Kalsium Karbonat
Kalsium karbonat umumnya dianggap aman bagi manusia dan lingkungan bila digunakan sesuai petunjuk. Namun, menghirup debu kalsium karbonat dapat menyebabkan iritasi pada saluran pernapasan, mata, dan kulit. Paparan debu kalsium karbonat konsentrasi tinggi dalam jangka panjang dapat menyebabkan kerusakan paru-paru. Kalsium karbonat juga dapat bereaksi dengan asam kuat menghasilkan karbon dioksida, yang dapat menyebabkan bahaya kebakaran atau ledakan pada situasi tertentu. Penting untuk mengikuti prosedur keselamatan yang tepat saat menangani kalsium karbonat, seperti memakai peralatan pelindung dan memastikan ventilasi yang memadai.
| Simbol bahaya | Tak dapat diterapkan |
| Deskripsi Keamanan | Hindari menghirup debu. Kenakan peralatan pelindung. |
| Nomor identifikasi PBB | Tidak diatur |
| kode HS | 2836.50.00 |
| Kelas bahaya | Tidak diatur |
| Kelompok pengepakan | Tak dapat diterapkan |
| Toksisitas | Toksisitas rendah bagi manusia dan lingkungan |
Metode sintesis kalsium karbonat
Berbagai metode dapat mensintesis kalsium karbonat (CaCo3), antara lain metode presipitasi, karbonasi, dan sol-gel.
Metode pengendapan melibatkan pencampuran kalsium hidroksida dengan garam karbonat larut, seperti natrium karbonat , dalam kondisi terkendali untuk membentuk endapan CaCo3. Untuk mendapatkan produk akhir, endapan harus disaring dan dikeringkan.
Metode karbonasi melibatkan reaksi kalsium oksida dengan karbon dioksida di bawah tekanan dan suhu tinggi untuk menghasilkan CaCo3. Reaksi harus dilakukan dalam sistem tertutup untuk mencegah keluarnya karbon dioksida. Selanjutnya, kalsium oksida atau karbon dioksida yang tidak bereaksi harus dipisahkan dari CaCo3 yang dihasilkan dan dimurnikan.
Metode sol-gel melibatkan hidrolisis dan kondensasi prekursor yang mengandung kalsium, seperti kalsium alkoksida atau kalsium nitrat, dengan adanya pelarut dan katalis. Untuk menghasilkan CaCo3, gel yang diperoleh harus dikeringkan dan dikalsinasi.
Metode sintesis CaCo3 melibatkan penggunaan biomineralisasi, dimana organisme hidup seperti karang atau cangkang tiram menghasilkan kristal CaCo3. Operator mengumpulkan kristal ini dan memprosesnya untuk mendapatkan produk akhir.
Setiap metode mempunyai kelebihan dan kekurangannya masing-masing, dan pilihan metode bergantung pada faktor-faktor seperti biaya, kemurnian, dan ukuran partikel produk akhir yang diinginkan.
Kegunaan Kalsium Karbonat
Kalsium karbonat memiliki banyak kegunaan di berbagai industri, karena sifat-sifatnya seperti toksisitas rendah, kemurnian tinggi, dan ketersediaan biaya rendah. Beberapa kegunaan umum kalsium karbonat adalah:
- Konstruksi: Digunakan sebagai bahan bangunan berupa batu kapur, marmer dan kapur. Digunakan sebagai bahan pengisi untuk meningkatkan kekuatan dan daya tahan semen, mortar dan beton.
- Farmasi: digunakan dalam produksi antasida dan suplemen kalsium. Digunakan sebagai eksipien dalam formulasi tablet dan kapsul.
- Makanan dan Minuman: Digunakan sebagai bahan tambahan makanan untuk membentengi kalsium dan sebagai pengatur pH dalam minuman.
- Kertas dan pulp: Digunakan sebagai bahan pengisi dan pelapis dalam produksi kertas dan papan, untuk meningkatkan kemampuan cetak dan putihnya.
- Plastik: Digunakan sebagai pengisi dan penguat produk plastik, untuk meningkatkan sifat mekanik dan mengurangi biaya.
- Cat dan Pelapis: Digunakan sebagai pigmen dan pengisi pada cat dan pelapis, untuk meningkatkan opasitas dan cakupannya.
- Pertanian: Digunakan sebagai bahan pembenah tanah untuk meningkatkan kualitas tanah dan pertumbuhan tanaman.
- Pengolahan Air: Digunakan untuk menetralkan air asam dan menghilangkan kotoran dari air.
Ini adalah beberapa kegunaan kalsium karbonat yang paling umum, namun ada banyak kegunaan lain di berbagai industri.
Pertanyaan:
Q: Apakah kalsium karbonat larut dalam air?
A: Kalsium karbonat memiliki kelarutan yang rendah dalam air, dengan kelarutan sekitar 0,0013 g/100 mL pada 25°C.
T: Apa itu kalsium karbonat?
A: Kalsium karbonat adalah senyawa kimia dengan rumus CaCO3. Ini adalah zat umum yang ditemukan di bebatuan, cangkang organisme laut dan di berbagai deposit mineral.
T: Di mana Anda bisa menemukan kalsium karbonat?
A: Kalsium karbonat dapat ditemukan di berbagai sumber alam seperti batu kapur, kapur dan marmer. Hal ini juga ditemukan pada cangkang organisme laut seperti tiram, kerang dan karang.
T: Apakah kalsium karbonat bersifat ionik atau kovalen?
A: Kalsium karbonat adalah senyawa ionik yang terdiri dari kation kalsium (Ca2+) dan anion karbonat (CO32-).
T: Kalsium karbonat adalah sejenis sedimen terhidrogenasi yang dapat terkubur dan mengeras menjadi _____.
A: Kalsium karbonat adalah jenis sedimen terhidrogenasi yang dapat terkubur dan mengeras menjadi batu kapur.
T: Struktur berlapis yang terbuat dari kalsium karbonat oleh cyanobacteria Prakambrium disebut _____.
J: Struktur berlapis yang terbuat dari kalsium karbonat oleh cyanobacteria Prakambrium disebut stromatolit.
