Asetofenon atau metilfenil keton merupakan senyawa organik aromatik dengan rumus C8H8O. Ini digunakan dalam produksi parfum dan resin, dan sebagai pelarut dan perantara dalam obat-obatan.
| Nama IUPAC | 1-feniletanon |
| Formula molekul | C8H8O |
| nomor CAS | 98-86-2 |
| Sinonim | Metilfenilketon, fenilmetilketon, AP, asetilbenzena, benzoilmetil, etilfenilketon, Hypnon |
| Di ChI | InciChI=1S/C8H8O/c1-7(9)8-5-3-2-4-6-8/h2-6H,1H3 |
Struktur asetofenon
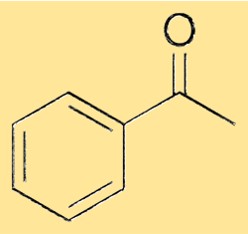
Struktur asetofenon terdiri dari gugus fenil yang terikat pada gugus karbonil melalui ikatan tunggal. Gugus karbonil terdiri dari atom karbon yang terikat ganda pada atom oksigen. Gugus fenil merupakan cincin atom karbon beranggota enam dengan lima atom hidrogen terikat, dan posisi keenam ditempati oleh atom karbon karbonil. Struktur ini memberikan sifat khas pada asetofenon dan memungkinkannya berfungsi sebagai bahan mentah serbaguna untuk sintesis berbagai bahan kimia.
Titik Leleh Asetofenon
Asetofenon memiliki titik leleh -15,7°C. Titik leleh adalah suhu di mana zat padat berubah menjadi cair pada tekanan tetap. Asetofenon merupakan padatan kristal pada suhu kamar dan memiliki titik leleh yang relatif rendah dibandingkan senyawa sejenis lainnya. Titik leleh suatu senyawa ditentukan oleh struktur molekulnya dan kekuatan gaya antarmolekulnya.
Spektrum IR asetofenon
Spektrum IR asetofenon menunjukkan puncak karakteristik pada 1705 cm^-1, yang sesuai dengan gugus karbonil, dan pada 3030-3100 cm^-1, yang sesuai dengan peregangan CH aromatik. Puncak-puncak ini memberikan informasi penting mengenai gugus fungsi yang ada dalam molekul.
Massa molar asetofenon:
Asetofenon memiliki massa molar 120,15 g/mol. Ini adalah senyawa organik aromatik dengan gugus karbonil yang terikat pada cincin fenil. Massa molar adalah jumlah massa atom dari atom-atom yang terkandung dalam satu mol senyawa. Dalam kasus asetofenon, ia memiliki 8 atom karbon, 8 atom hidrogen, dan satu atom oksigen, sehingga totalnya ada 17 atom dalam satu molekul. Massa molar merupakan sifat penting suatu senyawa karena digunakan untuk menghitung jumlah zat dalam sampel tertentu, yang diperlukan untuk berbagai aplikasi dalam kimia dan industri.
Titik didih asetofenon
Asetofenon mempunyai titik didih 202°C. Titik didih adalah suhu di mana zat cair berubah menjadi gas pada tekanan tetap. Asetofenon merupakan senyawa organik yang mudah menguap dan memiliki titik didih yang relatif tinggi dibandingkan senyawa sejenis lainnya. Titik didih suatu senyawa ditentukan oleh kekuatan gaya antarmolekulnya, yaitu gaya yang menyatukan molekul-molekul dalam keadaan cair atau padat. Dalam kasus asetofenon, ia memiliki gugus karbonil polar yang dapat membentuk ikatan hidrogen dengan molekul asetofenon lainnya, yang memperkuat gaya antarmolekul dan meningkatkan titik didih.
Massa jenis metilfenil keton g/ml
Metilfenil keton memiliki massa jenis 1,03 g/mL pada suhu kamar. Massa jenis adalah massa suatu zat per satuan volume. Metilfenil keton berbentuk cair pada suhu kamar dan memiliki massa jenis yang relatif tinggi dibandingkan senyawa sejenis lainnya. Massa jenis suatu senyawa ditentukan oleh berat molekulnya dan massa jenis molekulnya dalam volume tertentu. Dalam kasus metilfenil keton, ia memiliki berat molekul yang relatif tinggi dan struktur molekul yang relatif kompak, sehingga pengemasan molekulnya lebih efisien dan meningkatkan kepadatan.
Berat molekul metilfenil keton
Metilfenil keton memiliki berat molekul 120,15 g/mol. Berat molekul adalah jumlah berat atom seluruh atom dalam suatu molekul. Metilfenil keton memiliki 8 atom karbon, 8 atom hidrogen, dan satu atom oksigen, sehingga menghasilkan total 17 atom dalam satu molekul. Berat molekul merupakan sifat penting suatu senyawa karena digunakan untuk menghitung jumlah zat dalam sampel tertentu, yang diperlukan untuk berbagai aplikasi dalam kimia dan industri.
| Penampilan | Cairan tidak berwarna sampai kuning pucat |
| Berat jenis | 1.028-1.031 pada 25°C |
| Warna | Tidak berwarna sampai kuning pucat |
| Bau | Manis, berbunga-bunga, manis |
| Masa molar | 120,15 g/mol |
| Kepadatan | 1,03 g/mL pada 25°C |
| Titik fusi | -15,7°C |
| Titik didih | 202°C |
| Titik kilat | 78°C |
| Kelarutan dalam air | 3,3 g/L pada 25°C |
| Kelarutan | Larut dalam alkohol, eter, kloroform dan benzena |
| Tekanan uap | 0,27 mmHg pada 25°C |
| Kepadatan uap | 4.15 (udara = 1) |
| pKa | 10.01 |
| pH | Tidak berlaku (metilfenil keton bukan asam atau basa) |
Keamanan dan bahaya metilfenil keton
Metilfenil keton bisa berbahaya jika tidak ditangani dengan benar. Ini dapat menyebabkan iritasi pada kulit, mata dan sistem pernapasan jika bersentuhan atau terhirup. Paparan langsung terhadap uap metilfenil keton konsentrasi tinggi dapat menyebabkan sakit kepala, pusing, atau mual. Menelan metilfenil keton dapat menyebabkan iritasi gastrointestinal, muntah, atau diare. Metilfenil keton juga mudah terbakar dan dapat membentuk campuran yang mudah meledak dengan udara. Itu harus disimpan di tempat yang sejuk, kering, dan berventilasi baik, jauh dari sumber api. Alat pelindung diri, seperti sarung tangan, kacamata pengaman, dan respirator, harus dipakai saat menangani metilfenil keton.
| Simbol bahaya | Xi: Mengiritasi, F: Sangat mudah terbakar |
| Deskripsi Keamanan | S16: Jauhkan dari sumber api – Jangan merokok, S26: Jika kena mata, segera bilas dengan banyak air dan konsultasikan ke dokter, S36: Gunakan pakaian pelindung yang sesuai, S37: Gunakan sarung tangan yang sesuai, S39: Gunakan yang sesuai pakaian pelindung. perlindungan wajah |
| Nomor identifikasi PBB | PBB 2319 |
| kode HS | 291439 |
| Kelas bahaya | 3 (Cairan mudah terbakar) |
| Kelompok pengepakan | AKU AKU AKU |
| Toksisitas | Metilfenil keton diklasifikasikan sebagai iritasi mata Kategori 3 dan iritasi kulit Kategori 4. Itu tidak dianggap karsinogen atau mutagen. LD50 oral (dosis mematikan untuk 50% subjek yang diuji) pada tikus adalah sekitar 3.000 mg/kg. Hal ini tidak dianggap sebagai risiko lingkungan yang signifikan. |
Metode sintesis metilfenil keton
Berbagai metode ada untuk mensintesis metilfenil keton.
Metode yang umum adalah asilasi Friedel-Crafts benzena dengan asetil klorida dengan adanya katalis asam Lewis seperti aluminium klorida. Reaksi ini menghasilkan metilfenil keton dan hidrogen klorida sebagai produk sampingan.
Metode lainnya adalah oksidasi etilbenzena menggunakan udara atau oksigen dengan adanya katalis logam seperti kobalt atau mangan. Reaksi ini menghasilkan metilfenil keton dan asam asetat sebagai produk sampingan.
Metilfenilketon dapat disintesis dengan mereduksi fenilaseton menggunakan zat pereduksi seperti natrium borohidrida atau litium aluminium hidrida. Reaksi ini menghasilkan metilfenil keton dan alkohol yang sesuai sebagai produk sampingan.
Metode lain melibatkan reaksi benzoil klorida dengan etilbenzena dengan adanya katalis aluminium klorida untuk menghasilkan metilfenil keton dan hidrogen klorida sebagai produk sampingan.
Kegunaan metilfenil keton
Metilfenil keton memiliki beberapa kegunaan di berbagai industri.
- Metilfenil keton banyak digunakan sebagai pelarut berbagai resin, ester selulosa dan plastik.
- Industri makanan menggunakan metilfenil keton sebagai bahan penyedap rasa, khususnya untuk rasa ceri dan almond.
- Industri parfum menggunakan metilfenil keton sebagai bahan baku produksi parfum dan produk pewangi lainnya.
- Berbagai bahan kimia seperti obat-obatan, agrokimia dan pewarna disintesis menggunakan metilfenil keton.
- Methylphenylketone berfungsi sebagai perantara dalam produksi fenilaseton, prekursor untuk sintesis amfetamin.
- Coumarin, wewangian yang digunakan dalam sabun dan deterjen, disintesis dari metilfenil keton.
- Reagen kimia organik menggunakan metilfenil keton sebagai reagen untuk sintesis berbagai senyawa.
- Methylphenylketone berfungsi sebagai bahan baku produksi bahan kimia lain seperti styrene dan methylstyrene.
Secara keseluruhan, metil fenil keton memiliki aplikasi yang luas di berbagai industri karena sifat dan kegunaannya yang serbaguna.
Pertanyaan:
T: Apakah asetofenon bersifat polar?
J: Ya, asetofenon bersifat polar karena adanya gugus karbonil (C=O) dan cincin fenil, yang menciptakan momen dipol.
T: Apakah benzaldehida atau asetofenon lebih polar?
J: Benzaldehida lebih polar daripada asetofenon karena memiliki momen dipol yang lebih tinggi karena adanya gugus aldehida (CHO) selain cincin fenil.
Q: Spektrum IR asetofenon?
A: Spektrum IR asetofenon menunjukkan pita serapan yang kuat dan lebar sekitar 1700 cm^-1, yang merupakan karakteristik vibrasi regangan karbonil (C=O). Ia juga menunjukkan puncak sekitar 3000-3100 cm^-1, yang sesuai dengan vibrasi regangan CH aromatik.
T: Dari asetofenon menjadi asam benzoat?
A: Asetofenon dapat diubah menjadi asam benzoat melalui oksidasi menggunakan zat pengoksidasi seperti kalium permanganat atau asam kromat. Reaksi ini mengakibatkan pemutusan ikatan karbon-karbon yang berdekatan dengan gugus karbonil, diikuti dengan oksidasi zat antara yang dihasilkan untuk menghasilkan asam benzoat.
T: Dari benzena menjadi asetofenon?
A: Benzena dapat diubah menjadi asetofenon melalui asilasi Friedel-Crafts menggunakan asetil klorida atau asetat anhidrida dengan adanya katalis asam Lewis seperti aluminium klorida. Reaksi ini menghasilkan substitusi atom hidrogen benzena dengan gugus asetil (-COCH3), diikuti penataan ulang membentuk asetofenon.
