Klorin heptoksida atau Cl2O7 adalah senyawa yang sangat mudah meledak dan reaktif. Ia dapat terurai dengan cepat jika bersentuhan dengan bahan organik dan merupakan zat pengoksidasi kuat yang digunakan dalam sintesis dan analisis kimia.
| Nama IUPAC | Klorin heptoksida |
| Formula molekul | Cl2O7 |
| nomor CAS | 12015-53-1 |
| Sinonim | Perklorat anhidrida, diklorin heptoksida, klor (VII) oksida, klor oksida, perkloril perklorat |
| Di ChI | InChI=1S/Cl2O7/c2-1(3,4,5,6)10-7(8,9)11-12-13-14-10 |
Massa molar Klorin Heptoksida
Klorin heptoksida, rumus kimia Cl2O7, memiliki massa molar 182,9 g/mol. Senyawa ini terdiri dari dua atom klor dan tujuh atom oksigen, menjadikannya zat pengoksidasi yang tinggi. Massa molar klorin heptoksida digunakan untuk menghitung jumlah zat dalam massa atau volume sampel tertentu menggunakan konstanta Avogadro.
Titik didih klorin heptoksida
Klorin heptoksida adalah padatan tidak berwarna sampai kekuningan, sangat reaktif dan mudah menguap. Titik didih klorin heptoksida tidak dapat ditentukan dengan jelas karena ia terurai sebelum mencapai titik didihnya. Klorin heptoksida adalah zat pengoksidasi kuat yang dapat bereaksi dengan bahan organik, air, dan zat lain membentuk senyawa yang mudah meledak.
Titik lebur klorin heptoksida
Klorin heptoksida memiliki titik leleh -96°C (-141°F), menjadikannya padatan dengan titik leleh rendah. Klorin heptoksida dapat berbentuk cairan kekuningan pada suhu kamar karena titik lelehnya yang rendah dan reaktivitasnya yang tinggi. Penting untuk menangani klorin heptoksida dengan hati-hati karena dapat menyebabkan luka bakar parah dan merupakan zat pengoksidasi kuat.
Kepadatan klorin heptoksida g/ml
Massa jenis klorin heptoksida adalah 2,48 g/mL pada suhu kamar. Kepadatan klorin heptoksida yang tinggi menjadikannya cairan padat yang dapat dengan cepat tenggelam ke dasar wadah. Kepadatan dan reaktivitas klorin heptoksida yang tinggi menjadikannya senyawa yang sulit ditangani dan memerlukan tindakan pencegahan keamanan khusus saat digunakan dalam sintesis atau analisis kimia.
Berat Molekul Klorin Heptoksida
Berat molekul klorin heptoksida, juga dikenal sebagai massa molekul relatif, adalah 182,9 g/mol. Berat molekul klorin heptoksida penting dalam perhitungan kimia yang melibatkan jumlah zat, massa dan volume. Berat molekul klorin heptoksida yang tinggi menjadikannya senyawa padat dan mudah menguap sehingga memerlukan penanganan dan penyimpanan yang hati-hati.
Struktur klorin heptoksida
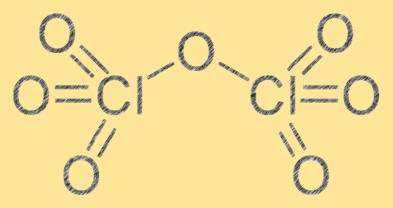
Struktur klorin heptoksida terdiri dari dua atom klor dan tujuh atom oksigen. Ia memiliki rumus molekul Cl2O7 dan geometri molekulnya berbentuk oktahedral yang terdistorsi karena tolakan antar atom oksigen. Klorin heptoksida merupakan oksidator kuat dan dapat bereaksi dengan berbagai zat organik dan anorganik. Struktur klorin heptoksida penting untuk memahami sifat kimianya dan perilakunya dalam berbagai reaksi.
Rumus klorin heptoksida
Rumus kimia klorin heptoksida adalah Cl2O7. Rumusnya menunjukkan bahwa setiap molekul klor heptoksida mengandung dua atom klor dan tujuh atom oksigen. Rumus tersebut digunakan untuk menghitung stoikiometri reaksi kimia yang melibatkan klorin heptoksida. Rumus klorin heptoksida juga penting dalam menentukan berat molekul, kepadatan, dan sifat fisik dan kimia lainnya.
| Penampilan | Padatan tidak berwarna sampai kekuningan |
| Berat jenis | 2,48 pada 25°C |
| Warna | Tidak berwarna sampai kekuningan |
| Bau | Pedas, asam |
| Masa molar | 182,9 g/mol |
| Kepadatan | 2,48 g/mL pada 25°C |
| Titik fusi | -96°C (-141°F) |
| Titik didih | Terurai sebelum titik didih |
| Titik kilat | Tak dapat diterapkan |
| Kelarutan dalam air | Bereaksi hebat dengan air |
| Kelarutan | Larut dalam pelarut organik |
| Tekanan uap | Tidak tersedia |
| Kepadatan uap | Tidak tersedia |
| pKa | Tidak tersedia |
| pH | Tak dapat diterapkan |
Keamanan dan bahaya klorin heptoksida
Klorin heptoksida adalah senyawa yang sangat reaktif dan berbahaya yang menimbulkan risiko keamanan yang signifikan jika tidak ditangani dengan benar. Bahan ini dapat menyebabkan luka bakar parah dan kerusakan pada mata, kulit, dan sistem pernapasan jika terkena. Klorin heptoksida juga dapat bereaksi hebat dengan air dan bahan organik sehingga menyebabkan ledakan dan bahaya kebakaran. Penting untuk menggunakan alat pelindung diri yang sesuai, termasuk sarung tangan, kacamata dan respirator saat menangani klorin heptoksida. Senyawa tersebut harus disimpan dan diangkut dalam wadah yang aman dan tertutup rapat, jauh dari sumber api, panas atau lembab. Prosedur penanganan yang tepat dan tindakan pencegahan keselamatan harus diikuti untuk meminimalkan risiko yang terkait dengan klorin heptoksida.
| Simbol bahaya | Agen pengoksidasi, korosif |
| Deskripsi Keamanan | Hindari kontak dengan air, asam, bahan organik dan zat pereduksi. Gunakan alat pelindung diri yang sesuai. Simpan dalam wadah tertutup rapat jauh dari panas, kelembapan dan sumber api. Jika terjadi kontak dengan mata, kulit atau sistem pernapasan, segera dapatkan bantuan medis. |
| Nomor identifikasi PBB | PBB 3083 |
| kode HS | 28299090 |
| Kelas bahaya | 5.1 (Bahan pengoksidasi) |
| Kelompok pengepakan | II |
| Toksisitas | Sangat beracun jika terhirup, tertelan atau terserap oleh kulit. Menyebabkan luka bakar parah dan kerusakan jaringan. Dapat menyebabkan ledakan dan bahaya kebakaran jika terkena air, bahan organik, dan zat reaktif lainnya. |
Metode sintesis klorin heptoksida
Klorin heptoksida merupakan senyawa yang sangat reaktif dan sulit disintesis.
Salah satu metode paling umum untuk mensintesis klor heptoksida adalah dengan mereaksikan gas klor dan ozon. Reaksi ini bersifat eksotermik dan dapat menyebabkan reaksi eksplosif jika tidak dikontrol dengan hati-hati.
Metode lain melibatkan reaksi gas klor dengan kalium klorat, yang menghasilkan klor heptoksida dan kalium klorida sebagai produk sampingan. Metode ini juga memerlukan kontrol yang cermat terhadap kondisi reaksi untuk mencegah pembentukan bahan antara yang mudah meledak.
Klorin heptoksida dapat disintesis dengan mereaksikan gas klor dengan diklorin pentoksida, yang menghasilkan klor heptoksida dan diklorin heksoksida sebagai produk sampingan. Namun, para peneliti jarang menggunakan metode ini karena sifat diklorin pentoksida yang berbahaya.
Metode lain untuk mensintesis klor heptoksida termasuk mereaksikan gas klor dengan berbagai senyawa organik, seperti benzena atau toluena, dalam kondisi terkendali. Namun, metode ini memerlukan optimalisasi kondisi reaksi yang cermat dan tidak dapat diandalkan atau umum digunakan seperti metode klor-ozon atau klor-kalium klorat.
Secara keseluruhan, sintesis klorin heptoksida memerlukan pengendalian kondisi reaksi yang cermat dan menimbulkan risiko keamanan yang signifikan karena sifat senyawa yang sangat reaktif. Tindakan pencegahan keselamatan dan prosedur penanganan yang tepat harus diikuti ketika bekerja dengan klorin heptoksida atau zat berbahaya lainnya.
Kegunaan Klorin Heptoksida
- Cl2O7 menemukan kegunaan utamanya sebagai zat pengoksidasi dalam sintesis dan penelitian kimia.
- Ia bertindak sebagai oksidan kuat, bereaksi dengan berbagai senyawa organik dan anorganik, sehingga berguna dalam banyak reaksi kimia.
- Salah satu kegunaan Cl2O7 yang paling umum adalah produksi klorin dioksida, zat disinfektan dan pemutih yang kuat yang digunakan dalam pengolahan air, produksi pulp dan kertas, dan manufaktur tekstil.
- Ia juga digunakan sebagai oksidan kuat dalam sintesis beberapa senyawa organik, termasuk obat-obatan dan bahan kimia pertanian.
- Cl2O7 digunakan dalam dunia akademis dan penelitian untuk mempelajari reaktivitas berbagai senyawa organik dan anorganik. Ini juga berfungsi sebagai katalis dalam sintesis senyawa tertentu, seperti resin epoksi dan asetat anhidrida.
- Karena sifatnya yang berbahaya, aplikasi industri skala besar umumnya tidak menggunakan Cl2O7. Hal ini memerlukan penanganan dan penyimpanan yang hati-hati untuk menghindari pembentukan zat antara yang mudah meledak dan bahaya keselamatan lainnya.
Secara keseluruhan, Cl2O7 adalah senyawa yang berguna dalam sintesis dan penelitian kimia, namun memerlukan tindakan pencegahan keselamatan dan prosedur penanganan yang tepat untuk meminimalkan risiko yang terkait dengan penggunaannya.
Pertanyaan:
T: Apa itu Cl2O7?
A: Cl2O7 adalah senyawa kimia yang tersusun dari dua atom klor dan tujuh atom oksigen, dengan rumus kimia Cl2O7.
T: Apa nama yang benar untuk Cl2O7?
J: Nama yang benar untuk Cl2O7 adalah diklorin heptoksida.
Q: Apakah Cl2O7 bersifat ionik atau kovalen?
Jawaban: Cl2O7 merupakan senyawa kovalen. Ia terdiri dari dua unsur non-logam, klorin dan oksigen, dan membentuk senyawa molekuler melalui pembagian elektron antar atom.
Q: Oksida manakah di bawah ini yang bereaksi dengan air membentuk asam lemah? MgO, Cl2O7, P4O10, Bi2O3, N2O5.
A: Oksida yang bereaksi dengan air membentuk asam lemah adalah N2O5. Ketika N2O5 bereaksi dengan air akan membentuk asam nitrat yang merupakan asam lemah. Oksida lain yang terdaftar, MgO, P4O10, Bi2O3 dan Cl2O7, tidak bereaksi dengan air membentuk asam lemah.
