Ion karbonat, CO32-, adalah ion bermuatan negatif yang terdiri dari satu atom karbon, tiga atom oksigen, dan muatan keseluruhan -2. Hal ini umumnya ditemukan dalam mineral seperti kalsit dan dolomit, serta dalam larutan berair seperti bikarbonat. Ini memainkan peran penting dalam mengendalikan tingkat pH di laut dan perairan lainnya.
| Nama IUPAC | Ion Karbonat |
| Formula molekul | CO32- |
| nomor CAS | 497-19-8 |
| Sinonim | Asam karbonat, Karbon trioksida |
| Di ChI | InChI=1S/CH2O3.2K/c2-1(3)4;/h(H2,2,3,4);/q;+2/p-2 |
Sifat ion karbonat
Rumus Karbonat
Rumus ion karbonat dilambangkan dengan CO3^2-, dengan C melambangkan karbon, O melambangkan oksigen, dan simbol 2- melambangkan muatan negatif ion tersebut. Rumus ini menunjukkan bahwa terdapat tiga atom oksigen dan satu atom karbon dalam ion karbonat, sehingga memberikan karakteristik struktur molekulnya.
Muatan Karbonat CO3
Ion karbonat, CO3^2-, memiliki muatan negatif 2 karena adanya tiga atom oksigen dan satu atom karbon dalam rumus kimianya. Muatan negatif dihasilkan dari adanya elektron ekstra pada ion karbonat, menjadikannya ion bermuatan negatif.
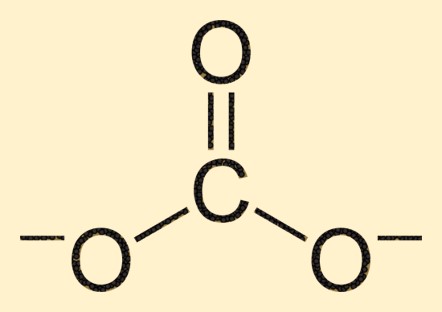
Struktur karbonat
Ion karbonat terdiri dari atom karbon di pusatnya, dikelilingi oleh tiga atom oksigen dalam susunan trigonal planar. Atom karbon membentuk ikatan rangkap dengan atom oksigen, sedangkan dua atom oksigen lainnya terikat ke atom karbon melalui ikatan tunggal. Struktur ini memberikan ion CO3 2- bentuk dan sifat khasnya.
Berat Molekul Ion Karbonat
Berat molekul ion karbonat kira-kira 60,01 g/mol, dihitung berdasarkan berat atom unsur penyusunnya (karbon, oksigen). Berat molekul asam karbonat penting dalam menentukan jumlah asam karbonat dalam suatu sampel, serta menentukan sifat fisik dan kimianya.
| Penampilan | Bubuk putih padat |
| Berat jenis | 2.5 |
| Warna | Putih |
| Bau | Tidak ada |
| Masa molar | 100,09 g/mol |
| Kepadatan | 2,83 gram/cm3 |
| Titik fusi | 825°C |
| Titik didih | 1484°C |
| Titik kilat | Tak dapat diterapkan |
| Kelarutan dalam air | Larut dalam air |
| Kelarutan | Larut dalam asam |
| Tekanan uap | Tak dapat diterapkan |
| Kepadatan uap | Tak dapat diterapkan |
| PKa | 10:33 |
| PH | 8.6 |
Keamanan dan bahaya ion karbonat
Ion karbonat, CO32-, banyak digunakan di berbagai industri, namun harus ditangani dengan hati-hati. Menghirup debu karbonat dalam kadar tinggi dapat menyebabkan gangguan pernafasan, sedangkan menelannya dalam jumlah banyak dapat menyebabkan gangguan pencernaan. Kontak dengan kulit dapat menyebabkan iritasi dan lesi kulit. Ia juga mudah terbakar dan dapat bereaksi dengan bahan kimia lain untuk menghasilkan gas berbahaya. Penting untuk mengikuti langkah-langkah keselamatan, seperti memakai alat pelindung diri dan menyimpan ion karbonat dalam wadah yang sesuai, untuk meminimalkan risiko kecelakaan.
| Simbol bahaya | Tidak ada |
| Deskripsi Keamanan | Ini tidak dianggap berbahaya dan tidak dikaitkan dengan simbol bahaya tertentu. |
| ID | T/A |
| kode HS | T/A |
| Kelas bahaya | T/A |
| Kelompok pengepakan | T/A |
| Toksisitas | Tidak beracun |
Metode sintesis ion karbonat
Ion karbonat (CO3 2- ) dapat disintesis dengan berbagai metode berbeda. Metode yang paling umum untuk menghasilkan ion CO3 2- adalah dengan mereaksikan karbon dioksida dan air. Reaksi ini menghasilkan larutan asam karbonat, yang kemudian dapat dinetralkan dengan alkali, seperti natrium hidroksida, untuk menghasilkan asam karbonat. Asam karbonat juga dapat diproduksi melalui elektrolisis larutan garam, dimana ion karbonat terbentuk di katoda. Ion-ion ini juga dapat diproduksi di laboratorium melalui reaksi kimia antara asam dan garam karbonat.
Kegunaan Ion Karbonat
Industri banyak menggunakan asam karbonat untuk berbagai keperluan. Produsen baking powder, produsen antasida, dan perusahaan minuman biasanya memasukkan asam karbonat ke dalam produk mereka. Industri pengolahan air mengontrol tingkat pH dalam air minum dan kolam renang menggunakan ion karbonat. Industri konstruksi menggunakan ion CO3 2- sebagai komponen utama semen untuk membuat beton. Petani menambahkan ion karbonat ke dalam tanah untuk meningkatkan alkalinitasnya dan mendorong pertumbuhan tanaman. Industri kimia menggunakan ion karbonat sebagai katalis dan reagen dalam berbagai reaksi kimia. Industri makanan mengawetkan makanan dengan memasukkan ion karbonat. Karena keserbagunaannya, ion karbonat memainkan peran penting dalam banyak produk sehari-hari dan proses industri.
