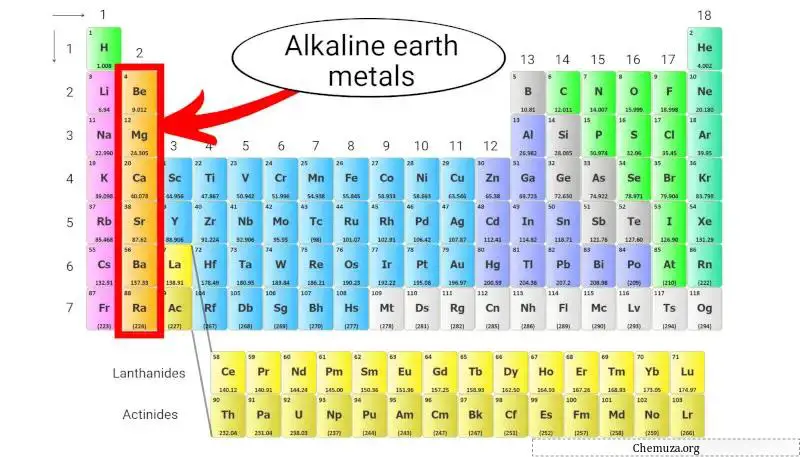
Logam alkali tanah merupakan sekelompok unsur yang terletak pada kolom kedua tabel periodik . Mereka termasuk berilium (Be), magnesium (Mg), kalsium (Ca), strontium (Sr), barium (Ba) dan radium (Ra).
Logam-logam ini memiliki dua elektron pada kulit terluarnya, [1] yang menjadikannya reaktif secara kimia tetapi tidak reaktif seperti logam alkali , yang berada pada kolom pertama.
Mari kita telusuri lebih jauh tentang logam alkali tanah pada tabel periodik.
Apa itu logam alkali tanah?

Logam alkali tanah merupakan bagian dari golongan 2 tabel periodik dan memiliki dua ciri khusus.
- Ketika bereaksi dengan air, mereka menghasilkan hidroksida yang bersifat basa atau basa.
- Mineral oksidanya (BeO, magnesit, MgO, beryl, dll.) ditemukan terutama di kerak bumi dan stabil terhadap panas.
Penjelasan
Ketika logam alkali tanah (Mg, Ca, Sr, Ba dan Ra) bereaksi dengan air, mereka membentuk hidroksida yang bersifat basa (atau basa). [2]
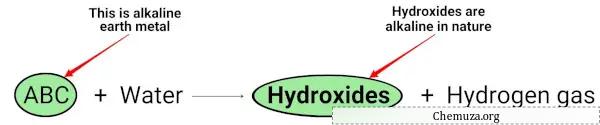
Dapat dilihat pada persamaan kimia di atas bahwa logam alkali menghasilkan hidroksida yang bersifat basa (memiliki pH > 7) dan melepaskan gas hidrogen.
Misalnya:
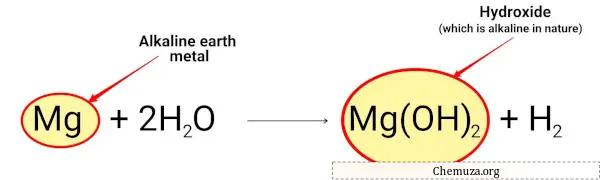
Magnesium bereaksi dengan air dan membentuk magnesium hidroksida yang bersifat basa.
Selain itu, logam-logam ini ditemukan terutama di kerak bumi (sebagai oksida) dan mineral-mineral teroksidasi ini stabil terhadap panas. [2]
Kedua kriteria ini memberi logam ini nama “logam alkali tanah”.
(Catatan: Penting untuk diperhatikan bahwa berilium, yang juga merupakan unsur Golongan 2, tidak membentuk larutan basa ketika bereaksi dengan air. Sebaliknya, hidroksidanya menunjukkan sifat amfoter, yang berarti dapat berperilaku seperti asam atau basa. Oleh karena itu, berilium tidak dianggap sebagai logam alkali tanah meskipun termasuk dalam golongan yang sama.)
Apa kesamaan semua logam alkali tanah?
Logam alkali tanah mempunyai beberapa ciri yang sama.
Misalnya, keduanya memiliki dua elektron valensi pada tingkat energi terluarnya, sehingga keduanya cukup reaktif.
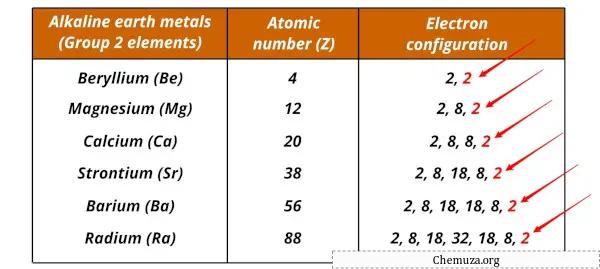
Reaktivitas ini disebabkan oleh kecenderungan kehilangan elektron selama reaksi kimia, sehingga menghasilkan pembentukan kation dengan muatan +2.
Selain itu, semua logam alkali tanah memiliki tampilan putih keperakan yang mengkilat.

Jadi itulah dua kesamaan utama yang dimiliki logam alkali tanah.
Daftar logam alkali dan konfigurasi elektroniknya
Logam alkali tanah dan konfigurasi elektroniknya ditunjukkan di bawah ini.
| Elemen | Konfigurasi elektronik |
| Berilium (Menjadi) | [Dia] 2s 2 |
| magnesium (Mg) | [Lakukan] 3s 2 |
| Kalsium (Ca) | [Ar] 4s 2 |
| Strontium (Sr) | [Kr] 5s 2 |
| Barium (Ba) | [Xe] 6s 2 |
| Radium (Ra) | [Rn] 7 detik 2 |
Tren Berkala Logam Alkali Tanah
Ketika seseorang bergerak ke bawah golongan logam alkali tanah pada tabel periodik, tren berikut dapat diamati:
- Valensi: Semua logam alkali tanah memiliki valensi +2 yang sama. Jadi tidak ada perubahan valensi saat kita turun grup.
- Ukuran atom: Ukuran atom logam alkali tanah meningkat seiring dengan bertambahnya golongan. Hal ini karena jumlah lapisan elektronik (atau orbit ) bertambah dan efek pelindung elektron internal mengurangi gaya tarik-menarik antara inti dan elektron terluar.
- Karakter Logam: Karakter logam logam alkali tanah meningkat seiring dengan bertambahnya golongan ke bawah. Hal ini disebabkan karena atom menjadi lebih besar dan mengandung lebih banyak elektron sehingga lebih mudah melepaskan elektron dan membentuk ion positif.
- Keelektronegatifan: Keelektronegatifan logam alkali tanah menurun seiring dengan penurunan golongan. Hal ini karena atom menjadi lebih besar dan memiliki lebih banyak kulit elektron, sehingga lebih sulit menarik elektron ke dalamnya.
- Afinitas Elektronik: Afinitas elektronik logam alkali tanah umumnya rendah dan menurun seiring dengan bertambahnya golongan ke bawah.
- Energi Ionisasi: Energi ionisasi logam alkali tanah berkurang seiring dengan bertambahnya golongan. Hal ini karena atom yang lebih besar memiliki lebih banyak kulit elektron dan elektron terluar lebih jauh dari inti, sehingga lebih mudah untuk dilepaskan.
Ringkasan
Logam alkali tanah termasuk berilium, magnesium, kalsium, strontium, barium dan radium. Logam ini mempunyai dua elektron pada kulit terluarnya, sehingga membuatnya reaktif namun kurang reaktif dibandingkan logam alkali.
Logam-logam ini menghasilkan alkali hidroksida ketika bereaksi dengan air dan mengandung mineral teroksidasi yang stabil terhadap panas. Ciri-ciri utama yang umum pada semua logam alkali tanah adalah mempunyai dua elektron valensi, berwarna putih keperakan dan mengkilat, serta membentuk kation dengan muatan +2.
Valensi tetap sama ketika seseorang berpindah golongan ke bawah, tetapi ukuran atom dan sifat logam meningkat, sedangkan keelektronegatifan, afinitas elektron, dan energi ionisasi menurun.
