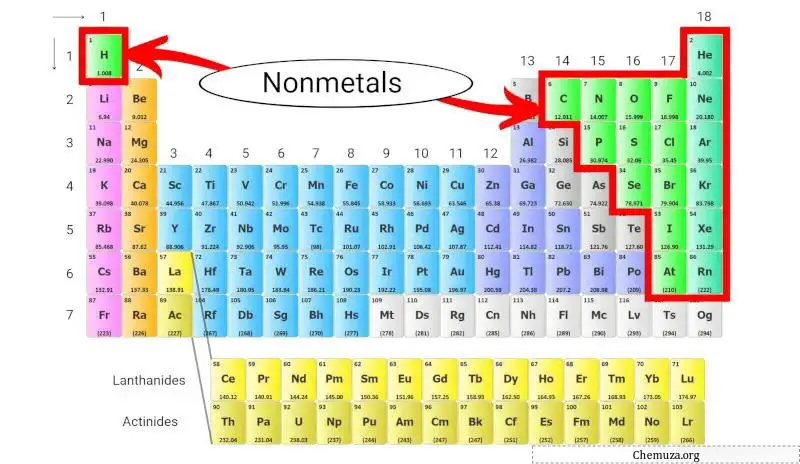
Nonlogam adalah sekelompok unsur yang tidak memiliki sifat logam, seperti konduktivitas listrik dan kilau yang tinggi. Nonlogam ini terletak di sisi kanan tabel periodik , kecuali hidrogen .
Nonlogam dapat ditemukan dalam berbagai bentuk, termasuk gas seperti oksigen dan klor , cairan seperti brom , dan padatan seperti belerang dan karbon . [1]
Mari kita lihat lebih banyak hal penting tentang non-logam.
Apa sebenarnya nonlogam itu?
Nonlogam adalah unsur yang cenderung memperoleh elektron selama reaksi kimia, membentuk ion atau anion bermuatan negatif.
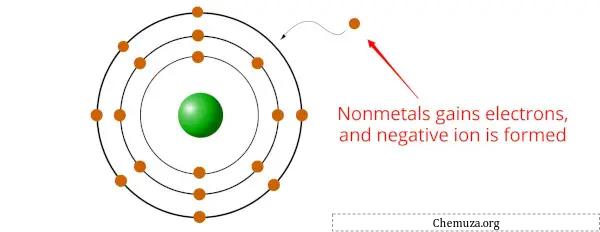
Hal ini karena nonlogam umumnya memiliki keelektronegatifan yang lebih tinggi dibandingkan logam, [2] yang berarti mereka memiliki daya tarik yang lebih besar terhadap elektron.
Ketika nonlogam berikatan dengan logam , unsur nonlogam memperoleh satu atau lebih elektron dari logam untuk membentuk senyawa yang stabil.
Misalnya, klor memperoleh elektron dari natrium untuk membentuk senyawa ionik natrium klorida (NaCl).
Dapat juga dikatakan bahwa – Nonlogam adalah sekelompok unsur kimia yang tidak memiliki sifat fisika dan kimia logam.
Baiklah, mari kita lihat daftar unsur nonlogam yang ada dalam tabel periodik.
Daftar non-logam yang ada dalam tabel periodik
Berikut adalah daftar non-logam yang ada dalam tabel periodik:
- Hidrogen (H)
- Helium (Dia)
- Karbon (C)
- Nitrogen (N)
- Oksigen (O)
- Fluorit (F)
- Neon (Ne)
- Fosfor (P)
- Belerang (S)
- Klorin (Cl)
- Argon (Ar)
- Selenium (Se)
- Brom (Br)
- Kripton (Kr)
- Yodium (saya)
- Xenon (Xe)
- Astatin (Pada)
- Radon (Rn)
Nonlogam ini terletak di sisi kanan tabel periodik, kecuali hidrogen, yang terletak di bagian atas tabel periodik di atas logam alkali .
Keadaan non-logam (padat, cair atau gas?)
Nonlogam dapat berada dalam tiga wujud materi: padat, cair, dan gas.
Keadaan suatu bukan logam bergantung pada kondisi suhu dan tekanan di mana ia terpapar.
Di antara semua non-logam pada tabel periodik;
- 11 nonlogam berada dalam wujud gas pada suhu kamar. [3]
- Brom (Br) adalah non-logam yang ditemukan dalam keadaan cair pada suhu kamar.
- Nonlogam lainnya berbentuk padat pada suhu kamar.
Bukan logam yang paling reaktif
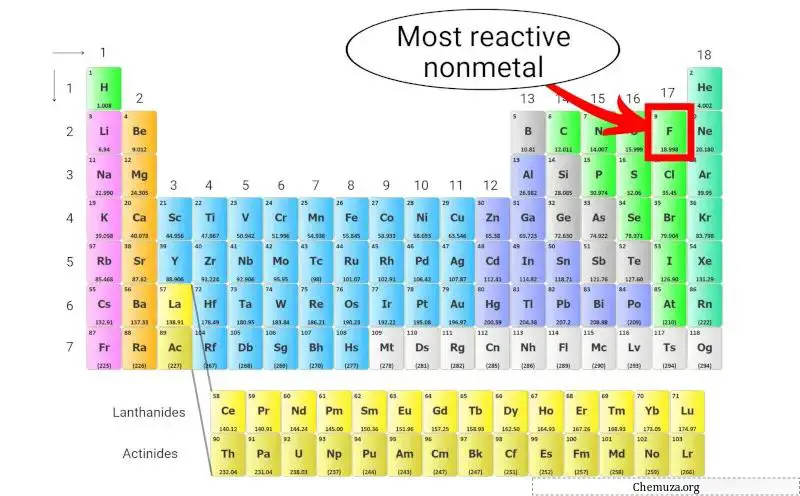
Fluor (F) adalah unsur non-logam paling reaktif yang ada dalam tabel periodik.
Tapi kenapa? Mengapa fluorida paling reaktif?
Hal ini karena ia memiliki keelektronegatifan tertinggi di antara semua unsur, yang berarti ia mempunyai daya tarik yang kuat terhadap elektron.
Fluor memiliki tujuh elektron pada tingkat energi terluarnya dan memerlukan elektron tambahan untuk mengisi kulit valensinya dan mencapai konfigurasi yang stabil.
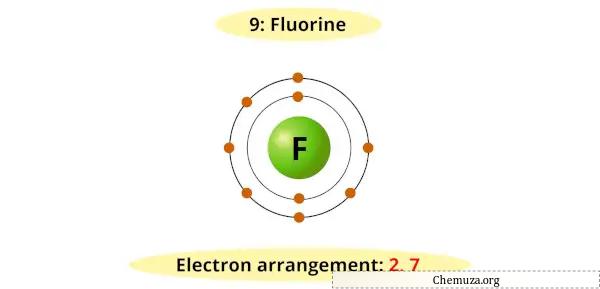
Oleh karena itu, ia mudah menerima elektron dari unsur lain untuk membentuk ion fluorida (F-).
Karena reaktivitasnya yang tinggi, fluor dapat bereaksi secara eksplosif dengan banyak unsur dan senyawa lain, termasuk air, logam, dan bahkan kaca. [4]
Fluor sangat reaktif sehingga biasanya disimpan dan diangkut dalam wadah khusus yang terbuat dari bahan yang tahan terhadap sifat korosifnya.
Peran bukan logam dalam aplikasi lingkungan dan industri
Nonlogam digunakan dalam berbagai proses industri dan aplikasi lingkungan karena sifatnya yang unik. Berikut beberapa contohnya:
- Pengendalian Polusi Udara: Non-logam seperti nitrogen dan oksigen memainkan peran penting dalam mengendalikan polusi udara. Nitrogen oksida (NOx) adalah polutan berbahaya yang dilepaskan dari kendaraan dan proses industri. Katalis non-logam digunakan untuk mengubah NOx menjadi gas tidak berbahaya seperti nitrogen dan air. Demikian pula, oksigen digunakan dalam proses pembakaran untuk mengurangi emisi berbahaya.
- Pupuk: Nitrogen, fosfor dan belerang merupakan nutrisi penting untuk pertumbuhan tanaman. Pupuk non-logam seperti amonium nitrat dan superfosfat banyak digunakan di bidang pertanian untuk meningkatkan hasil panen.
- Baterai: Unsur non-logam seperti belerang, karbon, dan litium digunakan dalam baterai. Baterai litium-ion umumnya digunakan pada perangkat elektronik, kendaraan listrik, dan sistem energi terbarukan.
- Pemurnian air: Non-logam seperti klorin dan yodium biasanya digunakan sebagai desinfektan dalam sistem pemurnian air. Mereka membunuh bakteri dan virus berbahaya serta membuat air aman untuk diminum. [5]
- Manufaktur bahan kimia: Non-logam seperti belerang dan klor banyak digunakan dalam produksi bahan kimia seperti asam sulfat, asam klorida, dan pelarut berbasis klor.
Ringkasan
Nonlogam tidak memiliki sifat logam seperti konduktivitas listrik dan kilau yang tinggi dan terletak di sisi kanan tabel periodik, kecuali hidrogen. Mereka ada di ketiga wujud materi tergantung pada kondisi suhu dan tekanan.
Fluor merupakan nonlogam yang paling reaktif karena elektronegativitasnya yang tinggi dan mudah menerima elektron dari unsur lain untuk membentuk ion fluorida (F-).
Nonlogam memiliki beberapa kegunaan dalam aplikasi lingkungan dan industri, termasuk pengendalian polusi udara, pupuk, baterai, pemurnian air, dan pembuatan bahan kimia.
