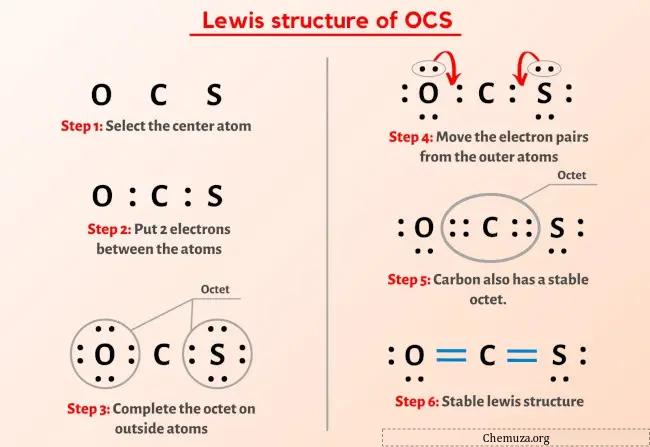
Jadi Anda sudah melihat gambar di atas kan?
Izinkan saya menjelaskan secara singkat gambar di atas.
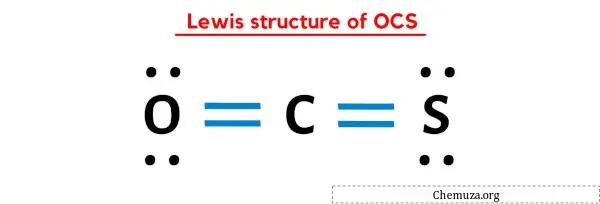
Struktur OCS Lewis memiliki atom karbon (C) di tengahnya yang dikelilingi oleh atom oksigen (O) dan atom sulfur (S). Terdapat 2 ikatan rangkap antara atom karbon (C) dan atom oksigen (O) serta antara atom karbon (C) dan atom belerang (S). Terdapat 2 pasangan elektron bebas pada atom oksigen (O) dan atom belerang (S).
Jika Anda tidak memahami apa pun dari gambar Struktur OCS Lewis di atas, tetaplah bersama saya dan Anda akan mendapatkan penjelasan langkah demi langkah yang mendetail tentang cara menggambar Struktur OCS Lewis.
Jadi mari kita lanjutkan ke langkah menggambar struktur OCS Lewis .
Langkah-langkah Menggambar Struktur OCS Lewis
Langkah 1: Temukan jumlah total elektron valensi dalam molekul OCS
Untuk mengetahui jumlah total elektron valensi dalam molekul OCS , pertama-tama Anda perlu mengetahui elektron valensi yang ada pada atom oksigen, atom karbon, dan juga atom belerang.
(Elektron valensi adalah elektron yang ada di orbit terluar atom mana pun.)
Disini saya akan memberi tahu Anda cara mudah mencari elektron valensi oksigen, karbon, dan belerang menggunakan tabel periodik.
Total elektron valensi dalam molekul OCS
→ Elektron valensi diberikan oleh atom oksigen:

Oksigen adalah unsur dalam golongan 16 tabel periodik. [1] Oleh karena itu, elektron valensi yang ada dalam oksigen adalah 6 .
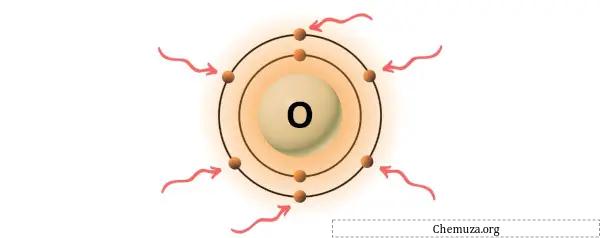
Anda dapat melihat 6 elektron valensi yang ada pada atom oksigen seperti terlihat pada gambar di atas.
→ Elektron valensi diberikan oleh atom karbon:
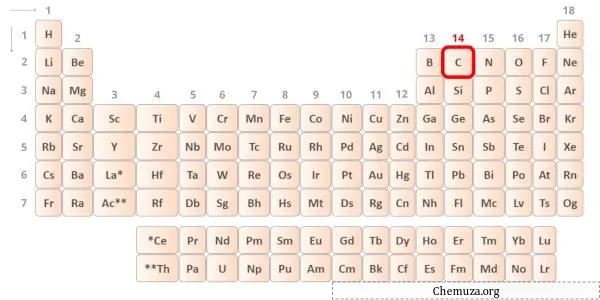
Karbon adalah unsur dalam golongan 14 tabel periodik. [2] Oleh karena itu, elektron valensi yang ada dalam karbon adalah 4 .
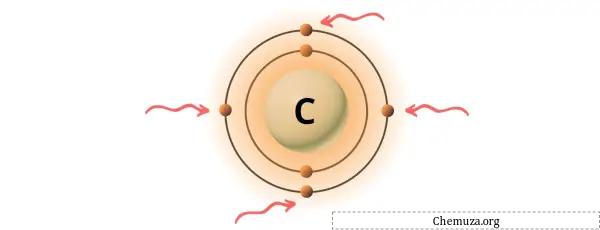
Anda dapat melihat 4 elektron valensi yang ada pada atom karbon seperti terlihat pada gambar di atas.
→ Elektron valensi diberikan oleh atom belerang:
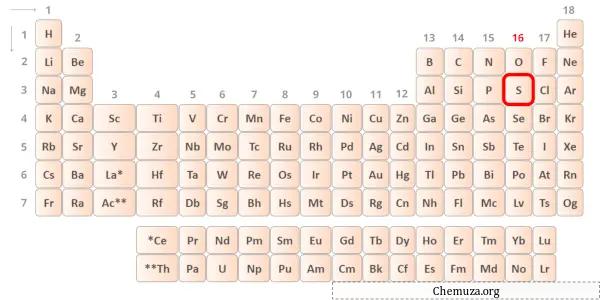
Belerang adalah unsur dalam golongan 16 tabel periodik. [3] Oleh karena itu, elektron valensi yang ada dalam belerang adalah 6 .
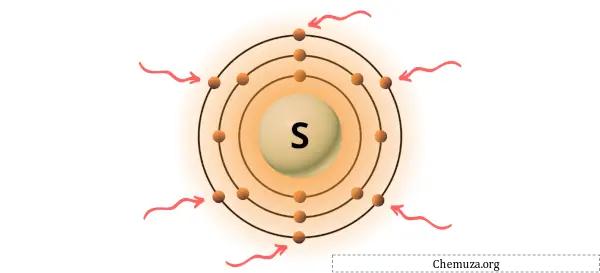
Anda dapat melihat 6 elektron valensi yang terdapat pada atom belerang seperti terlihat pada gambar di atas.
Jadi,
Jumlah elektron valensi dalam molekul OCS = elektron valensi yang disumbangkan oleh 1 atom oksigen + elektron valensi yang disumbangkan oleh 1 atom karbon + elektron valensi yang disumbangkan oleh 1 atom belerang = 6 + 4 + 6 = 16 .
Langkah 2: Pilih atom pusat
Untuk memilih atom pusat, kita harus ingat bahwa atom yang paling elektronegatifnya tetap berada di pusat.
Sekarang molekul yang diberikan adalah OCS dan mengandung satu atom oksigen (O), satu atom karbon (C) dan satu atom sulfur (S).
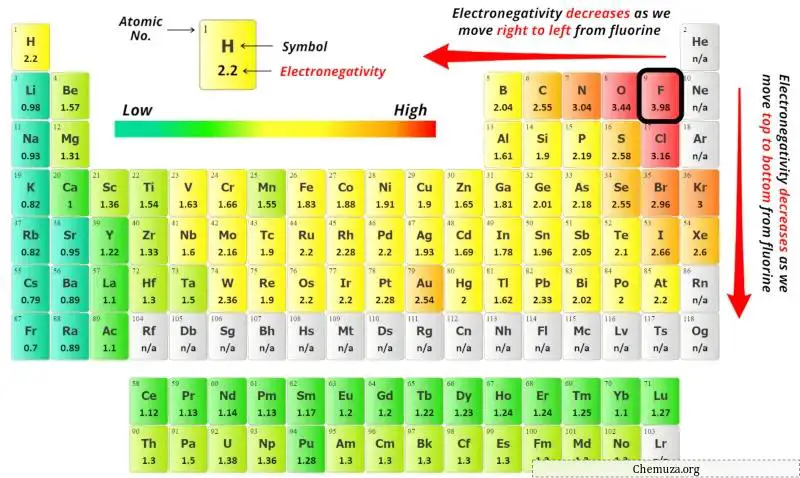
Nilai keelektronegatifan atom oksigen (O), atom karbon (C), dan atom belerang (S) dapat Anda lihat pada tabel periodik di atas.
Jika kita membandingkan nilai keelektronegatifan oksigen (O), karbon (C) dan belerang (S), maka atom karbon kurang elektronegatif .
Di sini, atom karbon (C) adalah atom pusat dan atom oksigen (O) serta atom belerang (S) adalah atom terluar.
Langkah 3: Hubungkan setiap atom dengan menempatkan sepasang elektron di antara keduanya
Sekarang dalam molekul OCS Anda perlu menempatkan pasangan elektron antara atom oksigen, karbon dan sulfur.
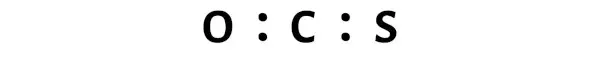
Hal ini menunjukkan bahwa atom-atom ini terikat secara kimia satu sama lain dalam molekul OCS.
Langkah 4: Jadikan Atom Eksternal Stabil
Pada langkah ini Anda perlu memeriksa stabilitas atom luar.
Di sini, pada sketsa molekul OCS, Anda dapat melihat bahwa atom terluar adalah atom karbon dan atom belerang.
Atom-atom eksternal ini membentuk oktet dan karenanya stabil.
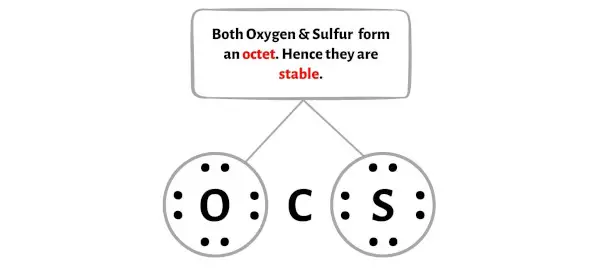
Selain itu, pada langkah 1, kami menghitung jumlah elektron valensi yang ada dalam molekul OCS.
Molekul OCS memiliki total 16 elektron valensi dan semua elektron valensi ini digunakan dalam diagram OCS di atas.
Oleh karena itu, tidak ada lagi pasangan elektron yang dapat disimpan pada atom pusat.
Jadi sekarang mari kita lanjutkan ke langkah berikutnya.
Langkah 5: Periksa oktet pada atom pusat. Jika tidak mempunyai oktet, pindahkan pasangan elektron bebasnya sehingga membentuk ikatan rangkap dua atau ikatan rangkap tiga.
Pada langkah ini, Anda perlu memeriksa apakah atom karbon pusat (C) stabil atau tidak.
Untuk memeriksa kestabilan atom karbon pusat (C), kita perlu memeriksa apakah atom tersebut membentuk oktet atau tidak.
Sayangnya, atom karbon tidak membentuk oktet di sini. Karbon hanya memiliki 4 elektron dan tidak stabil.
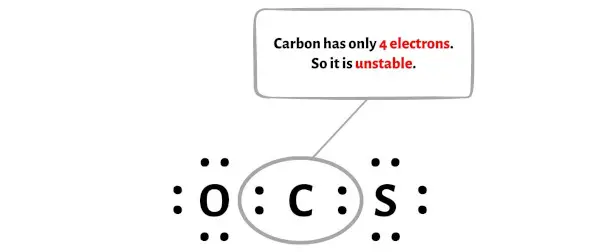
Nah, untuk membuat atom karbon ini stabil, Anda perlu menggeser pasangan elektron dari atom oksigen terluar agar atom karbon tersebut dapat memiliki 8 elektron (yaitu satu oktet).

Namun setelah berpindah sepasang elektron, atom karbon tetap tidak membentuk oktet karena hanya memiliki 6 elektron.

Sekali lagi, kita perlu memindahkan sepasang elektron tambahan dari atom belerang.

Setelah pasangan elektron ini berpindah, atom karbon pusat akan menerima 2 elektron lagi dan total elektronnya menjadi 8.

Anda dapat melihat pada gambar di atas bahwa atom karbon membentuk oktet.
Dan karena itu atom karbon stabil.
Sekarang mari kita beralih ke langkah terakhir untuk memeriksa apakah struktur Lewis OCS stabil atau tidak.
Langkah 6: Periksa stabilitas struktur Lewis
Sekarang Anda telah sampai pada langkah terakhir di mana Anda perlu memeriksa stabilitas struktur Lewis OCS.
Stabilitas struktur Lewis dapat diverifikasi dengan menggunakan konsep muatan formal .
Singkatnya, sekarang kita harus mencari muatan formal pada atom oksigen (O), atom karbon (C) serta atom belerang (S) yang ada dalam molekul OCS.
Untuk menghitung pajak formal, Anda harus menggunakan rumus berikut:
Muatan formal = Elektron valensi – (Elektron ikatan)/2 – Elektron non-ikatan
Jumlah elektron ikatan dan elektron non-ikatan setiap atom molekul OCS dapat Anda lihat pada gambar di bawah ini.
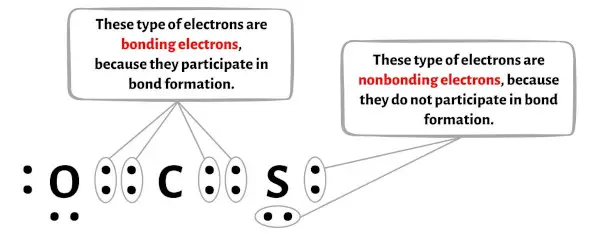
Untuk atom oksigen (O):
Elektron valensi = 6 (karena oksigen berada pada golongan 16)
Elektron ikatan = 4
Elektron tidak terikat = 4
Untuk atom karbon (C):
Elektron valensi = 4 (karena karbon berada pada golongan 14)
Elektron ikatan = 8
Elektron tidak terikat = 0
Untuk atom Sulfur (S):
Elektron valensi = 6 (karena belerang termasuk golongan 16)
Elektron ikatan = 4
Elektron tidak terikat = 4
| Tuduhan formal | = | elektron valensi | – | (Mengikat elektron)/2 | – | Elektron yang tidak terikat | ||
| Oh | = | 6 | – | 4/2 | – | 4 | = | 0 |
| VS | = | 4 | – | 8/2 | – | 0 | = | 0 |
| S | = | 6 | – | 4/2 | – | 4 | = | 0 |
Dari perhitungan muatan formal di atas terlihat bahwa atom oksigen (O), karbon (C) dan belerang (S) mempunyai muatan formal “nol” .
Hal ini menunjukkan bahwa struktur OCS Lewis di atas stabil dan tidak ada perubahan lebih lanjut pada struktur OCS di atas.
Dalam struktur titik Lewis OCS di atas, Anda juga dapat menyatakan setiap pasangan elektron ikatan (:) sebagai ikatan tunggal (|). Melakukan hal ini akan menghasilkan struktur Lewis OCS berikut.
Saya harap Anda telah memahami sepenuhnya semua langkah di atas.
Untuk lebih banyak latihan dan pemahaman yang lebih baik, Anda dapat mencoba struktur Lewis lainnya yang tercantum di bawah.
Cobalah (atau setidaknya lihat) struktur Lewis ini untuk pemahaman yang lebih baik:
