Fosgen adalah gas beracun yang digunakan dalam proses industri dan peperangan. Menghirupnya menimbulkan risiko kesehatan yang serius, menyebabkan kerusakan pernafasan dan bisa berakibat fatal.
| Nama IUPAC | Karbonil diklorida |
| Formula molekul | COCl2 |
| nomor CAS | 75-44-5 |
| Sinonim | Karbonat diklorida, gas fosgen, karbonil klorida |
| Di ChI | InChI=1S/CCl2O/c2-1(3)4 |
Sifat fosgen
Rumus Fosgen
Rumus kimia fosgen atau karbon diklorida adalah COCl2. Terdiri dari satu atom karbon (C), satu atom oksigen (O) dan dua atom klor (Cl). Komposisi molekul ini penting untuk memahami sifat dan reaksinya.
Massa Molar Fosgen
Massa molar karbon diklorida kira-kira 98,92 g/mol. Dihitung dengan menjumlahkan massa atom penyusunnya, yaitu karbon (12,01 g/mol), oksigen (16,00 g/mol), dan klor (masing-masing 35,45 g/mol).
Titik didih fosgen
Karbonat diklorida memiliki titik didih yang relatif rendah sekitar -23,3°C (-9,94°F). Pada suhu ini, ia berubah dari wujud cair menjadi gas, yang sangat penting untuk penerapannya dalam berbagai proses industri.
Titik Leleh Fosgen
Titik leleh karbon dioksida cukup rendah, sekitar -118,3°C (-180,94°F). Pada suhu ini, bentuk padat karbon diklorida berubah menjadi cair. Memahami sifat ini penting untuk menangani karbon diklorida dengan aman.
Kepadatan fosgen g/mL
Karbonat diklorida memiliki kepadatan sekitar 1,432 g/mL pada suhu kamar (25°C atau 77°F). Sifat ini sangat penting dalam menentukan perilaku dan interaksinya dengan zat lain.
Berat Molekul Fosgen
Berat molekul karbon diklorida adalah 98,92 g/mol. Nilai ini sangat penting untuk berbagai perhitungan dalam kimia, termasuk stoikiometri dan menentukan jumlah karbon diklorida yang diperlukan untuk reaksi.
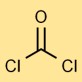
Struktur fosgen
Karbonat diklorida memiliki struktur molekul linier, dimana atom karbon terikat ganda pada atom oksigen dan terikat tunggal pada setiap atom klor. Pengaturan ini mempengaruhi daya tanggap dan stabilitasnya.
Kelarutan fosgen
Karbonat diklorida sulit larut dalam air, dan hanya sedikit gas yang larut dalam cairan. Namun, ia dapat bereaksi dengan air menghasilkan asam klorida dan karbon dioksida, sehingga berbahaya di lingkungan berair.
Memahami sifat-sifat karbonat diklorida ini penting untuk menangani dan menggunakan bahan kimia secara aman dalam aplikasi industri dan pengaturan lainnya. Tindakan pencegahan yang tepat harus selalu dilakukan saat menangani senyawa beracun dan reaktif ini untuk mencegah kecelakaan dan bahaya kesehatan.
| Penampilan | Gas tidak berwarna |
| Berat jenis | 3.428 (gas) |
| Warna | T/A |
| Bau | Mencekik, menyengat |
| Masa molar | 98,92 g/mol |
| Kepadatan | 1,432 g/mL (cair) |
| Titik fusi | -118,3°C (-180,94°F) |
| Titik didih | -23,3°C (-9,94°F) |
| Titik kilat | T/A |
| Kelarutan dalam air | Bereaksi dengan air |
| Kelarutan | Bereaksi dengan air menghasilkan asam klorida dan karbon dioksida |
| Tekanan uap | 736 mmHg (25°C) |
| Kepadatan uap | 2,98 (udara = 1) |
| pKa | T/A |
| pH | T/A |
Sifat fisikokimia ini memberikan informasi penting tentang karbon diklorida, memfasilitasi penanganan yang aman dan memahami perilakunya di berbagai lingkungan.
Keamanan dan bahaya fosgen
Karbonat diklorida menimbulkan risiko keamanan yang signifikan karena sifatnya yang beracun dan reaktif. Saat menangani karbon diklorida, kenakan alat pelindung diri (APD) yang sesuai, termasuk pelindung pernapasan, sarung tangan, dan pelindung mata. Pastikan ventilasi yang memadai di area kerja untuk menghindari paparan melalui inhalasi. Hindari kontak dengan kulit dan mata karena dapat menyebabkan iritasi serius dan luka bakar. Gas karbon diklorida tidak berbau sehingga sulit dideteksi. Oleh karena itu, perangkat pemantauan sangatlah penting. Jika terpapar, segera dapatkan bantuan medis. Simpan dan angkut karbon diklorida dengan aman, sesuai peraturan dan praktik terbaik. Memahami bahayanya sangat penting untuk mencegah kecelakaan dan melindungi kesehatan manusia dan lingkungan.
| Simbol bahaya | Tengkorak dan tulang bersilang |
| Deskripsi Keamanan | Gas yang sangat beracun. Tangani dengan sangat hati-hati. Gunakan APD yang sesuai. Hindari penghirupan dan kontak dengan kulit. |
| Nomor identifikasi PBB | UN1076 |
| kode HS | 2812.10.0000 |
| Kelas bahaya | 2.3 (Gas beracun) |
| Kelompok pengepakan | SAYA |
| Toksisitas | Fosgen sangat beracun dan dapat berakibat fatal jika terhirup atau terkena kulit. Gunakan langkah-langkah keamanan yang ketat. |
Memahami aspek risiko dan keselamatan karbon diklorida sangat penting untuk penanganan yang aman dan pencegahan kecelakaan. Bahan ini sangat beracun dan menimbulkan risiko kesehatan yang signifikan, sehingga prosedur keselamatan dan tindakan pencegahan yang tepat menjadi penting.
Metode sintesis fosgen
Beberapa metode memungkinkan sintesis karbon diklorida.
Pendekatan yang umum adalah “proses Diakon”, di mana gas klor bereaksi dengan karbon monoksida pada suhu tinggi dengan adanya katalis yang sesuai seperti tembaga(II) klorida . Metode lain melibatkan “klorinasi langsung” karbon monoksida dengan gas klor, yang difasilitasi oleh besi atau logam klorida lainnya sebagai katalis.
Produksi karbonat diklorida melibatkan “karbonilasi oksidatif” metilen klorida atau metil klorida, menggunakan oksigen dan katalis logam seperti kupro klorida. Metode lain untuk mensintesis karbonat diklorida adalah “rute urea”, yang menghasilkan karbonat diklorida sebagai produk sampingan selama produksi urea.
Namun, penting untuk dicatat bahwa karbon diklorida adalah zat yang sangat berbahaya dan sintesisnya memerlukan kehati-hatian dan keahlian maksimal. Pekerja harus melakukan proses ini di lingkungan industri yang terkendali dengan baik dengan langkah-langkah keselamatan dan peralatan pelindung yang ketat untuk menghindari paparan gas beracun dan memastikan keselamatan mereka dan lingkungan.
Kegunaan fosgen
Karbonat diklorida memiliki berbagai aplikasi industri karena sifatnya yang unik, namun penting untuk dicatat bahwa penggunaannya harus ditangani dengan sangat hati-hati karena sifatnya yang beracun. Berikut beberapa kegunaannya:
- Bahan Antara Kimia: Karbonat diklorida membantu menghasilkan beberapa bahan kimia penting, termasuk isosianat, yang memainkan peran penting dalam pembuatan busa poliuretan, pelapis dan perekat.
- Produksi pestisida: Karbonat diklorida memfasilitasi sintesis pestisida dan herbisida tertentu, sehingga berkontribusi terhadap perlindungan tanaman dan pengendalian hama.
- Produksi polikarbonat: Karbon dioksida merupakan komponen penting dalam produksi plastik polikarbonat, yang digunakan dalam berbagai produk, mulai dari kacamata hingga botol air.
- Industri tekstil: Karbonat diklorida terlibat dalam produksi pewarna tertentu dan bahan kimia lain yang digunakan dalam industri tekstil.
- Produksi Busa: Karbon dioksida memainkan peran penting dalam pembuatan bahan busa, termasuk beberapa jenis busa yang digunakan dalam insulasi.
- Obat-obatan: Karbonat diklorida bertindak sebagai zat antara kimia dalam produksi obat-obatan tertentu.
- Penelitian laboratorium: Peneliti terkadang menggunakan karbon diklorida dalam percobaan laboratorium.
- Produksi karet sintetis: Karbon dioksida merupakan bagian integral dari produksi beberapa karet sintetis.
- Pemurnian air: Karbonat diklorida sebelumnya telah digunakan dalam jumlah kecil untuk pemurnian air, namun kini alternatif yang lebih aman lebih umum digunakan untuk tujuan ini.
Meskipun karbon diklorida memiliki kegunaan industri yang penting, toksisitasnya yang tinggi dan sifat berbahayanya memerlukan tindakan keselamatan yang ketat selama penanganan, penyimpanan, dan pengangkutan untuk mencegah kecelakaan dan menjamin kesejahteraan pekerja dan manusia. lingkungan.
Pertanyaan:
T: Apa pengaruh gas fosgen terhadap manusia?
J: Gas karbon diklorida dapat menyebabkan cedera pernafasan, menyebabkan kesulitan bernapas dan berpotensi menyebabkan edema paru yang fatal.
T: Apa itu fosgen?
J: Karbon dioksida adalah senyawa kimia yang sangat beracun yang digunakan dalam berbagai proses industri.
T: Apa itu gas fosgen?
J: Gas karbon diklorida adalah bentuk gas dari senyawa kimia, yang dikenal karena efeknya yang menyesakkan dan beracun pada sistem pernapasan.
T: Apa pengaruh fosgen terhadap tubuh?
J: Karbon dioksida dapat merusak paru-paru, menyebabkan penumpukan cairan dan gangguan pernapasan yang parah.
T: Seberapa sering Grignard bereaksi dengan fosgen?
A: Reagen Grignard hanya bereaksi satu kali dengan karbon diklorida, membentuk keton.
T: Organ manusia manakah yang diserang oleh gas klorin dan fosgen?
J: Gas klorin dan karbon diklorida terutama menyerang paru-paru.
T: Bagaimana gas fosgen membunuh Anda?
J: Gas karbon diklorida menyebabkan iritasi paru-paru yang parah, menyebabkan penumpukan cairan dan mati lemas.
T: Siapa yang menemukan gas fosgen?
A: Gas karbon dioksida ditemukan oleh ahli kimia Inggris John Davy pada tahun 1812.
T: Pengaruh gas karbon diklorida?
J: Gas karbon diklorida dapat menyebabkan kerusakan pernafasan, edema paru, dan dalam kasus yang parah, kematian.
T: Struktur Lewis karbon dioksida?
J: Struktur Lewis karbonat diklorida terdiri dari karbon yang terikat rangkap dengan oksigen dan ikatan tunggal dengan dua atom klor.
T: Gas karbon diklorida Perang Dunia I?
J: Karbon diklorida digunakan sebagai senjata kimia selama Perang Dunia I, menyebabkan dampak buruk pada tentara.
T: Kapan gas fosgen pertama kali digunakan?
A: Gas karbon diklorida pertama kali digunakan sebagai senjata kimia selama Perang Dunia I pada tahun 1915.
T: Dari mana asal fosgen?
J: Karbon dioksida biasanya dihasilkan dengan mereaksikan klorin dengan karbon monoksida atau senyawa yang mengandung karbon lainnya.
