Thionylchlorid ist eine chemische Verbindung, die in verschiedenen industriellen Anwendungen eingesetzt wird. Es reagiert mit Alkoholen und Carbonsäuren und erzeugt die entsprechenden Chloride bzw. Sulfurylchlorid.
| Name der IUPAC | Thionylchlorid |
| Molekularformel | SOCl₂ |
| CAS-Nummer | 7719-09-7 |
| Synonyme | Schwefeldichlorid, Schwefeloxychlorid, Thionyldichlorid |
| InChI | InChI=1S/Cl2OS/c1-4(2)3 |
Eigenschaften von Thionylchlorid
Thionylchlorid-Formel
Die Formel für Thionyldichlorid lautet SOCl₂ und steht für ein Schwefelatom, das an zwei Chloratome gebunden ist. Es handelt sich um eine chemische Verbindung, die in verschiedenen Branchen weit verbreitet ist.
Molmasse von Thionylchlorid
Thionyldichlorid hat eine Molmasse von etwa 118,97 Gramm pro Mol. Die Molmasse wird durch Addition der Atommassen seiner Bestandteile bestimmt.
Siedepunkt von Thionylchlorid
Thionyldichlorid hat einen Siedepunkt von etwa 79,6 Grad Celsius. Dies ist die Temperatur, bei der die flüssige Form von Thionyldichlorid in den gasförmigen Zustand übergeht.
Schmelzpunkt von Thionylchlorid
Der Schmelzpunkt von Thionyldichlorid liegt bei etwa -104,5 Grad Celsius. Dies ist die Temperatur, bei der die feste Form von Thionyldichlorid in den flüssigen Zustand übergeht.
Dichte von Thionylchlorid g/ml
Thionyldichlorid hat eine Dichte von etwa 1,64 Gramm pro Milliliter. Die Dichte ist das Maß für die Masse pro Volumeneinheit und ein wichtiges Merkmal eines Stoffes.
Molekulargewicht von Thionylchlorid
Das Molekulargewicht von Thionyldichlorid beträgt etwa 118,97 Gramm pro Mol. Sie wird durch Addition der Atomgewichte von Schwefel, Chlor und Sauerstoff berechnet.
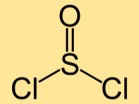
Struktur von Thionylchlorid
Die Struktur von Thionyldichlorid besteht aus einem Schwefelatom, das an zwei Chloratome gebunden ist. Die Schwefel- und Chloratome sind linear angeordnet und bilden ein gebogenes Molekül.
Löslichkeit von Thionylchlorid
Thionyldichlorid ist in Wasser schlecht löslich, löst sich jedoch leicht in organischen Lösungsmitteln wie Benzol, Toluol und Tetrachlorkohlenstoff. Seine Löslichkeit ist ein wichtiger Faktor bei seinen Anwendungen.
| Aussehen | Farblose bis hellgelbe Flüssigkeit |
| Spezifisches Gewicht | 1.638 g/ml |
| Farbe | Farblos |
| Geruch | Scharf, erstickend |
| Molmasse | 118,97 g/Mol |
| Dichte | 1.638 g/ml |
| Fusionspunkt | -104,5°C |
| Siedepunkt | 79,6°C |
| Blitzpunkt | Unzutreffend |
| Löslichkeit in Wasser | Reagiert heftig |
| Löslichkeit | Löslich in organischen Lösungsmitteln wie Benzol, Toluol und Tetrachlorkohlenstoff |
| Dampfdruck | 4,33 kPa bei 20°C |
| Wasserdampfdichte | 3,9 (Luft = 1) |
| pKa | -6.3 |
| pH-Wert | Unzutreffend |
Sicherheit und Gefahren von Thionylchlorid
Thionyldichlorid birgt mehrere Sicherheitsrisiken und sollte mit Vorsicht gehandhabt werden. Es ist stark ätzend und kann bei Kontakt mit Haut, Augen oder Schleimhäuten schwere Verätzungen verursachen. Das Einatmen der Dämpfe kann zu Reizungen und Atemwegsschäden führen. Die Verbindung reagiert heftig mit Wasser und setzt giftige Gase wie Chlorwasserstoff frei. Daher muss es fern von Feuchtigkeitsquellen gelagert und gehandhabt werden. Thionyldichlorid reagiert außerdem heftig mit Alkoholen und wasserhaltigen Verbindungen, was zu Brand- oder Explosionsgefahr führen kann. Ausreichende Belüftung, persönliche Schutzausrüstung und ordnungsgemäße Lagerungspraktiken sind für den sicheren Umgang mit Thionyldichlorid unerlässlich.
| Gefahrensymbole | Ätzend (C), Giftig (T), Umweltgefährlich (N) |
| Sicherheitsbeschreibung | – Von Feuchtigkeitsquellen und unverträglichen Substanzen fernhalten.<br>- In einem gut belüfteten Bereich verwenden und geeignete persönliche Schutzausrüstung tragen.<br>- Vorsichtig handhaben, um Kontakt mit Haut, Augen und Schleimhäuten zu vermeiden.<br> – In einem dicht verschlossenen Behälter an einem kühlen, trockenen Ort aufbewahren. |
| UN-Identifikationsnummern | UN-Nr. 1836 (Thionyldichlorid) |
| HS-Code | 2812.10.00 |
| Gefahrenklasse | 8 (Ätzende Stoffe) |
| Verpackungsgruppe | II (Mäßig gefährlich) |
| Toxizität | Sehr giftig beim Einatmen, Verschlucken und Hautabsorption.<br>- Kann schwere Verbrennungen und Reizungen der Atemwege verursachen.<br>- Kann langfristig schädliche Auswirkungen auf Wasserorganismen haben. |
Methoden zur Synthese von Thionylchlorid
Verschiedene Methoden ermöglichen die Synthese von Thionyldichlorid.
Ein üblicher Ansatz beinhaltet die Reaktion zwischen Schwefeltrioxid (SO₃) und Schwefeldichlorid (SCl₂) in Gegenwart eines Katalysators wie Aktivkohle oder Aluminiumchlorid . Die Reaktion findet bei hohen Temperaturen, meist etwa 300 bis 400 °C, statt und erzeugt dabei Thionyldichlorid.
Eine andere Methode beinhaltet die direkte Reaktion von Schwefeldioxid (SO₂) mit Phosphorpentachlorid (PCl₅) oder Phosphoroxychlorid (POCl₃). Diese Reaktion findet unter Rückfluss mit fortschreitender Zugabe der Reagenzien statt und führt zu Thionyldichlorid.
Die Reaktion von Schwefel mit Phosphortrichlorid (PCl₃) ergibt Thionyldichlorid. Bei diesem Prozess werden die Reaktanten erhitzt und die Bildung von Thionyldichlorid ermöglicht.
Eine andere Methode beinhaltet die Reaktion zwischen Phosphorpentasulfid (P₂S₅) und Phosphorpentachlorid (PCl₅) in Gegenwart eines Lewis-Säure-Katalysators wie Aluminiumchlorid. Die Reaktion findet bei hohen Temperaturen statt und führt zur Bildung von Thionyldichlorid.
Es ist wichtig zu beachten, dass diese Synthesemethoden aufgrund der Gefährlichkeit der beteiligten Reagenzien eine ordnungsgemäße Handhabung und Sicherheitsvorkehrungen erfordern. Die sichere und effiziente Synthese von Thionyldichlorid erfordert das Fachwissen erfahrener Chemiker und den Einsatz geeigneter Laborgeräte.
Verwendung von Thionylchlorid
Aufgrund seiner vielseitigen chemischen Eigenschaften findet Thionyldichlorid breite Anwendung in verschiedenen Branchen. Hier sind einige häufige Anwendungen von Thionyldichlorid:
- Umwandlung von Carbonsäuren: Thionyldichlorid wandelt Carbonsäuren in Acylchloride um und nutzt dabei größtenteils die Vilsmeier-Haack-Reaktion in der organischen Synthese.
- Alkoholchlorierung: Thionyldichlorid reagiert mit Alkoholen unter Bildung von Alkylchloriden und findet Anwendung bei der Herstellung chlorierter Verbindungen für Pharmazeutika und Agrochemikalien, bekannt als Darzens-Reaktion.
- Entwässerungsmittel: Thionyldichlorid wirkt als Entwässerungsmittel und erleichtert die Entfernung verschiedener Verbindungen aus Wasser. Es wird häufig bei der Synthese von Farbstoffen, Parfümen und pharmazeutischen Zwischenprodukten verwendet.
- Herstellung von Lithium-Ionen-Batterien: Hersteller verwenden Thionyldichlorid zur Herstellung von Lithium-Thionyldichlorid-Batterien, die eine hohe Energiedichte und eine lange Haltbarkeit aufweisen. Diese Batterien finden Anwendung in medizinischen Geräten, militärischer Ausrüstung und Fernsensoren.
- Polymerisationsreaktionen: Thionyldichlorid nimmt an Polymerisationsreaktionen teil und trägt zur Synthese verschiedener Polymere bei, darunter Polycarbonate und Polyanhydride.
- Phosphorverbindungen: Thionyldichlorid reagiert mit Phosphorverbindungen wie Phosphortrichlorid und erzeugt Phosphorylchloride. Chemiker nutzen diese Zwischenprodukte zur Synthese von Organophosphatverbindungen und Flammschutzmitteln.
- Chemisches Reagenz: Thionyldichlorid dient als vielseitiges Reagenz bei vielen chemischen Umwandlungen, einschließlich Veresterung, Halogenierung und nukleophilen Substitutionsreaktionen.
Fragen:
F: Womit kann man Thionylchlorid spülen?
A: Thionyldichlorid kann mit einem großen Überschuss an Alkohol oder einer verträglichen Base wie Methanol oder Natriumbicarbonatlösung gespült werden.
F: Was ist das Produkt von Valeriansäure mit Thionylchlorid?
A: Die Reaktion von Valeriansäure mit Thionyldichlorid erzeugt Valerilchlorid sowie Schwefeldioxidgas.
F: Kann man Thionylchlorid mit einer Carbonsäure hinzufügen?
A: Ja, Thionyldichlorid kann einer Carbonsäure zugesetzt werden, um sie durch die Vilsmeier-Haack-Reaktion in Acylchlorid umzuwandeln.
F: Welche der folgenden ist die richtige Lewis-Formel für Thionylchlorid (SOCl2)?
A: Die korrekte Lewis-Formel für Thionyldichlorid (SOCl2) wird durch S=O | dargestellt Cl – Cl.
F: Was treibt die Thionylchlorid-Reaktion an?
A: Die Thionyldichlorid-Reaktion wird durch die hohe Reaktivität von Thionylchlorid vorangetrieben, das bei verschiedenen chemischen Umwandlungen als Elektrophil fungiert.
F: Wie löscht man Thionylchlorid?
A: Thionyldichlorid kann durch Zugabe eines geeigneten Löschmittels wie eines primären oder sekundären Alkohols oder durch vorsichtige Hydrolyse mit Wasser gelöscht werden.
F: Was würde man erhalten, wenn man Amine mit Thionylchlorid mischt?
A: Das Mischen von Aminen mit Thionyldichlorid führt zur Bildung der entsprechenden Aminhydrochloridsalze.
F: Was ist Thionylchlorid?
A: Thionyldichlorid ist eine chemische Verbindung mit der Formel SOCl2, die üblicherweise als Reagenz in der organischen Synthese und als Dehydratisierungsmittel verwendet wird.
F: Was bewirkt ein Überschuss an Thionylchlorid?
A: Überschüssiges Thionyldichlorid kann heftige Reaktionen hervorrufen, die möglicherweise zur Bildung giftiger Gase oder zur Explosionsgefahr führen und sollte mit Vorsicht gehandhabt werden.
F: Wie neutralisiert man Thionylchlorid?
A: Thionyldichlorid kann durch vorsichtige Zugabe zu einem großen Überschuss einer geeigneten Base wie Natriumbicarbonat oder Natriumhydroxid neutralisiert werden, wobei entsprechende Sicherheitsvorkehrungen zu beachten sind.
