Tetrahydrofuran (THF) ist eine farblose organische Verbindung. Aufgrund seiner Fähigkeit, ein breites Spektrum an Substanzen aufzulösen, wird es häufig in verschiedenen Industriezweigen als Lösungsmittel verwendet.
| IUPAC-Name | Oxolan |
| Molekularformel | C4H8O |
| CAS-Nummer | 109-99-9 |
| Synonyme | THF, Oxacyclopentan, Butylenoxid, Diethylenoxid, Cyclotetramethylenoxid |
| InChI | InChI=1S/C4H8O/c1-2-4-5-3-1/h1-4H2 |
Eigenschaften von Tetrahydrofuran
Tetrahydrofuran-Formel
Tetrahydrofuran (THF) hat die chemische Formel C4H8O. Es ist ein zyklischer Ether mit einem fünfgliedrigen Ring, der vier Kohlenstoffatome und ein Sauerstoffatom enthält. THF hat einen niedrigen Siedepunkt und wird in verschiedenen Industrien häufig als Lösungsmittel verwendet.
Molmasse von Tetrahydrofuran
Die Molmasse von THF beträgt etwa 72,11 g/mol. Dieser Wert wird durch Addition der Atommassen der Atombestandteile in der Summenformel berechnet. Die relativ geringe Molmasse von THF trägt zu seinem niedrigen Siedepunkt und seiner geringen Flüchtigkeit bei und macht es zu einem wirksamen Lösungsmittel für eine Vielzahl organischer Verbindungen.
Siedepunkt von Tetrahydrofuran
Der Siedepunkt von THF beträgt 66 °C (151 °F) bei normalem Atmosphärendruck. Der niedrige Siedepunkt von THF macht es zu einem nützlichen Lösungsmittel für chemische Reaktionen, die hohe Temperaturen erfordern, wie z. B. Grignard-Reaktionen. Aufgrund des niedrigen Siedepunkts ist THF jedoch auch sehr flüchtig, sodass beim Umgang damit Vorsicht geboten ist.
Schmelzpunkt von Tetrahydrofuran
Der Schmelzpunkt von THF beträgt etwa –108,5 °C (–163,3 °F). THF ist bei Raumtemperatur flüssig, kann sich jedoch bei niedrigen Temperaturen verfestigen. Der niedrige Schmelzpunkt von THF macht es als kryogenes Lösungsmittel für Anwendungen bei niedrigen Temperaturen nützlich.
Dichte von Tetrahydrofuran g/ml
Die Dichte von THF beträgt etwa 0,889 g/ml bei 20 °C (68 °F). Dieser Wert ist im Vergleich zu anderen gängigen Lösungsmitteln relativ niedrig. Die geringe Dichte von THF macht es zu einem nützlichen Lösungsmittel für dichteempfindliche Reaktionen, da es die Gesamtdichte der Reaktionsmischung verringern kann.
Molekulargewicht von Tetrahydrofuran
Das Molekulargewicht von THF beträgt etwa 72,11 g/mol. Dieser Wert wird durch Addition der Atommassen der Atombestandteile in der Summenformel berechnet. Das relativ niedrige Molekulargewicht von THF trägt zu seinem niedrigen Siedepunkt und seiner Flüchtigkeit bei.
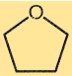
Struktur von Tetrahydrofuran
THF hat eine fünfgliedrige Ringstruktur mit vier Kohlenstoffatomen und einem Sauerstoffatom. Die Kohlenstoffatome sind in einer tetraedrischen Geometrie angeordnet, wobei jedes Kohlenstoffatom an zwei andere Kohlenstoffatome und ein Wasserstoffatom gebunden ist. Das Sauerstoffatom ist an ein Kohlenstoffatom und ein Wasserstoffatom gebunden.
Löslichkeit von Tetrahydrofuran
THF ist ein polares aprotisches Lösungsmittel, das eine Vielzahl organischer Verbindungen lösen kann. THF ist mit Wasser mischbar und wird häufig als Co-Lösungsmittel in verschiedenen chemischen Reaktionen verwendet. Allerdings ist THF möglicherweise mit einigen Materialien nicht kompatibel, daher ist es wichtig, die Kompatibilität vor der Verwendung zu prüfen.
| Aussehen | Farblose Flüssigkeit |
| Spezifische Dichte | 0,889 |
| Farbe | Farblos |
| Geruch | Geruch nach Äther |
| Molmasse | 72,11 g/Mol |
| Dichte | 0,889 g/ml |
| Fusionspunkt | −108,5 °C (−163,3 °F) |
| Siedepunkt | 66°C (151°F) |
| Blitzpunkt | −14 °C (7 °F) |
| Löslichkeit in Wasser | Mischbar |
| Löslichkeit | Löslich in Ethanol, Ether, Aceton, Benzol |
| Dampfdruck | 200 mmHg bei 20°C |
| Wasserdampfdichte | 2,5 (Luft = 1) |
| pKa | 25.3 |
| pH-Wert | Neutral (7) |
Sicherheit und Gefahren von Tetrahydrofuran
Tetrahydrofuran (THF) birgt mehrere Sicherheits- und Gesundheitsrisiken. THF ist leicht entflammbar und kann sich bei Raumtemperatur entzünden. Beim Erhitzen oder Verbrennen können außerdem giftige Dämpfe freigesetzt werden. Die Exposition gegenüber THF kann zu Haut- und Augenreizungen führen und eine längere Exposition kann zu Leber- und Nierenschäden führen. Es ist auch bekannt, dass THF Schwindel und Kopfschmerzen verursacht und wiederholtes Einatmen zu Atemproblemen führen kann. Beim Umgang mit THF ist Vorsicht geboten und es sollte Schutzausrüstung wie Handschuhe und Schutzbrille getragen werden. THF sollte an einem kühlen, gut belüfteten Ort, entfernt von Wärmequellen und inkompatiblen Materialien, gelagert werden.
| Gefahrensymbole | Entzündlich, giftig |
| Sicherheitsbeschreibung | Leicht entzündliche Flüssigkeit und Dampf. Verursacht schwere Augenreizung. Kann Schläfrigkeit oder Schwindelgefühl verursachen. Kann beim Verschlucken oder Einatmen gesundheitsschädlich sein. |
| UN-Identifikationsnummern | UN2056 |
| HS-Code | 29321100 |
| Gefahrenklasse | 3 (Brennbare Flüssigkeiten) |
| Verpackungsgruppe | II |
| Toxizität | LD50 (oral, Ratte) – 5.410 mg/kg |
Methoden zur Synthese von Tetrahydrofuran
Zur Synthese von Tetrahydrofuran (THF) können verschiedene Methoden eingesetzt werden.
Eine gängige Methode ist die katalytische Hydrierung von Furan. Dabei wird Furandampf in Gegenwart von Wasserstoffgas über einen Nickel- oder Palladiumkatalysator geleitet. Bei der resultierenden Reaktion entstehen THF und Wasser als Nebenprodukte.
Eine andere Methode beinhaltet die Reaktion von 1,4-Butandiol mit Schwefelsäure und die anschließende Destillation zur Herstellung von THF. Die Gefahren konzentrierter Schwefelsäure machen diese Methode weniger verbreitet.
Eine weitere Möglichkeit zur THF-Synthese ist die säurekatalysierte Dehydratisierung von 1,4-Butandiol. Bei dieser Methode wird 1,4-Butandiol mit einer starken Säure wie Schwefelsäure erhitzt, um Wasser zu entfernen und THF zu erzeugen.
Darüber hinaus kann THF durch katalytische Hydrogenolyse von Cellulose oder anderen aus Biomasse gewonnenen Zuckern gewonnen werden. Aufgrund des Potenzials erneuerbarer Quellen für die THF-Produktion ist diese Methode von wachsendem Interesse.
Jede Methode hat ihre Vor- und Nachteile, und die konkret gewählte Methode hängt von Faktoren wie Kosten, Verfügbarkeit der Rohstoffe und der gewünschten Reinheit des Endprodukts ab.
Verwendungsmöglichkeiten von Tetrahydrofuran
Tetrahydrofuran (THF) hat verschiedene Industrie- und Laboranwendungen, darunter:
- Lösungsmittel: Aufgrund seiner hohen Lösungsmittelkraft und seines niedrigen Siedepunkts wird es häufig als Lösungsmittel für verschiedene organische Verbindungen verwendet.
- Polymerisation: Wird als Co-Lösungsmittel bei der Polymerisation von Polystyrol und Polyvinylchlorid sowie bei der Herstellung von Polyurethanschäumen verwendet.
- Chemische Synthese: Wird als Reaktionslösungsmittel in der organischen chemischen Synthese verwendet, beispielsweise bei der Herstellung von Grignard-Reagenzien.
- Extraktion: Wird als Extraktionslösungsmittel für verschiedene Naturprodukte wie Alkaloide und Steroide verwendet.
- Klebstoffe: Werden als Bestandteil in Klebstoffformulierungen verwendet, wie sie beispielsweise in der Schuh- und Lederherstellung verwendet werden.
- Beschichtungen: Wird zur Herstellung von Beschichtungen und Lacken sowie zur Formulierung von Farben und Lacken verwendet.
- Analytische Chemie: Wird als mobiles Phasenlösungsmittel in Analysen mit Hochleistungsflüssigkeitschromatographie (HPLC) und Gaschromatographie (GC) verwendet.
Fragen:
F: Welches organische Produkt entsteht hauptsächlich, wenn Tetrahydrofuran mit überschüssigem HBr behandelt wird?
A: Wenn THF mit überschüssigem HBr behandelt wird, entsteht als organisches Hauptprodukt 3-Brom-1,4-dioxan.
F: Ist Tetrahydrofuran mit Wasser mischbar?
A: Ja, THF ist mit Wasser mischbar. Es weist eine hohe Löslichkeit in polaren Lösungsmitteln, insbesondere Wasser, auf.
F: Schadet Tetrahydrofuran dem Gummi?
A: Ja, THF kann Gummi beschädigen. Dies kann zum Quellen, Erweichen und Reißen von Gummimaterialien führen.
F: Ist Tetrahydrofuran polar oder unpolar?
A: THF ist ein polares Lösungsmittel. Aufgrund des in seiner Ringstruktur vorhandenen Sauerstoffatoms verfügt es über ein Dipolmoment, was es zu einem guten Lösungsmittel für polare Verbindungen macht.
F: Wird Tetrahydrofuran im Wasser explodieren?
A: Nein, THF explodiert nicht in Wasser. Allerdings kann es bei längerem Kontakt mit der Luft ein explosives Peroxid bilden. Um die Bildung von Peroxiden zu vermeiden, sind eine ordnungsgemäße Lagerung und Handhabung erforderlich.
F: Was ist das Sicherheitsdatenblatt von Tetrahydrofuran?
A: Das THF-Sicherheitsdatenblatt (Sicherheitsdatenblatt) enthält Informationen zu seinen physikalischen und chemischen Eigenschaften, Handhabungs- und Lagerungsanweisungen, Gesundheits- und Sicherheitsvorkehrungen sowie Notfallmaßnahmen. Bei der Arbeit mit THF ist es wichtig, die im Sicherheitsdatenblatt enthaltenen Informationen zu lesen und zu befolgen.
