Propansäure oder C3H6O2 ist eine farblose flüssige Carbonsäure mit stechendem Geruch. Es wird unter anderem bei der Herstellung von Arzneimitteln, Herbiziden und Lebensmittelkonservierungsmitteln eingesetzt.
| IUPAC-Name | Propansäure |
| Molekularformel | C3H6O2 |
| CAS-Nummer | 79-09-4 |
| Synonyme | Propionsäure, Methylessigsäure, Ethylameisensäure, Propanylameisensäure, Propionsäurelösung usw. |
| InChI | InChI=1S/C3H6O2/c1-2-3(4)5/h2H2.1H3,(H.4.5) |
Struktur von Propansäure
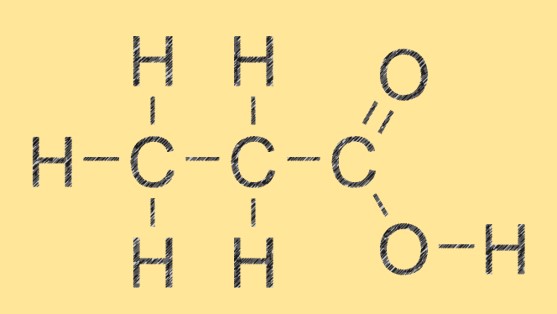
Propansäure hat eine einfache lineare Struktur bestehend aus drei Kohlenstoffatomen, sechs Wasserstoffatomen und zwei Sauerstoffatomen. Die Carbonsäuregruppe (-COOH) ist an das zweite Kohlenstoffatom des Moleküls gebunden. Diese Struktur ermöglicht es Propansäure, starke Wasserstoffbrückenbindungen mit anderen Propansäuremolekülen und anderen Verbindungen zu bilden, die Wasserstoffbrückenbindungsakzeptoren oder -donoren aufweisen.
Siedepunkt von Propansäure
Der Siedepunkt von Propansäure liegt bei 141,1°C. Dieser Wert wird durch die in der Verbindung vorhandenen intermolekularen Kräfte beeinflusst. Propansäure hat im Vergleich zu anderen einfachen Carbonsäuren aufgrund ihrer Fähigkeit, starke Wasserstoffbrückenbindungen zu bilden, einen relativ hohen Siedepunkt. Diese Eigenschaft macht Propansäure zu einem nützlichen Lösungsmittel in der organischen Chemie.
Propansäure-Formel
Die chemische Formel für Propansäure lautet C3H6O2. Diese Formel gibt die genaue Anzahl und Art der Atome in einem einzelnen Propansäuremolekül an. Die Formel kann zur Berechnung von Molmasse, Molekulargewicht und stöchiometrischen Verhältnissen bei chemischen Reaktionen mit Propansäure verwendet werden.
Molmasse von Propionsäure
Propionsäure hat eine Molmasse von 74,08 g/mol. Es handelt sich um eine einfache organische Carbonsäure mit drei Kohlenstoffatomen, sechs Wasserstoffatomen und zwei Sauerstoffatomen. Die Molmasse ist ein wichtiger Parameter in der Chemie, da sie zur Bestimmung der Stoffmenge in einer bestimmten Probe verwendet wird. Es wird auch in stöchiometrischen Berechnungen verwendet, um die Menge eines Reaktanten oder Produkts in einer chemischen Reaktion zu bestimmen.
Schmelzpunkt von Propionsäure
Propionsäure hat einen Schmelzpunkt von -20,8 °C. Dieser niedrige Schmelzpunkt ist das Ergebnis der schwachen intermolekularen Kräfte in der Verbindung. Propionsäure ist bei Raumtemperatur flüssig und kann sich bei niedrigen Temperaturen leicht verfestigen.
Dichte von Propionsäure g/ml
Propionsäure hat bei Raumtemperatur eine Dichte von 0,99 g/ml. Diese Eigenschaft wird durch das Molekulargewicht und die Packungsdichte der Moleküle der Verbindung beeinflusst. Aufgrund ihrer Dichte ist Propionsäure weniger dicht als Wasser und kann daher auf der Wasseroberfläche schwimmen.
Molekulargewicht von Propionsäure
Das Molekulargewicht von Propionsäure beträgt 74,08 g/mol. Dieser Wert wird durch Addition der Atomgewichte der Atome, aus denen das Molekül besteht, berechnet. Das Molekulargewicht von Propionsäure wird verwendet, um die Molmasse und die Anzahl der Mol der Verbindung in einer bestimmten Probe zu bestimmen.
| Aussehen | Farblose Flüssigkeit |
| Spezifisches Gewicht | 0,99 g/ml |
| Farbe | Farblos |
| Geruch | Acre |
| Molmasse | 74,08 g/Mol |
| Dichte | 0,99 g/ml |
| Fusionspunkt | -20,8°C |
| Siedepunkt | 141,1°C |
| Blitzpunkt | 60°C |
| Löslichkeit in Wasser | Mischbar |
| Löslichkeit | Löslich in Ethanol, Ether, Aceton |
| Dampfdruck | 1,5 mmHg bei 25°C |
| Wasserdampfdichte | 2,5 (gegen Luft) |
| pKa | 4,87 |
| pH-Wert | 2,8 (1M-Lösung) |
Hinweis: Die in der Tabelle angegebenen Werte sind Näherungswerte und können je nach Datenquelle variieren.
Propansäure Sicherheit und Gefahren
Unsachgemäßer Umgang mit Propansäure kann Sicherheits- und Gesundheitsrisiken bergen. Dieser Stoff ist ätzend und kann beim Einatmen schwere Haut- und Augenreizungen sowie Atemwegserkrankungen verursachen. Darüber hinaus ist Propansäure brennbar und kann mit Luft explosionsfähige Gemische bilden. Um die Sicherheit zu gewährleisten, lagern Sie es an einem kühlen, trockenen und gut belüfteten Ort, entfernt von Wärmequellen, Funken oder Flammen. Tragen Sie beim Umgang mit diesem Stoff Schutzausrüstung wie Handschuhe, Schutzbrillen und Atemschutzmasken, um Haut- und Augenkontakt sowie das Einatmen von Dämpfen zu vermeiden. Bei Verschlucken oder Kontakt mit Haut und Augen sofort einen Arzt aufsuchen.
| Gefahrensymbole | Ätzend (C) |
| Sicherheitsbeschreibung | S26-S36/37/39-S45 |
| AN-Kennungen | Ein 1848 |
| HS-Code | 2915.90.10 |
| Gefahrenklasse | 8 (Korrosives Material) |
| Verpackungsgruppe | III |
| Toxizität | LD50 (oral, Ratte) = 1,26 g/kg |
Methoden zur Propansäuresynthese
Propionsäure kann auf verschiedene Weise synthetisiert werden. Eine gängige Methode ist die Propylenoxidation, bei der Propylen mit Luft in Gegenwart eines Katalysators, meist einem Metalloxid, zu Acrolein reagiert. Acrolein wird dann zu Acrylsäure oxidiert, die dann durch eine Decarboxylierungsreaktion in Propionsäure umgewandelt wird.
Eine andere Methode beinhaltet die Ethylencarboxylierung, bei der Ethylen mit Kohlendioxid und Wasser in Gegenwart eines Katalysators, normalerweise eines Metallsalzes oder eines Palladiumkomplexes, zu Ethylen umgesetzt wird. Acetaldehyd. Acetaldehyd wird dann zu Essigsäure oxidiert, die dann durch eine Decarboxylierungsreaktion in Propansäure umgewandelt wird.
Eine dritte Methode ist die Hydrolyse von Ethylcyanid, bei der Ethylcyanid mit Wasser in Gegenwart einer starken Säure oder Base unter Bildung von Propionsäure umgesetzt wird.
Eine vierte Methode ist die Kohlenhydratfermentation, bei der Bakterien wie Propionibacterium freudenreichii zur Umwandlung von Zucker in Propionsäure eingesetzt werden. Dieses Verfahren wird in der Lebensmittelindustrie häufig zur Herstellung von Propionsäure zur Verwendung als Konservierungsmittel eingesetzt.
Insgesamt bieten diese Methoden je nach gewünschter Reinheit, Ausbeute und Umweltbelastung verschiedene Optionen für die Synthese von Propionsäure.
Verwendung von Propansäure
- Die Lebensmittelindustrie verwendet Propansäure als Konservierungsmittel, um das Wachstum von Bakterien und Schimmel in Backwaren, Milchprodukten und Tiernahrung zu verhindern.
- Propionsäure dient als chemisches Zwischenprodukt bei der Herstellung anderer Chemikalien, darunter Ester, die bei der Herstellung von Parfümen, Aromen und Kunststoffen verwendet werden.
- Propionsäureanhydrid, hergestellt aus Propansäure, wird als Lösungsmittel und Reagenz in der organischen Synthese verwendet.
- Die Pharmaindustrie verwendet Propansäure als Rohstoff für die Synthese von Arzneimitteln wie Ibuprofen, Naproxen und Fenoprofen.
- Propionsäure wird auch bei der Herstellung von Herbiziden und Insektiziden verwendet.
- Aus Propionsäure wird Celluloseacetatpropionat hergestellt, ein Überzugsmittel für Arzneimittel und Bestandteil von Farben, Lacken und Beschichtungen.
Insgesamt verfügt Propionsäure aufgrund ihrer antibakteriellen und konservierenden Eigenschaften sowie ihrer Vielseitigkeit als chemisches Zwischenprodukt über ein breites Anwendungsspektrum.
Fragen:
Welche Verbindung hat voraussichtlich ähnliche chemische Eigenschaften wie Propansäure (ch3ch2cooh)?
Propionsäure (CH3CH2COOH) sagt voraus, dass Verbindungen mit einer ähnlichen chemischen Struktur vergleichbare chemische Eigenschaften haben. Butansäure (CH3CH2CH2COOH) ist eine Verbindung mit einer Struktur ähnlich der Propionsäure, mit einer zusätzlichen Methylengruppe in der Kohlenstoffkette. Es wird erwartet, dass diese zusätzliche Methylengruppe die Polarität und den Säuregehalt des Moleküls beeinflusst, aber beide Verbindungen haben analoge Eigenschaften, z. B. dass sie schwache organische Säuren sind.
Die Lebensmittelindustrie verwendet Buttersäure als Konservierungsmittel und dient ähnlich wie Propansäure als chemisches Zwischenprodukt bei der Herstellung von Estern, Lösungsmitteln und Arzneimitteln. Butansäure kann in einigen Anwendungen auch Propionsäure ersetzen, da sie einen ähnlichen pKa-Wert hat.
Ist Propansäure eine starke Säure?
Propansäure ist eine schwache Säure. Sein pKa-Wert beträgt ungefähr 4,87, was darauf hinweist, dass es bei einer chemischen Reaktion nicht ohne weiteres ein Proton an eine Base abgibt.
Im Vergleich dazu haben starke Säuren wie Salzsäure (HCl) und Schwefelsäure (H2SO4) viel niedrigere pKa-Werte und geben bei chemischen Reaktionen leicht Protonen ab. Obwohl es sich um eine schwache Säure handelt, ist Propionsäure in einigen Anwendungen dennoch nützlich. Aufgrund seines geringen Säuregehalts eignet es sich als Konservierungsmittel in der Lebensmittelindustrie, da es das Wachstum von Bakterien und Pilzen wirksam hemmt, ohne den Geschmack oder Geruch von Lebensmitteln zu beeinträchtigen.
