Phosphortribromid (PBr3) ist eine Verbindung, die aus einem Phosphoratom und drei Bromatomen besteht. Es wird als Reagens bei verschiedenen chemischen Reaktionen verwendet, insbesondere bei der Synthese organischer Verbindungen.
| IUPAC-Name | Phosphortribromid |
| Molekularformel | PBr3 |
| CAS-Nummer | 7789-60-8 |
| Synonyme | Phosphor(III)-bromid, Bromphosphorbromid, Tribromophosphin |
| InChI | InChI=1S/Br3P/c1-4(2)3 |
Eigenschaften von Phosphortribromid
Phosphortribromid-Formel
Die Formel für Phosphor(III)-bromid lautet PBr3. Es besteht aus einem Phosphoratom und drei Bromatomen. Diese Verbindung entsteht, wenn Phosphor mit Brom reagiert. Die Formel gibt die Zusammensetzung der Verbindung genau wieder.
Molmasse von Phosphortribromid
Die Molmasse von Phosphor(III)-bromid kann durch Addition der Atommassen seiner Bestandteile berechnet werden. Phosphor hat eine Atommasse von etwa 31,0 Gramm pro Mol, während Brom eine Atommasse von etwa 79,9 Gramm pro Mol hat. Addiert man die dreifache Atommasse von Brom zur Atommasse von Phosphor, erhält man die Molmasse von Phosphor(III)-bromid, die etwa 270,7 Gramm pro Mol beträgt.
Siedepunkt von Phosphortribromid
Phosphor(III)-bromid hat einen Siedepunkt von etwa 173 Grad Celsius. Das bedeutet, dass die Verbindung bei Temperaturen oberhalb dieses Punktes einen Phasenwechsel von einer Flüssigkeit zu einem Gas durchläuft. Der Siedepunkt ist ein wichtiges Merkmal, das dabei hilft, die Bedingungen zu bestimmen, unter denen die Verbindung verwendet oder gereinigt werden kann.
Schmelzpunkt von Phosphortribromid
Der Schmelzpunkt von Phosphor(III)-bromid liegt bei etwa -41 Grad Celsius. Diese Temperatur gibt den Punkt an, an dem die Verbindung vom festen in den flüssigen Zustand übergeht. Die Kenntnis des Schmelzpunkts ist für die Handhabung und Manipulation der Verbindung in verschiedenen chemischen Prozessen von entscheidender Bedeutung.
Dichte von Phosphortribromid g/ml
Die Dichte von Phosphor(III)-bromid beträgt etwa 2,85 Gramm pro Milliliter (g/ml). Die Dichte misst die Masse einer Substanz pro Volumeneinheit. Aufgrund seiner relativ hohen Dichte ist Phosphor(III)-bromid dichter als viele andere gängige Flüssigkeiten, was darauf hindeutet, dass es im Verhältnis zu seinem Volumen relativ schwer ist.
Molekulargewicht von Phosphortribromid
Das Molekulargewicht von Phosphor(III)-bromid beträgt etwa 270,7 Gramm pro Mol. Dieser Wert wird durch Addition der Atommassen aller Atome in der Verbindung berechnet, basierend auf der Summenformel PBr3. Das Molekulargewicht ist für verschiedene Berechnungen nützlich, einschließlich der Bestimmung der in einer bestimmten Masse vorhandenen Substanzmenge.
Struktur von Phosphortribromid
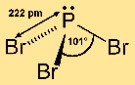
Phosphor(III)-bromid hat eine pyramidenförmige Molekülstruktur. Es besteht aus einem zentralen Phosphoratom, an das drei Bromatome gebunden sind. Diese Anordnung verleiht dem Molekül die Form einer trigonalen Pyramide, mit dem Phosphoratom an der Spitze und den Bromatomen an der Basis. Diese Struktur ist wichtig für das Verständnis der Reaktivität und des Verhaltens der Verbindung bei chemischen Reaktionen.
Löslichkeit von Phosphortribromid
Phosphor(III)-bromid ist in Wasser schlecht löslich. Es reagiert mit Wasser unter Bildung von Bromwasserstoffsäure und Phosphorsäure. Es ist jedoch in organischen Lösungsmitteln wie Benzol und Tetrachlorkohlenstoff löslich. Die Löslichkeit bestimmt das Ausmaß, in dem sich eine Verbindung in einem bestimmten Lösungsmittel lösen kann, was Auswirkungen auf ihre Anwendungen und Handhabung in verschiedenen Prozessen hat.
| Aussehen | Farblose Flüssigkeit |
| Spezifisches Gewicht | 2,85 g/ml |
| Farbe | Farblos |
| Geruch | Acre |
| Molmasse | 270,7 g/Mol |
| Dichte | 2,85 g/ml |
| Fusionspunkt | -41°C |
| Siedepunkt | 173°C |
| Blitzpunkt | Nicht verfügbar |
| Löslichkeit in Wasser | Reagiert |
| Löslichkeit | Löslich in organischen Lösungsmitteln wie Benzol und Tetrachlorkohlenstoff |
| Dampfdruck | Nicht verfügbar |
| Wasserdampfdichte | Nicht verfügbar |
| pKa | Nicht verfügbar |
| pH-Wert | Nicht verfügbar |
Sicherheit und Gefahren von Phosphortribromid
Phosphor(III)-bromid birgt einige Sicherheitsrisiken und sollte mit Vorsicht gehandhabt werden. Es ist ätzend und kann bei Kontakt mit Haut, Augen oder Atemwegen schwere Verbrennungen verursachen. Das Einatmen oder direkte Verschlucken dieser Verbindung kann zu Reizungen der Atemwege und des Magen-Darm-Trakts führen. Es reagiert heftig mit Wasser, setzt giftige Dämpfe frei und erzeugt Hitze. Bei der Arbeit mit Phosphor(III)-bromid sollte für ausreichende Belüftung und persönliche Schutzausrüstung wie Handschuhe und Schutzbrillen gesorgt werden. Darüber hinaus sollte es fern von inkompatiblen Substanzen gelagert werden, um mögliche Reaktionen zu vermeiden. Insgesamt sind die strikte Einhaltung der Sicherheitsprotokolle und die Kenntnis der mit dieser Verbindung verbundenen Gefahren für eine sichere Handhabung unerlässlich.
| Gefahrensymbole | Ätzend |
| Sicherheitsbeschreibung | Mit Anzahlung umgehen. Kontakt mit Haut, Augen und Atemwegen vermeiden. Für ausreichende Belüftung und persönliche Schutzausrüstung sorgen. Getrennt von unverträglichen Substanzen lagern. |
| UN-Identifikationsnummern | UN1805 |
| HS-Code | 2812.90.90 |
| Gefahrenklasse | 8 (ätzend) |
| Verpackungsgruppe | II |
| Toxizität | Giftig beim Einatmen und Verschlucken. Kann schwere Verbrennungen und Reizungen verursachen. |
Methoden zur Synthese von Phosphortribromid
Bei einer gängigen Methode zur Synthese von Phosphor(III)-bromid werden im Reaktionsgefäß elementarer Phosphor und Brom direkt kombiniert, üblicherweise unter kontrollierten Bedingungen. Die Reaktion verläuft unter der Übertragung von Bromatomen auf Phosphoratome, was zur Bildung von Phosphor(III)bromid führt.
Eine andere Methode beinhaltet die Reaktion zwischen Phosphortrichlorid (PCl3) und Bromwasserstoff (HBr) . Bei diesem Ansatz reagiert Phosphortrichlorid zunächst mit Bromwasserstoffgas, wobei als Nebenprodukte Phosphor(III)bromid und Chlorwasserstoffgas entstehen. Diese Methode bietet einen alternativen Weg zur Gewinnung von Phosphor(III)-bromid.
Bei der „Rot-Phosphor-Methode“ wird roter Phosphor mit Brom oder Bromwasserstoffsäure kombiniert und die Reaktion unter kontrollierten Bedingungen durchgeführt. Roter Phosphor dient als Phosphorquelle und reagiert mit Brom oder Bromwasserstoffsäure unter Bildung von Phosphor(III)-bromid.
Diese Synthesemethoden eröffnen Möglichkeiten für die Herstellung von Phosphor(III)-bromid, jede mit ihren eigenen Vorteilen und Überlegungen. Die Wahl der Methode hängt von Faktoren wie der Verfügbarkeit der Reagenzien, der gewünschten Ausbeute und den spezifischen Reaktionsbedingungen ab. Es ist wichtig, diese Synthesen in einem gut ausgestatteten Labor durchzuführen und dabei Sicherheitsprotokolle und Verfahren für den Umgang mit den beteiligten Chemikalien einzuhalten.
Verwendung von Phosphortribromid
Phosphor(III)-bromid findet aufgrund seiner Reaktivität und einzigartigen Eigenschaften vielfältige Anwendungen. Hier sind einige seiner Verwendungsmöglichkeiten:
- Organische Synthese: Chemiker verwenden Phosphor(III)-bromid häufig als Reagens in der organischen Synthese, um Alkohole in Alkylbromide umzuwandeln, ein wichtiger Schritt bei der Synthese vieler organischer Verbindungen.
- Pharmazeutische Industrie: Die Herstellung von Arzneimitteln ist in hohem Maße auf Phosphor(III)-bromid angewiesen, um verschiedene Arzneimittelzwischenprodukte und pharmazeutische Wirkstoffe (API) zu synthetisieren.
- Flammschutzmittel: Hersteller verwenden Phosphor(III)-bromid bei der Herstellung von Flammschutzmitteln und verbessern so die Feuerbeständigkeit bestimmter Polymere für den Einsatz in Branchen wie Elektronik und Textilien.
- Chemische Herstellung: Phosphor(III)bromid dient als wertvolles Zwischenprodukt bei der Herstellung anderer Chemikalien, darunter Phosphorverbindungen wie Phosphorsäurederivate, Phosphonate und Phosphate.
- Herbizide und Pestizide: Bei der Synthese spezifischer Wirkstoffe für Herbizide und Pestizide wird Phosphor(III)-bromid zur wirksamen Bekämpfung von Unkräutern, Schädlingen und Krankheiten in der Landwirtschaft eingesetzt.
- Laborforschung: Im Labor verwenden Forscher häufig Phosphor(III)-bromid als Reagenz in verschiedenen Experimenten und Reaktionen, insbesondere solchen, die Bromierung und Manipulation organischer Verbindungen beinhalten.
- Chemische Analyse: Phosphor(III)-bromid findet Anwendung in chemischen Analysetechniken und ermöglicht die Bestimmung des Vorhandenseins spezifischer funktioneller Gruppen in organischen Verbindungen durch Bromsubstitutionsreaktionen.
Diese vielfältigen Einsatzmöglichkeiten verdeutlichen die Bedeutung von Phosphor(III)-bromid in der organischen Synthese, bei Pharmazeutika, Flammschutzmitteln, in der chemischen Herstellung, in der Landwirtschaft, in der Laborforschung und in der chemischen Analyse. Seine Reaktivität und Vielseitigkeit machen es zu einer wertvollen Verbindung in verschiedenen Branchen und wissenschaftlichen Disziplinen.
Fragen:
F: Warum wird AlBr3 Aluminiumbromid genannt, während PBr3 Phosphortribromid ist?
A: Die Namenskonvention für Verbindungen mit Metallen verwendet im Allgemeinen den Elementnamen des Metalls, gefolgt vom Namen des Nichtmetalls, während im Fall von PBr3 Phosphor angegeben wird, um das Vorhandensein eines zentralen Phosphoratoms anzuzeigen.
F: Welches Wort oder welche Zwei-Wort-Phrase beschreibt die Form von Phosphortribromid am besten?
A: Die Form von Phosphor(III)-bromid lässt sich am besten als trigonal-pyramidal beschreiben.
F: Wie viele Valenzelektronen gibt es im Molekül von Phosphortribromid, PBr3?
A: Phosphor(III)bromid (PBr3) hat 26 Valenzelektronen.
F: Ist Phosphortribromid ionisch oder kovalent?
A: Phosphor(III)bromid (PBr3) ist eine kovalente Verbindung.
F: Wie lautet die chemische Formel von Phosphortribromid?
A: Die chemische Formel für Phosphor(III)bromid lautet PBr3.
F: Lewis-Struktur für Phosphortribromid, PBr3?
A: Die Lewis-Struktur von PBr3 zeigt Phosphor als Zentralatom, umgeben von drei gebundenen Bromatomen, die jeweils durch eine Einfachbindung verbunden sind.
F: Ist PBr3 eine Inversion?
A: Nein, Phosphor(III)bromid (PBr3) zeigt keine Inversion.
F: Ist PBr3 ein Elektrophil?
A: Ja, PBr3 kann bei bestimmten Reaktionen als Elektrophil wirken und dort Elektronen aufnehmen.
F: Wie ist die Molekülgeometrie von PBr3?
A: Die Molekülgeometrie von PBr3 ist trigonal-pyramidal.
F: Ist PBr3 polar oder unpolar?
A: PBr3 ist aufgrund der ungleichmäßigen Verteilung der Elektronendichte, die durch das Vorhandensein polarer P-Br-Bindungen verursacht wird, ein polares Molekül.
F: Wie viele Mol PBr3 enthalten 3,68 × 10^25 Bromatome?
A: Um die Anzahl der Mol zu bestimmen, benötigen wir die Molmasse von PBr3, dann dividieren wir die angegebene Anzahl an Bromatomen durch die Avogadro-Zahl.
F: Wie lautet der korrekte Name für PBr3?
A: Der korrekte Name für PBr3 ist Phosphor(III)bromid.
F: Ist PBr3 polar?
A: Ja, PBr3 ist aufgrund der Anwesenheit polarer Bindungen und der ungleichmäßigen Elektronendichteverteilung ein polares Molekül.
