Phosgen ist ein giftiges Gas, das in industriellen Prozessen und in der Kriegsführung eingesetzt wird. Das Einatmen stellt ein ernstes Gesundheitsrisiko dar, verursacht Atemwegsschäden und kann tödlich sein.
| IUPAC-Name | Carbonyldichlorid |
| Molekularformel | COCl2 |
| CAS-Nummer | 75-44-5 |
| Synonyme | Kohlendichlorid, Phosgengas, Carbonylchlorid |
| InChI | InChI=1S/CCl2O/c2-1(3)4 |
Eigenschaften von Phosgen
Phosgen-Formel
Die chemische Formel für Phosgen oder Kohlenstoffdichlorid lautet COCl2. Es besteht aus einem Kohlenstoffatom (C), einem Sauerstoffatom (O) und zwei Chloratomen (Cl). Diese molekulare Zusammensetzung ist wichtig für das Verständnis seiner Eigenschaften und Reaktionen.
Phosgen-Molmasse
Die Molmasse von Kohlenstoffdichlorid beträgt etwa 98,92 g/mol. Sie wird durch Addition der Atommassen seiner Bestandteile berechnet, nämlich Kohlenstoff (12,01 g/mol), Sauerstoff (16,00 g/mol) und Chlor (jeweils 35,45 g/mol).
Siedepunkt von Phosgen
Kohlendichlorid hat einen relativ niedrigen Siedepunkt von etwa -23,3 °C (-9,94 °F). Bei dieser Temperatur geht es vom flüssigen in den gasförmigen Zustand über, was für seinen Einsatz in verschiedenen industriellen Prozessen entscheidend ist.
Phosgen-Schmelzpunkt
Der Schmelzpunkt von Kohlendioxid ist recht niedrig und liegt bei etwa -118,3 °C (-180,94 °F). Bei dieser Temperatur wird die feste Form von Kohlenstoffdichlorid flüssig. Das Verständnis dieser Eigenschaft ist für den sicheren Umgang mit Kohlendioxid wichtig.
Phosgendichte g/ml
Kohlendichlorid hat bei Raumtemperatur (25 °C oder 77 °F) eine Dichte von etwa 1,432 g/ml. Diese Eigenschaft ist entscheidend für sein Verhalten und seine Wechselwirkungen mit anderen Substanzen.
Phosgen-Molekulargewicht
Das Molekulargewicht von Kohlenstoffdichlorid beträgt 98,92 g/mol. Dieser Wert ist für verschiedene Berechnungen in der Chemie von entscheidender Bedeutung, einschließlich der Stöchiometrie und der Bestimmung der Menge an Kohlendioxid, die für Reaktionen benötigt wird.
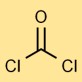
Struktur von Phosgen
Kohlendichlorid hat eine lineare Molekülstruktur, bei der das Kohlenstoffatom doppelt an das Sauerstoffatom und einfach an jedes Chloratom gebunden ist. Diese Anordnung beeinflusst die Reaktionsfähigkeit und Stabilität.
Löslichkeit von Phosgen
Kohlendichlorid ist in Wasser schlecht löslich, nur eine geringe Menge Gas löst sich in der Flüssigkeit. Allerdings kann es mit Wasser unter Bildung von Salzsäure und Kohlendioxid reagieren, was es in wässrigen Umgebungen gefährlich macht.
Das Verständnis dieser Eigenschaften von Kohlendichlorid ist für die sichere Handhabung und Verwendung der Chemikalie in industriellen Anwendungen und anderen Umgebungen von entscheidender Bedeutung. Beim Umgang mit dieser giftigen und reaktiven Verbindung sollten stets geeignete Vorsichtsmaßnahmen getroffen werden, um Unfälle und Gesundheitsrisiken zu vermeiden.
| Aussehen | Farbloses Gas |
| Spezifisches Gewicht | 3.428 (Gas) |
| Farbe | N / A |
| Geruch | Erstickend, stechend |
| Molmasse | 98,92 g/Mol |
| Dichte | 1.432 g/ml (flüssig) |
| Fusionspunkt | -118,3°C (-180,94°F) |
| Siedepunkt | -23,3°C (-9,94°F) |
| Blitzpunkt | N / A |
| Löslichkeit in Wasser | Reagiert mit Wasser |
| Löslichkeit | Reagiert mit Wasser unter Bildung von Salzsäure und Kohlendioxid |
| Dampfdruck | 736 mmHg (25 °C) |
| Wasserdampfdichte | 2,98 (Luft = 1) |
| pKa | N / A |
| pH-Wert | N / A |
Diese physikalisch-chemischen Eigenschaften liefern wesentliche Informationen über Kohlendioxid und erleichtern dessen sichere Handhabung und das Verständnis seines Verhaltens in verschiedenen Umgebungen.
Sicherheit und Gefahren von Phosgen
Kohlendichlorid birgt aufgrund seiner toxischen und reaktiven Natur erhebliche Sicherheitsrisiken. Tragen Sie beim Umgang mit Kohlendioxid geeignete persönliche Schutzausrüstung (PSA), einschließlich Atemschutz, Handschuhe und Augenschutz. Sorgen Sie für ausreichende Belüftung in den Arbeitsbereichen, um eine Exposition durch Einatmen zu vermeiden. Vermeiden Sie den Kontakt mit Haut und Augen, da dies zu schweren Reizungen und Verbrennungen führen kann. Kohlendioxidgas hat keinen Geruch und ist daher schwer zu erkennen. Daher sind Überwachungsgeräte von entscheidender Bedeutung. Bei Exposition sofort einen Arzt aufsuchen. Lagern und transportieren Sie Kohlendioxid sicher und gemäß den Vorschriften und Best Practices. Um Unfälle zu verhindern und die menschliche Gesundheit und die Umwelt zu schützen, ist es wichtig, die Gefahren zu verstehen.
| Gefahrensymbole | Totenkopf |
| Sicherheitsbeschreibung | Hochgiftiges Gas. Mit äußerster Vorsicht umgehen. Verwenden Sie geeignete PSA. Einatmen und Hautkontakt vermeiden. |
| UN-Identifikationsnummern | UN1076 |
| HS-Code | 2812.10.0000 |
| Gefahrenklasse | 2.3 (Giftiges Gas) |
| Verpackungsgruppe | ICH |
| Toxizität | Phosgen ist hochgiftig und kann beim Einatmen oder Hautkontakt tödlich sein. Setzen Sie strenge Sicherheitsmaßnahmen ein. |
Das Verständnis der Risiko- und Sicherheitsaspekte von Kohlendioxid ist für den sicheren Umgang und die Unfallverhütung von entscheidender Bedeutung. Es ist hochgiftig und birgt erhebliche Gesundheitsrisiken, weshalb geeignete Sicherheitsverfahren und Vorsichtsmaßnahmen unerlässlich sind.
Methoden der Phosgensynthese
Mehrere Methoden ermöglichen die Synthese von Kohlenstoffdichlorid.
Ein gängiger Ansatz ist der „Deacon-Prozess“, bei dem Chlorgas bei erhöhten Temperaturen in Gegenwart eines geeigneten Katalysators wie Kupfer(II)-chlorid mit Kohlenmonoxid reagiert. Eine andere Methode beinhaltet die „direkte Chlorierung“ von Kohlenmonoxid mit Chlorgas, erleichtert durch Eisen oder andere Metallchloride als Katalysatoren.
Die Herstellung von Kohlendichlorid umfasst die „oxidative Carbonylierung“ von Methylenchlorid oder Methylchlorid unter Verwendung von Sauerstoff und einem Metallkatalysator wie Kupferchlorid. Eine weitere Methode zur Synthese von Kohlendichlorid ist die „Harnstoffroute“, bei der bei der Harnstoffproduktion Kohlendichlorid als Nebenprodukt entsteht.
Es ist jedoch unbedingt zu beachten, dass Kohlendioxid ein sehr gefährlicher Stoff ist und seine Synthese höchste Sorgfalt und Fachwissen erfordert. Die Arbeiter müssen diese Prozesse in gut kontrollierten Industrieumgebungen mit strengen Sicherheitsmaßnahmen und Schutzausrüstung durchführen, um eine Exposition gegenüber giftigen Gasen zu vermeiden und ihre Sicherheit und die der Umwelt zu gewährleisten.
Verwendung von Phosgen
Kohlendichlorid findet aufgrund seiner einzigartigen Eigenschaften verschiedene industrielle Anwendungen, es ist jedoch wichtig zu beachten, dass seine Verwendung aufgrund seiner toxischen Natur mit äußerster Vorsicht gehandhabt werden sollte. Hier sind einige seiner Verwendungsmöglichkeiten:
- Chemische Zwischenprodukte: Kohlendichlorid hilft bei der Produktion mehrerer wichtiger Chemikalien, darunter Isocyanate, die bei der Herstellung von Polyurethanschäumen, Beschichtungen und Klebstoffen eine wesentliche Rolle spielen.
- Produktion von Pestiziden: Kohlendichlorid erleichtert die Synthese bestimmter Pestizide und Herbizide und trägt so zum Pflanzenschutz und zur Schädlingsbekämpfung bei.
- Herstellung von Polycarbonat: Kohlendioxid ist ein entscheidender Bestandteil bei der Herstellung von Polycarbonat-Kunststoffen, die in einer Vielzahl von Produkten verwendet werden, von Brillen bis hin zu Wasserflaschen.
- Textilindustrie: Kohlendichlorid ist an der Herstellung bestimmter Farbstoffe und anderer Chemikalien beteiligt, die in der Textilindustrie verwendet werden.
- Schaumproduktion: Kohlendioxid spielt eine Schlüsselrolle bei der Herstellung von Schaummaterialien, einschließlich einiger Schaumarten, die zur Isolierung verwendet werden.
- Arzneimittel: Kohlendichlorid fungiert als chemisches Zwischenprodukt bei der Herstellung bestimmter Arzneimittel.
- Laborforschung: Forscher verwenden manchmal Kohlendioxid in Laborexperimenten.
- Herstellung von synthetischem Kautschuk: Kohlendioxid ist ein wesentlicher Bestandteil bei der Herstellung einiger synthetischer Kautschuke.
- Wasseraufbereitung: Früher wurde Kohlendichlorid in geringen Mengen zur Wasseraufbereitung verwendet, heutzutage werden für diesen Zweck jedoch häufiger sicherere Alternativen verwendet.
Obwohl Kohlendioxid wichtige industrielle Anwendungen hat, erfordern seine hohe Toxizität und seine gefährlichen Eigenschaften strenge Sicherheitsmaßnahmen bei Handhabung, Lagerung und Transport, um Unfälle zu verhindern und das Wohlbefinden von Arbeitern und Menschen zu gewährleisten. die Umgebung.
Fragen:
F: Was macht Phosgengas mit einem Menschen?
A: Kohlendioxidgas kann Atemwegsschäden verursachen, die zu Atembeschwerden und möglicherweise tödlichen Lungenödemen führen können.
F: Was ist Phosgen?
A: Kohlendioxid ist eine hochgiftige chemische Verbindung, die in verschiedenen industriellen Prozessen verwendet wird.
F: Was ist Phosgengas?
A: Kohlendioxidgas ist die gasförmige Form der chemischen Verbindung, die für ihre erstickende und toxische Wirkung auf die Atemwege bekannt ist.
F: Was macht Phosgen mit dem Körper?
A: Kohlendioxid kann die Lunge schädigen und zu Flüssigkeitsansammlungen und schwerer Atemnot führen.
F: Wie oft wird Grignard mit Phosgen reagieren?
A: Das Grignard-Reagenz reagiert nur einmal mit Kohlenstoffdichlorid und bildet ein Keton.
F: Welches menschliche Organ greift Chlorgas und Phosgen an?
A: Chlor- und Kohlendioxidgase greifen hauptsächlich die Lunge an.
F: Wie tötet Sie Phosgengas?
A: Kohlendioxidgas verursacht schwere Lungenreizungen, die zu Flüssigkeitsansammlungen und Erstickungsgefahr führen.
F: Wer hat Phosgengas erfunden?
A: Kohlendioxidgas wurde 1812 vom britischen Chemiker John Davy entdeckt.
F: Auswirkungen von Kohlendioxidgas?
A: Kohlendioxidgas kann Atemschäden, Lungenödeme und in schweren Fällen den Tod verursachen.
F: Lewis-Struktur von Kohlendioxid?
A: Die Lewis-Struktur von Kohlendichlorid besteht aus einem Kohlenstoff, der doppelt an Sauerstoff gebunden ist, und einer Einfachbindung an zwei Chloratome.
F: Kohlendioxidgas im Ersten Weltkrieg?
A: Kohlendioxid wurde im Ersten Weltkrieg als chemische Waffe eingesetzt und hatte verheerende Auswirkungen auf Soldaten.
F: Wann wurde Phosgengas zum ersten Mal verwendet?
A: Kohlendioxidgas wurde erstmals 1915 im Ersten Weltkrieg als chemische Waffe eingesetzt.
F: Woher kommt Phosgen?
A: Kohlendioxid entsteht normalerweise durch die Reaktion von Chlor mit Kohlenmonoxid oder anderen kohlenstoffhaltigen Verbindungen.
