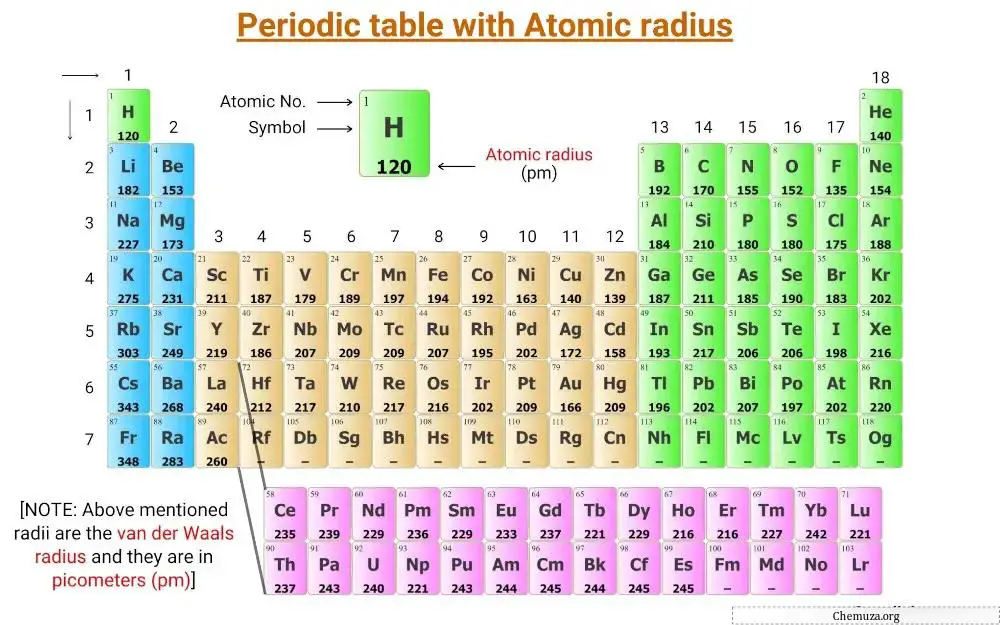
Dabei handelt es sich um ein Periodensystem mit den darauf beschrifteten Atomradiuswerten der Elemente.
Die im obigen Periodensystem genannten Radien sind der Van-der-Waals-Radius und werden in Pikometern (pm) angegeben.
Nun, es gibt einige wichtige konzeptionelle Dinge über den Atomradius von Elementen, die Sie wissen sollten.
Also lasst uns gleich loslegen.
Was ist der Atomradius?
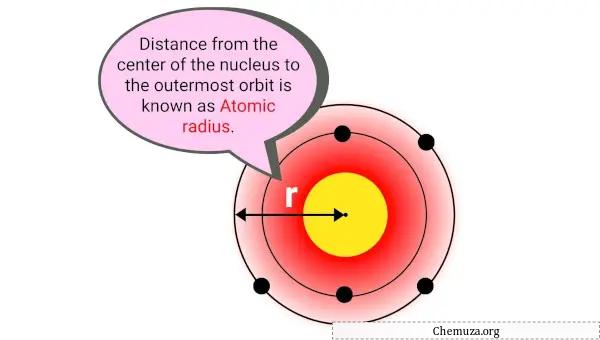
Der Atomradius ist der Abstand zwischen der Mitte des Atomkerns und dem äußersten Elektron in seiner Elektronenwolke.
Einfacher ausgedrückt ist es die Größe eines Atoms. Der Atomradius wird normalerweise in Pikometern (pm) oder einem Billionstel Meter gemessen.
Atome sind extrem klein und schwer vorstellbar, aber das Konzept des Atomradius hilft uns zu verstehen, wie Atome miteinander interagieren und wie sie sich bei verschiedenen chemischen Reaktionen verhalten.
Die Größe eines Atoms kann seine chemischen Eigenschaften beeinflussen, beispielsweise wie es sich mit anderen Atomen oder Molekülen verbindet.
Wie messen wir den Atomradius?
Der Atomradius wird üblicherweise mit verschiedenen experimentellen Methoden wie Röntgenkristallographie, Elektronenbeugung und Spektroskopie gemessen.
Bei diesen Methoden wird das Verhalten von Atomen untersucht, wenn sie mit bestimmten Energieformen wie Röntgenstrahlen oder Elektronen interagieren.
- Bei der Röntgenkristallographie wird ein Röntgenstrahl auf einen Kristall des zu untersuchenden Elements gerichtet. Die Röntgenstrahlen beugen die Atome im Kristall und das resultierende Beugungsmuster kann verwendet werden, um den Abstand zwischen den Atomen und damit ihre Radien zu bestimmen.
- Bei der Elektronenbeugung wird ein Elektronenstrahl auf einen dünnen Film des zu untersuchenden Elements gerichtet. Wenn die Elektronen den Film passieren, streuen sie die Atome und erzeugen ein Beugungsmuster, das analysiert werden kann, um den Atomradius zu bestimmen.
- Bei der Spektroskopie geht es um die Untersuchung der Wechselwirkungen zwischen Licht und Materie. Durch die Analyse der Wellenlängen des von einem Atom absorbierten oder emittierten Lichts können Wissenschaftler seinen Atomradius bestimmen.
Faktoren, die den Atomradius beeinflussen
Die Größe eines Atoms wird von verschiedenen Faktoren beeinflusst, darunter:
- Atomladung
- Elektronische Konfiguration
- Abstand der Valenzelektronen vom Kern usw.
Atomladung
Die Anzahl der Protonen im Atomkern wird als Ordnungszahl bezeichnet. [1]
Mit zunehmender Ordnungszahl nimmt die Anzahl der Protonen im Kern zu, was zu einer größeren Kernladung führt.
Diese erhöhte Ladung zieht Elektronen stärker zum Kern, was zu einem kleineren Atomradius führt.
Elektronische Konfiguration
Die Art und Weise, wie Elektronen um den Atomkern herum angeordnet sind, bestimmt seine elektronische Konfiguration. [2]
Je näher die Elektronen am Kern sind, desto kleiner ist der Atomradius.
Atome mit einer größeren Anzahl von Elektronen in ihrem äußersten Energieniveau (Valenzschale) haben einen größeren Atomradius, da die Elektronen weiter vom Kern entfernt sind und weniger stark von ihm angezogen werden.
Abstand der Valenzelektronen vom Kern
Auch der Abstand zwischen den Valenzelektronen und dem Kern beeinflusst den Atomradius.
Mit zunehmender Zahl der Elektronenhüllen entfernen sich Valenzelektronen vom Kern, was zu einer Vergrößerung des Atomradius führt.
Es ist wichtig zu beachten, dass die Faktoren, die den Atomradius beeinflussen, miteinander verknüpft sind. Während beispielsweise eine Erhöhung der Kernladung zu einem kleineren Atomradius führt, führt eine Erhöhung der Anzahl der Elektronen im äußersten Energieniveau (Valenzschale) zu einem größeren Atomradius. Daher ergibt sich die Gesamtgröße eines Atoms aus einem Gleichgewicht zwischen diesen Faktoren.
Für weitere Informationen sollten Sie die Atomradiustrends im Periodensystem lesen.
Zusammenfassung
Der Atomradius ist die Größe eines Atoms, gemessen in Pikometern, vom Zentrum des Kerns bis zum äußersten Elektron in der Elektronenwolke.
Dies hilft uns zu verstehen, wie Atome interagieren und ihre chemischen Eigenschaften beeinflussen. Zur Messung des Atomradius werden experimentelle Methoden wie Röntgenkristallographie, Elektronenbeugung und Spektroskopie eingesetzt.
Faktoren, die den Atomradius beeinflussen, sind die Kernladung, die elektronische Konfiguration und der Abstand zwischen Valenzelektronen und dem Kern. Diese Faktoren hängen miteinander zusammen und bestimmen die Gesamtgröße eines Atoms.
