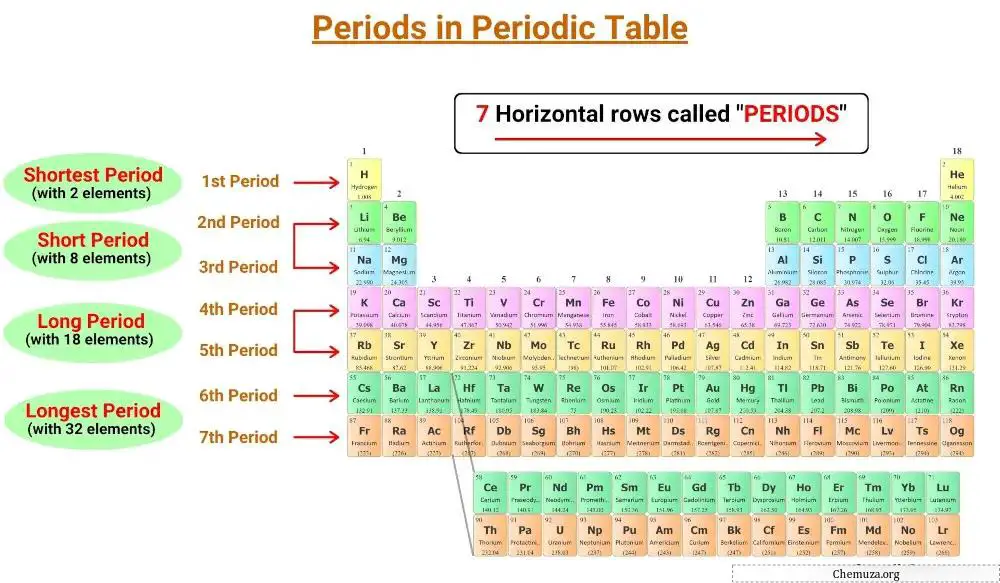
Die horizontalen Linien des Periodensystems werden Perioden genannt und es gibt 7 Perioden im Periodensystem.
Elemente, die sich im gleichen Zeitraum befinden, haben die gleiche Anzahl elektronischer Schichten.
Lassen Sie uns die Perioden im Periodensystem genauer untersuchen.
Was sind Perioden im Periodensystem?
Im Periodensystem sind Punkte die Linien, die horizontal von links nach rechts verlaufen.
Das Periodensystem ist so organisiert, dass Elemente mit ähnlichen Eigenschaften in Spalten, die Gruppen oder Familien genannt werden, gruppiert sind, während Elemente aus derselben Periode die gleiche Anzahl an Elektronenhüllen haben.
Es gibt sieben Perioden im Periodensystem, nummeriert von 1 bis 7. [1]
Anzahl der Schalen eines Elements und seine Periodennummer
Die Anzahl der Schalen eines Elements bestimmt seine Periode im Periodensystem.
Beispielsweise haben Elemente der Periode 1 nur eine Elektronenhülle, während Elemente der Periode 2 zwei Elektronenhüllen haben und so weiter.
Diese Organisation hilft Chemikern, die Eigenschaften eines Elements anhand seiner Position im Periodensystem vorherzusagen.
Eigenschaften von Elementen in Perioden
Wenn Sie sich durch eine Periode des Periodensystems bewegen, ändern sich mehrere Eigenschaften der Elemente auf vorhersehbare Weise. Dies ist auf die periodischen Trends zurückzuführen, die bei den Eigenschaften der Elemente beobachtet werden.
Atomradius:
Wenn man sich über einen bestimmten Zeitraum von links nach rechts bewegt, nimmt der Atomradius im Allgemeinen ab. [2]
Dies liegt daran, dass die Anzahl der Protonen im Kern zunimmt, was zu einer größeren Anziehungskraft zwischen dem Kern und den Elektronen auf dem äußersten Energieniveau führt. Dies führt zu einem kleineren Atomradius.
Elektronegativität:
Elektronegativität ist das Maß für die Fähigkeit eines Atoms, in einer chemischen Bindung Elektronen an sich zu ziehen.
Wenn man sich über einen bestimmten Zeitraum von links nach rechts bewegt, nimmt die Elektronegativität im Allgemeinen zu. [3]
Dies liegt daran, dass der Atomradius kleiner und die positive Ladung des Kerns stärker ist, wodurch er für negativ geladene Elektronen attraktiver wird.
Ionisationsenergie:
Die Ionisierungsenergie ist die Energiemenge, die benötigt wird, um ein Elektron aus einem Atom zu entfernen.
Wenn Sie sich über einen bestimmten Zeitraum von links nach rechts bewegen, nimmt die Ionisierungsenergie im Allgemeinen zu. [4]
Dies liegt daran, dass der Atomradius kleiner ist und die Elektronen fester vom Kern gehalten werden, wodurch es schwieriger wird, ein Elektron zu entfernen.
Andere Eigenschaften:
Schmelz- und Siedepunkte: Steigen im Allgemeinen über einen bestimmten Zeitraum von links nach rechts an, jedoch mit einigen Ausnahmen.
Metallischer Charakter: nimmt im Verlauf eines Zeitraums von links nach rechts ab, da Nichtmetalle häufiger vorkommen.
Reaktivität: Elemente werden weniger reaktiv, wenn man sich über einen bestimmten Zeitraum von links nach rechts bewegt, da Elektronen fester festgehalten werden und die Wahrscheinlichkeit geringer ist, dass sie an chemischen Reaktionen teilnehmen.
Bedeutung von Perioden in der Chemie
Die Perioden des Periodensystems sind für das Verständnis des Verhaltens von Elementen von entscheidender Bedeutung, da sie Informationen über die elektronische Konfiguration von Elementen und ihre Wechselwirkungen mit anderen Elementen liefern. Hier sind einige Gründe, warum Perioden in der Chemie wichtig sind:
- Eigenschaften vorhersagen: Das Periodensystem ermöglicht es Wissenschaftlern, die Eigenschaften von Elementen basierend auf ihrer Position im Periodensystem vorherzusagen. Beispielsweise haben Elemente aus derselben Zeit die gleiche Anzahl an Elektronenhüllen, was dabei helfen kann, ihre Atomgröße, Reaktivität und andere Eigenschaften vorherzusagen.
- Trends erkennen: Die Anordnung der Elemente im Periodensystem ermöglicht es Wissenschaftlern, Trends in ihren Eigenschaften zu erkennen. Beispielsweise neigen Elektronegativität und Ionisierungsenergie dazu, über einen bestimmten Zeitraum von links nach rechts zuzunehmen, während die Atomgröße tendenziell abnimmt. Diese Informationen können verwendet werden, um Vorhersagen darüber zu treffen, wie sich Elemente bei chemischen Reaktionen verhalten.
- Gruppierung von Elementen: Das Periodensystem gruppiert Elemente basierend auf ihren Eigenschaften in Kategorien, z. B. Metalle, Nichtmetalle und Metalloide . Dies hilft Wissenschaftlern, die Ähnlichkeiten und Unterschiede zwischen Elementen und wie sie miteinander interagieren, zu verstehen.
- Entdeckung neuer Elemente: Das Periodensystem hilft Wissenschaftlern auch dabei, die Existenz und Eigenschaften neuer Elemente vorherzusagen. Durch die Untersuchung von Lücken in der Tabelle können Wissenschaftler die Eigenschaften unentdeckter Elemente vorhersagen und diese im Labor erforschen.
Zusammenfassung
Das Periodensystem hat sieben horizontale Linien, die Perioden genannt werden. Elemente aus derselben Zeit haben die gleiche Anzahl elektronischer Schichten. Es gibt sieben Perioden im Periodensystem, nummeriert von 1 bis 7, und die Anzahl der Schalen eines Elements bestimmt seine Periode.
Wenn Sie eine Periode des Periodensystems durchlaufen, nimmt der Atomradius im Allgemeinen ab, während die Elektronegativität und die Ionisierungsenergie im Allgemeinen zunehmen. Auch andere Eigenschaften wie Schmelz- und Siedepunkte, Metallcharakter und Reaktivität ändern sich im Laufe der Zeit vorhersehbar.
Die Perioden des Periodensystems sind wichtig, um die Eigenschaften von Elementen vorherzusagen, Trends zu erkennen, Elemente zu gruppieren und neue Elemente zu entdecken. Durch die Untersuchung von Lücken in der Tabelle können Wissenschaftler die Eigenschaften unentdeckter Elemente vorhersagen und diese im Labor erforschen.
