p-Toluolsulfonsäure ist eine starke organische Säure mit stechendem Geruch. Es wird als Katalysator in verschiedenen chemischen Reaktionen und als Reagens in der organischen Synthese verwendet.
| IUPAC-Name | p-Toluolsulfonsäure |
| Molekularformel | C7H8O3S |
| CAS-Nummer | 104-15-4 |
| Synonyme | PTSA, 4-Methylbenzolsulfonsäure, p-Toluolsulfonsäure |
| InChI | InChI=1S/C7H8O3S/c1-6-2-4-7(5-3-6)11(8,9)10/h2-5H,1H3,(H,8,9,10) |
Eigenschaften von p-Toluolsulfonsäure
p-Toluolsulfonsäure-Formel
Die Formel für 4-Methylbenzolsulfonsäure lautet C7H8O3S. Es stellt die molekulare Zusammensetzung der Säure dar, bestehend aus sieben Kohlenstoffatomen, acht Wasserstoffatomen, drei Sauerstoffatomen und einem Schwefelatom.
p-Toluolsulfonsäure Molmasse
Die Molmasse von 4-Methylbenzolsulfonsäure wird auf etwa 172,2 Gramm pro Mol geschätzt. Unter Molmasse versteht man die Masse eines Mols eines Stoffes, die durch Addition der Atommassen seiner Atombestandteile bestimmt wird.
Siedepunkt von p-Toluolsulfonsäure
4-Methylbenzolsulfonsäure hat einen Siedepunkt von etwa 100 bis 110 Grad Celsius. Der Siedepunkt stellt die Temperatur dar, bei der sich die flüssige Form einer Substanz in einen Gaszustand umwandelt, wobei der Dampfdruck dem Atmosphärendruck entspricht.
p-Toluolsulfonsäure Schmelzpunkt
Der Schmelzpunkt von 4-Methylbenzolsulfonsäure liegt im Allgemeinen zwischen 105 und 107 Grad Celsius. Der Schmelzpunkt gibt die Temperatur an, bei der ein fester Stoff unter normalem Atmosphärendruck in den flüssigen Zustand übergeht.
Dichte von p-Toluolsulfonsäure g/ml
Die Dichte von 4-Methylbenzolsulfonsäure beträgt etwa 1,28 Gramm pro Milliliter (g/ml). Die Dichte bezieht sich auf die Masse einer Substanz pro Volumeneinheit und wird üblicherweise in Gramm pro Milliliter oder Gramm pro Kubikzentimeter ausgedrückt.
Molekulargewicht von p-Toluolsulfonsäure
Das Molekulargewicht von 4-Methylbenzolsulfonsäure beträgt etwa 172,2 Gramm pro Mol. Es stellt die Summe der Atomgewichte aller Atome in der Summenformel der Säure dar und gibt deren Masse auf der Molekülskala an.
Struktur von p-Toluolsulfonsäure
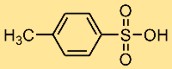
4-Methylbenzolsulfonsäure hat eine chemische Struktur, die aus einem Toluolring mit einer funktionellen Sulfonsäuregruppe (-SO3H) besteht, die an der para-Position (p-) des aromatischen Rings angebracht ist. Diese Struktur verleiht Säure und beeinflusst seine Reaktivität bei chemischen Reaktionen.
Löslichkeit von p-Toluolsulfonsäure
4-Methylbenzolsulfonsäure ist in Wasser und in vielen organischen Lösungsmitteln wie Ethanol und Aceton löslich. Seine Löslichkeit in Wasser beruht auf der Anwesenheit der polaren Sulfonsäuregruppe, die über Wasserstoffbrückenbindungen mit polaren Wassermolekülen interagiert.
| Aussehen | Weißes bis cremefarbenes kristallines Pulver |
| Spezifisches Gewicht | 1,28 g/ml |
| Farbe | Farblos bis hellgelb |
| Geruch | Stechender Geruch |
| Molmasse | 172,2 g/Mol |
| Dichte | 1,28 g/ml |
| Fusionspunkt | 105-107°C |
| Siedepunkt | 100-110°C |
| Blitzpunkt | Nicht verfügbar |
| Löslichkeit in Wasser | Löslich |
| Löslichkeit | Löslich in Ethanol, Aceton und anderen organischen Lösungsmitteln |
| Dampfdruck | Nicht verfügbar |
| Wasserdampfdichte | Nicht verfügbar |
| pKa | ~ -2 |
| pH-Wert | < 1 |
Sicherheit und Gefahren von p-Toluolsulfonsäure
4-Methylbenzolsulfonsäure birgt bestimmte Sicherheitsbedenken und Gefahren. Es wirkt ätzend auf Haut, Augen und Atemwege und verursacht bei Kontakt Reizungen und Verbrennungen. Das Einatmen seiner Dämpfe oder Stäube kann zu Atembeschwerden führen. Bei der Handhabung sollten Schutzmaßnahmen wie Handschuhe und Schutzbrillen getragen werden. Es sollte in einem dicht verschlossenen Behälter, fern von unverträglichen Substanzen, aufbewahrt werden. Bei Verschlucken oder versehentlicher Exposition ist sofortige ärztliche Hilfe erforderlich. Der Umgang mit Säure sollte in einem gut belüfteten Bereich erfolgen, um die Bildung gefährlicher Dämpfe zu vermeiden. Insgesamt sind geeignete Vorsichtsmaßnahmen und die Einhaltung von Sicherheitsrichtlinien unerlässlich, um potenzielle Risiken zu minimieren.
| Gefahrensymbole | Ätzend |
| Sicherheitsbeschreibung | – Kontakt mit Haut, Augen und Atemwegen vermeiden. – Tragen Sie Handschuhe, Schutzbrille und Schutzkleidung. – In einem dicht verschlossenen Behälter, entfernt von unverträglichen Substanzen, aufbewahren. |
| Identifikatoren der Vereinten Nationen | Nicht verfügbar |
| HS-Code | 29041000 |
| Gefahrenklasse | 8 (Ätzender Stoff) |
| Verpackungsgruppe | III (Geringe Gefahr) |
| Toxizität | Ätzend und reizend für Haut und Augen. Das Einatmen von Dämpfen oder Staub kann zu Atembeschwerden führen. |
Methoden zur Synthese von p-Toluolsulfonsäure
Verschiedene Methoden ermöglichen die Synthese von 4-Methylbenzolsulfonsäure. Ein üblicher Ansatz besteht darin, Toluol mit konzentrierter Schwefelsäure umzusetzen. Die Synthese von p-Toluolsulfonsäure erfordert die Aufrechterhaltung einer kontrollierten Temperatur während der Zugabe von Toluol zur Schwefelsäure. Bei der Reaktion entsteht als Hauptprodukt p-Toluolsulfonsäure.
Eine andere Methode beinhaltet die Oxidation des p-Toluolsulfonsäure-Vorläufers, p-Toluolsulfonylchlorid, unter Verwendung eines Oxidationsmittels wie Kaliumpermanganat oder Natriumdichromat . Die Reaktion findet in einem wässrigen oder organischen Lösungsmittel statt und führt zur Bildung von p-Toluolsulfonsäure.
Zur Herstellung von p-Toluolsulfonsäure kann rauchende Schwefelsäure (Oleum) oder Schwefeltrioxid zur Sulfonierung des Toluols verwendet werden. Bei dieser Methode wird Schwefelsäure oder Schwefeltrioxid unter kontrollierten Bedingungen in Toluol eingeführt, wodurch p-Toluolsulfonsäure entsteht.
Bei der Reaktion von Toluol mit Schwefelsäure zur Synthese von p-Toluolsulfonsäure ist ein Katalysator wie Benzoylperoxid oder Eisen(III)-chlorid vorhanden. Der Katalysator erleichtert den Sulfonierungsprozess und führt zur Bildung von p-Toluolsulfonsäure.
Diese Synthesemethoden ermöglichen die Herstellung von p-Toluolsulfonsäure, die in verschiedenen Branchen Anwendung findet, darunter Pharmazeutika, Farbstoffe und organische Synthese. Es ist wichtig zu beachten, dass bei diesen Syntheseprozessen entsprechende Sicherheitsvorkehrungen und ordnungsgemäße Handhabungsverfahren befolgt werden müssen.
Verwendung von p-Toluolsulfonsäure
4-Methylbenzolsulfonsäure hat viele Anwendungen in verschiedenen Branchen. Hier sind einige seiner häufigsten Verwendungszwecke:
- Chemische Reaktionen: 4-Methylbenzolsulfonsäure katalysiert Veresterungs-, Acylierungs- und Polymerisationsreaktionen.
- Organische Synthese: Verwenden Sie 4-Methylbenzolsulfonsäure als Reagenz, um funktionelle Sulfonsäuregruppen in Moleküle einzuführen und so Sulfonylierungs- und Desulfonierungsreaktionen in der organischen Synthese zu erleichtern.
- Pharmazeutika: Verwendung von 4-Methylbenzolsulfonsäure bei der Synthese pharmazeutischer Zwischenprodukte, einschließlich Antibiotika, Analgetika und Entzündungshemmer.
- Farbstoffherstellung: Verwendung von 4-Methylbenzolsulfonsäure bei der Herstellung von Farbstoffen und Pigmenten durch Sulfonierung aromatischer Verbindungen zur Herstellung von Farbstoffen.
- Galvanisieren: Verwenden Sie 4-Methylbenzolsulfonsäure als Säurekatalysator in Galvanisierungsprozessen, um Metallbeschichtungen auf verschiedenen Oberflächen abzuscheiden.
- Ionenaustauscherharze: Verwenden Sie 4-Methylbenzolsulfonsäure bei der Herstellung von Ionenaustauscherharzen für Wasseraufbereitungs-, Chromatographie- und Trennprozesse.
- Polymerindustrie: Einsatz von 4-Methylbenzolsulfonsäure als Polymerisationskatalysator und Stabilisator bei der Herstellung synthetischer Polymere und Kunststoffe.
- Oberflächenbehandlung: Verwenden Sie 4-Methylbenzolsulfonsäure zur Oberflächenbehandlung von Metallen wie Aluminium und Stahl, um deren Korrosionsbeständigkeit und Haftungseigenschaften zu verbessern.
- Reinigungsmittel: Fügen Sie 4-Methylbenzolsulfonsäure als Bestandteil in Reinigungsmitteln und Reinigungsmitteln hinzu, um mineralische Ablagerungen und Rostflecken zu entfernen.
- Analytische Chemie: Verwenden Sie 4-Methylbenzolsulfonsäure als Standardsubstanz für Kalibrierungszwecke in verschiedenen Analysetechniken, wie beispielsweise der Hochleistungsflüssigkeitschromatographie (HPLC).
Diese vielfältigen Anwendungen unterstreichen die Vielseitigkeit und Bedeutung von 4-Methylbenzolsulfonsäure in verschiedenen industriellen Prozessen und wissenschaftlichen Bereichen.
Fragen:
F: Wie reagieren Ethanol und p-Toluolsulfonsäure mit einem Carbonyl?
A: Ethanol und 4-Methylbenzolsulfonsäure können mit einem Carbonyl verestert werden, was zur Bildung eines Esters führt.
F: Wofür wird p-Toluolsulfonsäure verwendet?
Eine 4-Methylbenzolsulfonsäure findet Anwendung als Katalysator, Reagenz in der organischen Synthese, bei der Herstellung von Farbstoffen, in der pharmazeutischen Synthese und bei der Oberflächenbehandlung von Metallen.
F: Ist Pyridinium-p-toluolsulfonat eine Säure?
A: Ja, Pyridinium-p-toluolsulfonat ist eine Säure, insbesondere ein Derivat der Pyridinsulfonsäure.
F: Ist p-Toluolsulfonsäure anorganisch?
A: Nein, 4-Methylbenzolsulfonsäure ist eine organische Verbindung, die Kohlenstoff-, Wasserstoff-, Sauerstoff- und Schwefelatome enthält.
F: Was ist der Mechanismus von p-Toluolsulfonsäure und Alkohol?
A: Der Mechanismus beinhaltet die Protonierung des Alkohols durch 4-Methylbenzolsulfonsäure, gefolgt von der Abspaltung eines Wassermoleküls, was zur Bildung eines Alkyl-p-toluolsulfonats führt.
F: Zeichnen Sie das/die organische(n) Produkt(e) der folgenden Reaktion: p-Toluolsulfonsäure.
A: Das/die organische(n) Produkt(e) hängt von den spezifischen Reaktionsbedingungen und beteiligten Reagenzien ab, da 4-Methylbenzolsulfonsäure an einer Vielzahl von Reaktionen teilnehmen kann.
F: Was sind p-Toluolsulfonsäure-Reaktionen?
A: 4-Methylbenzolsulfonsäure kann Reaktionen wie Veresterung, Sulfonierung, Desulfonierung und Substitutionsreaktionen mit verschiedenen organischen Verbindungen eingehen.
F: Ist p-Toluolsulfonsäure eine organische Base?
A: Nein, 4-Methylbenzolsulfonsäure ist keine organische Base, sondern aufgrund des Vorhandenseins einer Sulfonsäuregruppe eine organische Säure.
F: Wie stellt man ein Alken mit p-Toluolsulfonsäure her?
A: 4-Methylbenzolsulfonsäure allein wandelt eine Verbindung nicht direkt in ein Alken um. Es kann jedoch als Katalysator oder Reagens in bestimmten Reaktionen verwendet werden, die zur Bildung von Alkenen führen, wie z. B. Dehydratisierungs- oder Eliminierungsreaktionen.
