Milchsäure wird bei anstrengender körperlicher Betätigung von den Muskeln produziert und führt zu Müdigkeit. Es kommt auch in fermentierten Lebensmitteln wie Joghurt vor und wird in Hautpflegeprodukten zum Peeling verwendet.
| IUPAC-Name | 2-Hydroxypropansäure |
| Molekularformel | C3H6O3 |
| CAS-Nummer | 50-21-5 |
| Synonyme | Milchsäure, 2-Hydroxypropionsäure, DL-Milchsäure |
| InChI | InChI=1S/C3H6O3/c1-2(4)3(5)6/h2.4H,1H3,(H.5.6) |
Eigenschaften von Milchsäure
Milchsäureformel
Die chemische Formel für Milchsäure lautet C3H6O3. Es besteht aus drei Kohlenstoffatomen, sechs Wasserstoffatomen und drei Sauerstoffatomen. Diese Formel stellt die Anordnung und Art der in einem Milchsäuremolekül vorhandenen Atome dar.
Molmasse der Milchsäure
Die Molmasse der Milchsäure beträgt etwa 90,08 Gramm pro Mol. Sie wird berechnet, indem die Atommassen aller in einem Milchsäuremolekül vorhandenen Atome addiert werden.
Siedepunkt von Milchsäure
Milchsäure hat einen Siedepunkt von etwa 122 bis 135 Grad Celsius. Bei dieser Temperatur geht die Milchsäure vom flüssigen in den gasförmigen Zustand über. Der Siedepunkt kann je nach Reinheit und Konzentration der Milchsäure variieren.
Schmelzpunkt von Milchsäure
Der Schmelzpunkt der Milchsäure liegt bei etwa 17 bis 18 Grad Celsius. Bei dieser Temperatur vollzieht die Milchsäure einen Phasenwechsel von fest zu flüssig. Der Schmelzpunkt kann je nach spezifischer Form der Milchsäure leicht variieren.
Milchsäuredichte g/ml
Die Dichte der Milchsäure beträgt etwa 1,2 Gramm pro Milliliter (g/ml). Dieser Dichtewert gibt die Masse der Milchsäure an, die in einem bestimmten Volumen vorhanden ist. Dies ist ein wichtiges Merkmal zur Bestimmung der Konzentration von Milchsäurelösungen.
Molekulargewicht von Milchsäure
Das Molekulargewicht von Milchsäure beträgt etwa 90,08 Gramm pro Mol. Es stellt die Summe der Atomgewichte aller Atome in einem Milchsäuremolekül dar. Das Molekulargewicht wird in verschiedenen chemischen Berechnungen und Analysen verwendet.
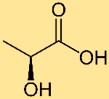
Struktur von Milchsäure
Milchsäure hat eine Struktur, die aus drei in einer Kette miteinander verbundenen Kohlenstoffatomen besteht, wobei an einem Kohlenstoff eine Hydroxylgruppe (-OH) und an einem anderen Kohlenstoff eine Carboxylgruppe (-COOH) gebunden ist. Diese Struktur ist für die sauren Eigenschaften der Milchsäure verantwortlich.
Löslichkeit von Milchsäure
Milchsäure ist wasserlöslich und bildet eine klare, farblose Lösung. Aufgrund seiner Fähigkeit, Wasserstoffbrückenbindungen mit Wassermolekülen zu bilden, löst es sich leicht auf. Die Löslichkeit von Milchsäure kann je nach Faktoren wie Temperatur und Konzentration variieren.
| Aussehen | Farblose Flüssigkeit |
| Spezifisches Gewicht | 1,2 g/ml |
| Farbe | Farblos |
| Geruch | Leicht säuerlicher Geruch |
| Molmasse | 90,08 g/Mol |
| Dichte | 1,2 g/ml |
| Fusionspunkt | 17-18°C |
| Siedepunkt | 122–135 °C |
| Blitzpunkt | 79°C |
| Löslichkeit in Wasser | Vollständig mischbar |
| Löslichkeit | Löslich in Ethanol, Wasser und Ether |
| Dampfdruck | 3,03 mmHg bei 25°C |
| Wasserdampfdichte | 2,55 (Luft=1) |
| pKa | 3,86 |
| pH-Wert | Ungefähr 2,4-3,4 |
Sicherheit und Gefahren von Milchsäure
Milchsäure birgt einige Sicherheitsbedenken und Gefahren. Es gilt als leicht reizend für Haut, Augen und Atemwege. Direkter Kontakt kann zu Reizungen, Rötungen und Beschwerden führen. Das Verschlucken konzentrierter Milchsäure kann zu Bauchschmerzen, Übelkeit und Erbrechen führen. Es ist wichtig, vorsichtig mit Milchsäure umzugehen und geeignete Schutzmaßnahmen wie Handschuhe und Schutzbrillen zu verwenden. Bei Haut- oder Augenkontakt wird eine Spülung mit reichlich Wasser empfohlen. Darüber hinaus sollte beim Arbeiten mit Milchsäure für ausreichende Belüftung gesorgt werden, um das Einatmen von Dämpfen zu vermeiden.
| Gefahrensymbole | Ätzend (C), Reizend (Xi) |
| Sicherheitsbeschreibung | Schutzhandschuhe und Augen-/Gesichtsschutz tragen. Vermeiden Sie das Einatmen von Dämpfen. Freisetzung in die Umwelt vermeiden. |
| UN-Identifikationsnummern | UN3265 |
| HS-Code | 2918.12.00 |
| Gefahrenklasse | Klasse 8 (ätzend) |
| Verpackungsgruppe | GE III |
| Toxizität | Milchsäure wird eine geringe akute Toxizität zugeschrieben. Dies kann zu Reizungen und Verbrennungen der Haut und Augen führen. Das Einatmen von Dämpfen kann zu Reizungen der Atemwege führen. Das Verschlucken konzentrierter Milchsäure kann zu Magen-Darm-Reizungen führen. Um potenzielle Risiken zu minimieren, sollten die ordnungsgemäße Handhabung und Sicherheitsvorkehrungen befolgt werden. |
Methoden der Milchsäuresynthese
Es gibt verschiedene Methoden zur Synthese von Milchsäure.
Eine gängige Methode ist die Fermentation von Kohlenhydraten durch Milchsäurebakterien. Bei diesem Prozess wandeln Mikroorganismen durch anaeroben Stoffwechsel Zucker wie Glukose oder Laktose in Milchsäure um. Diese Fermentation findet auf natürliche Weise in Lebensmitteln wie Joghurt, Sauerkraut und Gurken statt.
Eine andere Methode beinhaltet die chemische Synthese unter Verwendung von Acetaldehyd als Ausgangsmaterial. Acetaldehyd reagiert mit Cyanidionen unter Bildung von Lactonitril. Dann kommt es zur Hydrolyse, die zur Umwandlung von Lactonitril in Milchsäure führt. Diese Methode erfordert eine sorgfältige Handhabung und Kontrolle der Reaktionsbedingungen.
Wissenschaftler produzieren aktiv Milchsäure durch biotechnologische Techniken, indem sie Bakterien wie Escherichia coli genetisch verändern. Sie modifizieren diese Bakterien so, dass sie Enzyme exprimieren, die Glukose oder andere Zucker in Milchsäure umwandeln. Dieses Verfahren ermöglicht die Produktion von Milchsäure in größerem Maßstab und mit besserer Prozesskontrolle.
Milchsäure wird aus nachwachsenden Rohstoffen wie Mais oder Zuckerrohr gewonnen, indem die in diesen Pflanzenmaterialien enthaltene Stärke oder Zellulose chemisch zu Glukose hydrolysiert wird. Durch mikrobielle oder enzymatische Einwirkung wird die Glukose dann zu Milchsäure fermentiert.
Jede dieser Methoden hat ihre Vorteile und Einschränkungen hinsichtlich Kosten, Skalierbarkeit und Umweltauswirkungen. Die Wahl der Synthesemethode hängt von der konkreten Anwendung und den gewünschten Eigenschaften der Milchsäure ab.
Verwendung von Milchsäure
Milchsäure findet zahlreiche Anwendungen in verschiedenen Branchen. Hier sind einige häufige Verwendungszwecke:
- Lebensmittel- und Getränkeindustrie: Milchsäure fungiert als natürliches Konservierungsmittel, Säureregulator und Geschmacksverstärker in Lebensmitteln wie Milchprodukten, Backwaren und Getränken. Es trägt zum würzigen Geschmack von Joghurt bei und verleiht Sauerteigbrot einen sauren Geschmack.
- Pharmazeutische Industrie: Milchsäure trägt aktiv zur Herstellung pharmazeutischer Produkte bei, darunter Medikamente, Salben und Cremes. Es dient als pH-Regler und Stabilisator in Formulierungen und verbessert deren Wirksamkeit und Haltbarkeit.
- Hautpflege und Kosmetik: Milchsäure ist aufgrund ihrer peelenden Eigenschaften ein wichtiger Inhaltsstoff in Hautpflegeprodukten. Es hilft, abgestorbene Hautzellen zu entfernen und sorgt für einen glatteren, strahlenderen Teint. Anti-Aging-Cremes und -Lotionen nutzen es aktiv als Inhaltsstoff.
- Textilindustrie: In der Textilindustrie ist Milchsäure aktiv am Färben beteiligt und reguliert den pH-Wert während des Färbe- und Druckprozesses. Es trägt zur Verbesserung der Farbechtheit und Farbstoffpenetration bei.
- Biokunststoffe: Milchsäure ist ein Vorläufer für die Herstellung biologisch abbaubarer Polymere wie Polymilchsäure (PLA). Unternehmen verwenden PLA häufig in Verpackungsmaterialien, Einwegbesteck und anderen umweltfreundlichen Produkten.
- Reinigungsprodukte: Reinigungsprodukte verwenden Milchsäure als starkes natürliches Desinfektions- und Entkalkungsmittel. Es hilft dabei, Mineralablagerungen und Flecken von Oberflächen zu entfernen und ist damit eine umweltfreundliche Alternative zu aggressiven Chemikalien.
- Industrielle Anwendungen: Milchsäure dient als Rohstoff für die Synthese verschiedener Chemikalien, darunter Laktate, Lösungsmittel und biologisch abbaubare Kunststoffe.
Die Vielseitigkeit von Milchsäure macht sie zu einem wertvollen Bestandteil in verschiedenen Branchen und trägt zur Entwicklung nachhaltiger und funktioneller Produkte bei.
Fragen:
F: Was ist Milchsäure?
A: Milchsäure ist eine Verbindung, die von den Muskeln bei intensivem Training oder durch die Fermentation von Zucker durch Mikroorganismen produziert wird und in fermentierten Lebensmitteln wie Joghurt vorkommt.
F: Wo findet die Milchsäuregärung statt?
A: Die Säuregärung von Milch findet in einer Vielzahl von Organismen statt, darunter Bakterien, Pilze und unsere eigenen Muskelzellen.
F: Was ist Milchsäuregärung?
A: Milchsäuregärung ist ein Stoffwechselprozess, der unter Abwesenheit von Sauerstoff Zucker in Milchsäure umwandelt und so Energie erzeugt.
F: Wofür wird Milchsäure verwendet?
A: Milchsäure trägt zu Müdigkeit und Muskelschmerzen bei, reguliert den Säuregehalt im Körper und vermittelt verschiedene biochemische Prozesse.
F: Was ist eine kommerzielle Nutzung der Milchsäuregärung?
A: Die saure Fermentation von Milch wird kommerziell bei der Herstellung von Joghurt, Sauerkraut, Gurken und anderen fermentierten Lebensmitteln eingesetzt.
F: Wie wird man Milchsäure los?
A: Sanfte Bewegung, ausreichende Flüssigkeitszufuhr und Dehnung können dabei helfen, Milchsäure aus den Muskeln zu entfernen und abzubauen.
F: Wo kommt Milchsäure vor?
A: Milchsäure kommt in verschiedenen natürlichen Quellen vor, beispielsweise in Milchprodukten, fermentierten Lebensmitteln und tierischen Muskeln.
F: Wie kann man die Milchsäure im Körper reduzieren?
A: Um die Bildung von Milchsäure zu reduzieren, kann man geeignete Aufwärm- und Abkühlroutinen einbauen, eine ausgewogene Ernährung einhalten und die Trainingsintensität im Laufe der Zeit schrittweise steigern.
