Lithiumaluminiumhydrid (LiAlH4) ist ein starkes Reduktionsmittel, das in der organischen Chemie zur Umwandlung von Carbonylverbindungen in Alkohole verwendet wird. Es reagiert heftig mit Wasser.
| IUPAC-Name | Lithiumaluminiumhydrid |
| Molekularformel | LiAlH4 |
| CAS-Nummer | 16853-85-3 |
| Synonyme | Lithium(III)-tetrahydridoaluminat, Lithiumaluminium(III)-hydrid |
| InChI | InChI=1S/Al.Li.4H |
Eigenschaften von Lithiumaluminiumhydrid (LiAlH4)
Formel für Lithiumaluminiumhydrid (LiAlH4).
Die Formel von Lithiumtetrahydridoaluminat (LiAlH4) gibt seine Zusammensetzung an. Es besteht aus einem Lithiumatom (Li), einem Aluminiumatom (Al) und vier Wasserstoffatomen (H). Die Formel lautet LiAlH4, was auf das Vorhandensein dieser Elemente hinweist.
Molmasse von Lithiumaluminiumhydrid (LiAlH4).
Die Molmasse von Lithiumtetrahydridoaluminat (LiAlH4) ist die Summe der Atommassen seiner Bestandteile. Es wird wie folgt berechnet:
- Lithium (Li) hat eine Molmasse von etwa 6,94 g/mol.
- Aluminium (Al) hat eine Molmasse von etwa 26,98 g/mol.
- Wasserstoff (H) hat eine Molmasse von etwa 1,01 g/mol.
Addiert man diese Werte zusammen, beträgt die Molmasse von LiAlH4 etwa 37,95 g/mol.
Lithiumaluminiumhydrid (LiAlH4) Siedepunkt
Lithiumtetrahydridoaluminat (LiAlH4) hat keinen eindeutigen Siedepunkt, da es sich zersetzt, bevor eines seiner einzelnen Bestandteile den Siedepunkt erreicht. Beim Erhitzen unterliegt LiAlH4 einer Zersetzungsreaktion, bei der Wasserstoffgas freigesetzt wird.
Lithiumaluminiumhydrid (LiAlH4) Schmelzpunkt
Lithiumtetrahydridoaluminat (LiAlH4) hat einen relativ niedrigen Schmelzpunkt. Es schmilzt bei etwa 150–160 °C (302–320 °F). Bei dieser Temperatur geht das feste LiAlH4 in einen flüssigen Zustand über und kann so an chemischen Reaktionen teilnehmen.
Lithiumaluminiumhydrid (LiAlH4) Dichte g/ml
Die Dichte von Lithiumtetrahydridoaluminat (LiAlH4) beträgt etwa 0,917 g/ml. Dieser Dichtewert gibt die in einem bestimmten Volumen vorhandene Masse von LiAlH4 in der Einheit Gramm pro Milliliter an.
Lithiumaluminiumhydrid (LiAlH4) Molekulargewicht
Das Molekulargewicht von Lithiumtetrahydridoaluminat (LiAlH4) wird durch Addition der Atomgewichte aller seiner Bestandteile berechnet. Das Molekulargewicht von LiAlH4 beträgt etwa 37,95 g/mol.
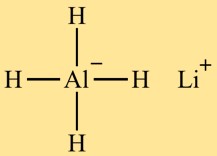
Struktur von Lithiumaluminiumhydrid (LiAlH4)
Lithiumtetrahydridoaluminat (LiAlH4) hat eine tetraedrische Struktur. Im Zentrum befindet sich das Aluminiumatom, umgeben von vier Wasserstoffatomen. Das Lithiumatom ist außerdem mit dem Aluminiumatom verbunden, wodurch die Struktur vervollständigt wird.
Löslichkeit von Lithiumaluminiumhydrid (LiAlH4)
Lithiumtetrahydridoaluminat (LiAlH4) ist in den meisten organischen Lösungsmitteln wie Ethern und Kohlenwasserstoffen unlöslich. Es ist jedoch sehr reaktiv mit Wasser, geht eine heftige exotherme Reaktion ein und erzeugt Wasserstoffgas. Daher wird LiAlH4 im Allgemeinen unter wasserfreien Bedingungen gehandhabt und gelagert, um jegliche negative Reaktion mit Feuchtigkeit zu vermeiden.
| Aussehen | weißes Puder |
| Spezifisches Gewicht | 0,917 g/ml |
| Farbe | Farblos |
| Geruch | Geruchlos |
| Molmasse | 37,95 g/Mol |
| Dichte | 0,917 g/ml |
| Fusionspunkt | 150-160°C |
| Siedepunkt | Zersetzt |
| Blitzpunkt | Unzutreffend |
| Löslichkeit in Wasser | Reagiert heftig mit Wasser |
| Löslichkeit | Unlöslich in organischen Lösungsmitteln wie Ethern und Kohlenwasserstoffen |
| Dampfdruck | Unzutreffend |
| Wasserdampfdichte | Unzutreffend |
| pKa | Unzutreffend |
| pH-Wert | Unzutreffend |
Sicherheit und Gefahren von Lithiumaluminiumhydrid (LiAlH4).
Lithiumtetrahydridoaluminat (LiAlH4) birgt erhebliche Sicherheitsrisiken und sollte mit äußerster Vorsicht gehandhabt werden. Es handelt sich um eine hochreaktive Verbindung, die heftig mit Wasser reagiert und dabei brennbares Wasserstoffgas freisetzt. LiAlH4 ist pyrophor, das heißt, es kann sich an der Luft spontan entzünden. Es sollte vor Feuchtigkeit geschützt und in dicht verschlossenen Behältern gelagert werden. Direkter Kontakt mit LiAlH4 kann schwere Verbrennungen und Reizungen der Haut, Augen und Atemwege verursachen. Das Einatmen von Staub oder Dämpfen kann zu Atembeschwerden führen. Bei der Arbeit mit LiAlH4 sollte geeignete persönliche Schutzausrüstung wie Handschuhe und Schutzbrille getragen werden, und die Handhabung sollte nur in gut belüfteten Bereichen mit entsprechenden Sicherheitsmaßnahmen erfolgen.
| Gefahrensymbole | F, C |
| Sicherheitsbeschreibung | Hochentzündlich. Reagiert heftig mit Wasser. Mit äußerster Vorsicht umgehen. |
| UN-Identifikationsnummern | UN 1410 |
| HS-Code | 2850.00.00 |
| Gefahrenklasse | 4.3 |
| Verpackungsgruppe | ICH |
| Toxizität | Sehr giftig, kann schwere Verbrennungen und Atembeschwerden verursachen. |
Hinweis: Die verwendeten Gefahrensymbole sind „F“ für entzündlich und „C“ für ätzend. Die Beschreibung Sicherheit hebt die Reaktionsfähigkeit mit Wasser hervor und betont die Notwendigkeit äußerster Vorsicht. UN-Kennungen und HS-Code sind spezifische Identifikationscodes, die für Transport- und Handelszwecke verwendet werden. Die Gefahrenklasse gibt die Einstufung des Stoffes anhand seiner Eigenschaften an. Die Verpackungsgruppe gibt den Gefahrengrad beim Transport an. Lithiumtetrahydridoaluminat (LiAlH4) ist hochgiftig und kann bei Kontakt oder Einatmen schwere Verbrennungen und Atembeschwerden verursachen.
Methoden zur Synthese von Lithiumaluminiumhydrid (LiAlH4)
Verschiedene Methoden ermöglichen die Synthese von Lithiumtetrahydridoaluminat (LiAlH4).
Eine übliche Methode zur Synthese von Lithiumtetrahydridoaluminat (LiAlH4) besteht darin, AlCl3 zu erhitzen und es mit Lithiumhydrid (LiH) in einem Lösungsmittel wie Diethylether zu kombinieren. Die Reaktion findet unter Hitzeeinwirkung statt und führt zur Bildung von LiAlH4.
Eine andere Methode besteht darin, pulverförmiges Aluminiummetall mit Lithiumhydrid zu mischen und die Mischung dann zu erhitzen. Die Reaktion führt zur Bildung von LiAlH4.
Um LiAlH4 mit einem anderen Ansatz zu synthetisieren, kombinieren Sie Lithiumaluminiumdeuterid (LiAlD4) mit LiH in einem Lösungsmittel wie Tetrahydrofuran (THF) . Erhitzen Sie die Mischung, was zu einer Reaktion zwischen LiAlD4 und Lithiumhydrid führt, was zur Bildung von LiAlH4 führt.
Es ist zu beachten, dass diese Synthesemethoden aufgrund der Reaktivität der beteiligten Verbindungen eine sorgfältige Handhabung erfordern. Vorsichtsmaßnahmen wie das Arbeiten unter inerten Bedingungen, die Verwendung geeigneter Sicherheitsausrüstung und die Durchführung von Reaktionen in gut belüfteten Bereichen sind für eine sichere und erfolgreiche Synthese unerlässlich.
Verwendung von Lithiumaluminiumhydrid (LiAlH4)
Lithiumtetrahydridoaluminat (LiAlH4) findet aufgrund seiner starken reduzierenden Eigenschaften mehrere Anwendungen in der organischen Chemie. Hier sind einige häufige Verwendungszwecke:
- Reduktion von Carbonylverbindungen: LiAlH4 wandelt verschiedene Carbonylverbindungen wie Aldehyde, Ketone, Ester und Carbonsäuren erheblich in die entsprechenden Alkohole um. Diese Reduktionsreaktion ist bei der Synthese von Pharmazeutika, Feinchemikalien und organischen Zwischenprodukten von entscheidender Bedeutung.
- Reduktion von Nitroverbindungen: LiAlH4 kann Nitroverbindungen zu primären Aminen reduzieren. Diese Umwandlung ist wertvoll für die Synthese einer Vielzahl organischer Verbindungen, darunter Pharmazeutika, Farbstoffe und Agrochemikalien.
- Desoxygenierung: LiAlH4 kann selektiv Sauerstoffatome aus verschiedenen funktionellen Gruppen wie Alkoholen, Säuren und Oximen entfernen. Dieser Desoxygenierungsprozess ist nützlich bei der Herstellung sauerstoffempfindlicher Verbindungen oder wenn die Sauerstofffunktionalität entfernt werden muss.
- Polymerisationsreaktionen: LiAlH4 fungiert bei bestimmten Polymerisationsreaktionen als Reduktionsmittel und erleichtert die Bildung von Polymeren. Forscher nutzen LiAlH4 bei der Herstellung von Hochleistungsmaterialien, darunter leitfähige Polymere und Spezialkunststoffe.
- Synthetische Anwendungen: LiAlH4 wird bei der Synthese verschiedener organischer Verbindungen verwendet, darunter Hydrazine, Phosphine und metallorganische Verbindungen. Diese Verbindungen sind in der pharmazeutischen Forschung, Katalyse und Materialwissenschaft unverzichtbar.
- Laborreduktionsmittel: LiAlH4 dient als vielseitiges Reduktionsmittel im Labor. Es ermöglicht Chemikern, bestimmte funktionelle Gruppen selektiv zu reduzieren und so komplexe Moleküle mit hoher Präzision zu synthetisieren.
Insgesamt spielt Lithiumtetrahydridoaluminat (LiAlH4) eine entscheidende Rolle in der organischen Synthese, da es Chemikern ein leistungsstarkes Werkzeug für verschiedene Reduktionsreaktionen bietet und die Herstellung einer Vielzahl wertvoller Verbindungen ermöglicht.
Fragen:
F: Reduziert Lithiumaluminiumhydrid Doppelbindungen?
A: Ja, Lithiumtetrahydridoaluminat kann Doppelbindungen reduzieren und in Einfachbindungen umwandeln.
F: Welches Gas setzt Lithiumaluminiumhydrid frei, wenn es mit einem protischen Lösungsmittel reagiert?
A: Wenn Lithiumtetrahydridoaluminat mit einem protischen Lösungsmittel reagiert, wird Wasserstoffgas freigesetzt.
F: Wo kann ich Lithiumaluminiumhydrid kaufen?
A: Lithiumtetrahydridoaluminat kann bei Chemikalienlieferanten oder spezialisierten Laborgerätelieferanten erworben werden.
F: Basiert Lithiumaluminiumhydrid?
A: Nein, Lithiumtetrahydridoaluminat gilt nicht als Base, sondern als starkes Reduktionsmittel.
F: Was reduziert LiAlH4?
A: Lithiumtetrahydridoaluminat kann verschiedene funktionelle Gruppen reduzieren, darunter Carbonylverbindungen, Nitrogruppen und Alkohole.
F: Ist Lithiumaluminiumhydrid ein Nukleophil?
A: Ja, Lithiumtetrahydridoaluminat wirkt aufgrund der Anwesenheit des Hydridions in vielen organischen Reaktionen als Nukleophil.
F: Reduziert Lithiumaluminiumhydrid Alkohole?
A: Ja, Lithiumtetrahydridoaluminat kann Alkohole reduzieren, um primäre oder sekundäre Alkohole zu erzeugen.
F: Reduziert Lithiumaluminiumhydrid Alkene?
A: Nein, Lithiumtetrahydridoaluminat reagiert im Allgemeinen nicht mit Alkenen.
F: Mit welchen der folgenden Lösungsmittel reagiert Lithiumaluminiumhydrid nicht?
A: Lithiumtetrahydridoaluminat reagiert im Allgemeinen nicht mit unpolaren Lösungsmitteln wie Hexan oder Diethylether.
F: Beeinflusst Lithiumaluminiumhydrid Alkohole?
A: Ja, Lithiumtetrahydridoaluminat kann Alkohole reduzieren, es sollte jedoch mit Vorsicht verwendet werden, da es sehr reaktiv und potenziell gefährlich sein kann.
