Eisen(ii)sulfat ist eine chemische Verbindung, die Eisen- und Sulfationen enthält. Es wird häufig zur Wasseraufbereitung und als Pflanzennährstoffergänzung verwendet.
| IUPAC-Name | Eisen(II)sulfat |
| Molekularformel | FeSO4 |
| CAS-Nummer | 7720-78-7 |
| Synonyme | Eisensulfat, Eisensulfat, grünes Vitriol, Melanterit, Szomolnokit |
| InChI | InChI=1S/Fe.H2O4S/c;1-5(2,3)4/h;(H2,1,2,3,4)/q+2;/p-2 |
Eigenschaften von Eisen(ii)sulfat
Eisen(II)-sulfat-Formel
Die chemische Formel für Eisen(II)sulfat lautet FeSO4. Diese Formel besagt, dass Eisensulfat aus einem Eisenatom, einem Schwefelatom und vier Sauerstoffatomen besteht. Die Formel von Eisensulfat ist ein wichtiger Parameter zur Berechnung verschiedener physikalischer und chemischer Eigenschaften der Verbindung, wie z. B. Molmasse und Molekulargewicht.
Molmasse von Eisen(II)sulfat
Die Molmasse von Eisensulfat beträgt 151,91 g/mol. Dieser Wert stellt die Masse eines Mols Eisensulfat dar, das 1 Eisenatom, 1 Schwefelmolekül und 4 Sauerstoffmoleküle enthält. Die Molmasse ist ein wichtiger Parameter zur Berechnung verschiedener physikalischer und chemischer Eigenschaften von Eisensulfat, wie z. B. Dichte und Konzentration.
Siedepunkt von Eisen(II)sulfat
Eisensulfat hat keinen bestimmten Siedepunkt, da es sich zersetzt, bevor es seinen Siedepunkt erreicht. Bei atmosphärischem Druck beginnt es sich bei etwa 300 °C zu zersetzen. Bei dieser Zersetzung gehen Wasser und Schwefeltrioxid verloren, wobei Eisen(III)-oxid zurückbleibt. Dieses Zersetzungsverhalten schränkt den Einsatz von Eisensulfat in Hochtemperaturanwendungen ein.
Eisen(II)-sulfat Schmelzpunkt
Der Schmelzpunkt von Eisensulfat hängt vom Hydratationsgrad ab. Wasserfreies Eisensulfat schmilzt bei 695 °C, während das gebildete Heptahydrat bei 64 °C schmilzt. Eisensulfat kann in verschiedenen hydratisierten Formen mit jeweils unterschiedlichem Schmelzpunkt vorliegen. Der Schmelzpunkt von Eisensulfat ist ein wichtiger Parameter zur Bestimmung der besten Bedingungen für die Herstellung und Handhabung der Verbindung.
Dichte von Eisen(II)sulfat g/ml
Die Dichte von Eisensulfat variiert je nach Hydratationsgrad. Wasserfreies Eisensulfat hat eine Dichte von 3,65 g/ml, während die Heptahydratform eine Dichte von 1,897 g/ml hat. Die Dichte von Eisensulfat ist ein wichtiger Parameter zur Berechnung des Volumens einer bestimmten Masse der Verbindung.
Molekulargewicht von Eisen(II)sulfat
Das Molekulargewicht von Eisensulfat beträgt 151,91 g/mol. Dieser Wert stellt die Summe der Atomgewichte der Atombestandteile eines Eisensulfatmoleküls dar. Das Molekulargewicht ist ein wichtiger Parameter zur Berechnung verschiedener physikalischer und chemischer Eigenschaften von Eisensulfat, wie Siedepunkt und Löslichkeit.
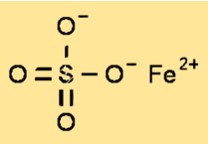
Struktur von Eisen(II)sulfat
Eisensulfat hat eine Kristallstruktur, die zum monoklinen System gehört. Die Kristallstruktur von Eisensulfat besteht aus Eisen(II)-Kationen, umgeben von sechs Wassermolekülen und Sulfatanionen. Die Kristallstruktur von Eisensulfat ist ein wichtiger Parameter für das Verständnis der physikalischen und chemischen Eigenschaften der Verbindung.
| Aussehen | Weißes oder hellgrünes kristallines Pulver |
| Spezifisches Gewicht | 3,65 g/cm3 (wasserfrei) |
| Farbe | Blasses Grün |
| Geruch | Geruchlos |
| Molmasse | 151,91 g/Mol |
| Dichte | 3,65 g/cm3 (wasserfrei), 1,89 g/cm3 (Heptahydrat) |
| Fusionspunkt | 695°C (wasserfrei), 64°C (Heptahydrat) |
| Siedepunkt | Zersetzt sich vor Erreichen des Siedepunkts |
| Blitzpunkt | Unzutreffend |
| Löslichkeit in Wasser | Sehr löslich |
| Löslichkeit | Löslich in Wasser, unlöslich in Ethanol |
| Dampfdruck | Unzutreffend |
| Wasserdampfdichte | Unzutreffend |
| pKa | Unzutreffend |
| pH-Wert | 4 (0,1 M Lösung) |
Sicherheit und Gefahren von Eisensulfat (ii)
Eisensulfat kann bestimmte Gefahren für die menschliche Gesundheit und Sicherheit darstellen. Bei Kontakt kann es zu Reizungen und Rötungen der Haut und Augen kommen, und das Einatmen des Staubs kann zu Reizungen der Atemwege führen. Beim Verschlucken kann es zu Bauchschmerzen, Übelkeit, Erbrechen und Durchfall kommen. Darüber hinaus kann die Exposition gegenüber Eisensulfat bei anfälligen Personen berufsbedingtes Asthma und Überempfindlichkeitspneumonitis verursachen. Es ist wichtig, die ordnungsgemäßen Handhabungs- und Lagerungsverfahren einzuhalten, geeignete persönliche Schutzausrüstung zu tragen und das Einatmen oder Verschlucken der Verbindung zu vermeiden. Im Falle einer versehentlichen Exposition suchen Sie sofort einen Arzt auf und konsultieren Sie das Sicherheitsdatenblatt.
| Gefahrensymbole | Xn,N |
| Sicherheitsbeschreibung | Von Feuchtigkeit, Säuren und Oxidationsmitteln fernhalten. Kontakt mit Haut, Augen und Kleidung vermeiden. Nicht einnehmen. Bei ausreichender Belüftung verwenden. Waschen Sie sich nach der Handhabung gründlich die Hände. |
| UN-Identifikationsnummern | UN3077, UN1376 |
| HS-Code | 2833.29.90 |
| Gefahrenklasse | 9 (verschiedene gefährliche Güter) |
| Verpackungsgruppe | III |
| Toxizität | Gesundheitsschädlich beim Verschlucken, verursacht Haut- und Augenreizungen und kann Reizungen der Atemwege verursachen. Kann durch Einatmen oder Hautkontakt zu Sensibilisierung führen. |
Methoden zur Synthese von Eisen(ii)sulfat
Es gibt verschiedene Methoden zur Synthese von Eisensulfat.
Eine gängige Methode ist die Reaktion von Eisenablagerungen mit Schwefelsäure in Gegenwart von Wasser und Sauerstoff. Dabei entsteht eine Eisensulfat-Heptahydrat-Lösung, die durch Kristallisation weiter gereinigt werden kann.
Eine andere Methode beinhaltet die Reaktion von Eisenoxid mit Schwefelsäure bei hoher Temperatur, gefolgt vom Abkühlen und Filtern der resultierenden Lösung.
Ein Reduktionsmittel wie Eisenpulver oder Schwefeldioxid kann Eisen(III)sulfat zu Eisensulfat reduzieren. Dabei entstehen Eisensulfat und Schwefelsäure . Zur Herstellung von Eisensulfat kann Eisen in Gegenwart von Wasser mit Schwefeldioxid und Sauerstoff umgesetzt werden.
Eine andere Methode beinhaltet die Reaktion von Eisen mit verdünnter Schwefelsäure in Gegenwart von Wasserstoffperoxid . Dabei entstehen Eisensulfat und Wasser.
Verwendung von Eisen(ii)sulfat
Eisen(II)sulfat hat ein breites Anwendungsspektrum in verschiedenen Branchen, darunter:
- Wasseraufbereitung: Wird häufig bei der Wasseraufbereitung verwendet, um Verunreinigungen wie Schwefelwasserstoff aus dem Wasser zu entfernen.
- Düngemittel: Werden bei der Herstellung von Düngemitteln verwendet, um Pflanzen mit essentiellen Eisennährstoffen zu versorgen.
- Pigmentherstellung: Wird als Vorstufe zur Herstellung verschiedener Eisenoxidpigmente wie Gelb- und Braunpigmente verwendet.
- Nahrungsergänzungsmittel: Wird als Nahrungsergänzungsmittel zur Behandlung von Eisenmangelanämie bei Menschen und Tieren verwendet.
- Abwasserbehandlung: Wird bei der Abwasserbehandlung zur Entfernung von Phosphat und anderen Verunreinigungen verwendet.
- Tintenherstellung: Wird bei der Tintenherstellung als Schwärzungsmittel verwendet.
- Holzschutzmittel: Werden als Holzschutzmittel verwendet, um Holz vor Pilz- und Insektenbefall zu schützen.
- Laborreagenz: Wird als Laborreagenz bei verschiedenen chemischen Reaktionen und Analysen verwendet.
Fragen:
Ist Eisensulfat wasserlöslich?
A: Eisensulfat, auch Eisensulfat genannt, ist in Wasser mäßig löslich.
F: Wie lautet die Formel für die Verbindung Eisen(ii)sulfat?
A: Die Formel für Eisensulfat lautet FeSO4.
F: Wie lautet die chemische Formel von Eisen(ii)sulfat?
A: Die chemische Formel für Eisensulfat lautet FeSO4.
F: Wie hoch ist der Schwefelanteil in Eisen(ii)sulfat?
A: Der Schwefelanteil in Eisensulfat beträgt 18,5 %.
F: Ist Eisen(ii)sulfat wasserlöslich?
A: Ja, Eisen-II-Sulfat, auch Eisensulfat genannt, ist wasserlöslich.
F: Was ist Eisensulfat?
A: Eisensulfat ist ein anderer Name für Eisensulfat, eine chemische Verbindung, die häufig in verschiedenen Branchen verwendet wird.
F: Wofür wird Eisensulfat verwendet?
A: Eisensulfat wird für eine Vielzahl von Zwecken verwendet, darunter Wasseraufbereitung, Düngemittelproduktion, Pigmentproduktion, Nahrungsergänzungsmittel, Tintenproduktion, Holzschutzmittel und Farbreagenzien. Labor.
