Tetrabromethan ist eine chemische Verbindung mit der Formel CBr4. Es ist ein farbloser kristalliner Feststoff mit süßem Geruch, der als Lösungsmittel und Flammschutzmittel verwendet wird. Es ist giftig und kann Mensch und Umwelt schaden.
| IUPAC-Name | Tetrabromethan |
| Molekularformel | CBr4 |
| CAS-Nummer | 558-13-4 |
| Synonyme | Kohlenstofftetrabromid, Tetrabromoform, Perbrommethan, Tetrabrommethan |
| InChI | InChI=1S/CBr4/c2-1(3,4)5 |
Eigenschaften von Tetrabromethan
Molmasse CBr4
Tetrabromethan hat eine Molmasse von etwa 331,63 g/mol. Im Vergleich zu anderen organischen Molekülen ist es eine relativ schwere Verbindung. Die Molmasse von Tetrabrommethan wird durch Addition der Atommassen aller Atome im Molekül bestimmt. In diesem Fall besteht es aus einem Kohlenstoffatom und vier Bromatomen.
Siedepunkt von CBr4
Tetrabromethan hat einen Siedepunkt von 189 °C (372 °F). Dies ist die Temperatur, bei der der Dampfdruck von flüssigem Tetrabromethan dem Atmosphärendruck entspricht. Bei dieser Temperatur beginnt das flüssige Tetrabrommethan zu sieden und zu einem Gas zu verdampfen.
Schmelzpunkt von CBr4
CBr4 hat einen Schmelzpunkt von 90,5 °C (194,9 °F). Dies ist die Temperatur, bei der festes CBr4 in den flüssigen Zustand übergeht. CBr4 hat für ein organisches Molekül einen relativ hohen Schmelzpunkt, was wahrscheinlich auf sein hohes Molekulargewicht und seine intermolekularen Kräfte zurückzuführen ist.
Dichte CBr4 g/ml
Die Dichte von Tetrabromethan beträgt bei Raumtemperatur 3,42 g/ml. Das bedeutet, dass ein bestimmtes Volumen Tetrabromethan 3,42-mal mehr wiegt als das gleiche Volumen Wasser. Die hohe Dichte von Tetrabromethan ist auf sein hohes Molekulargewicht und die dichte Anordnung seiner Atome zurückzuführen.
Molekulargewicht CBr4
Das Molekulargewicht von Tetrabromethan beträgt 331,63 g/mol. Es ist das Gesamtgewicht aller Atome im Molekül. Das Molekulargewicht von Tetrabromethan ist wichtig für die Berechnung seiner physikalischen Eigenschaften und für das Verständnis seines Verhaltens bei chemischen Reaktionen.
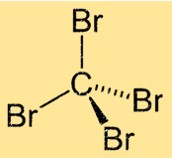
CBr4-Struktur
Tetrabrommethan hat eine tetraedrische Molekülgeometrie mit dem Kohlenstoffatom im Zentrum und den vier daran gebundenen Bromatomen. Das Molekül hat eine symmetrische Struktur mit vier identischen Br-C-Bindungen, die in gleichen Winkeln um das zentrale Kohlenstoffatom angeordnet sind. Diese Struktur verleiht Tetrabromethan seine einzigartigen physikalischen und chemischen Eigenschaften.
Tetrabromethan-Formel
Die Formel für Tetrabromethan lautet CBr4. Das bedeutet, dass es aus einem Kohlenstoffatom und vier Bromatomen besteht. Die Formel von Tetrabromethan ist wichtig für das Verständnis seiner chemischen Struktur und die Vorhersage seiner Reaktivität mit anderen Molekülen.
| Aussehen | Farbloser bis hellgelber kristalliner Feststoff |
| Spezifisches Gewicht | 3,42 g/ml |
| Farbe | Farblos bis hellgelb |
| Geruch | Weich |
| Molmasse | 331,63 g/Mol |
| Dichte | 3,42 g/ml |
| Fusionspunkt | 90,5 °C (194,9 °F) |
| Siedepunkt | 189°C (372°F) |
| Blitzpunkt | Nicht brennbar |
| Löslichkeit in Wasser | 0,0032 g/100 ml bei 20 °C |
| Löslichkeit | Unlöslich in Wasser, löslich in Benzol, Chloroform und Schwefelkohlenstoff |
| Dampfdruck | 0,006 mmHg bei 25 °C |
| Wasserdampfdichte | 14,2 (gegen Luft) |
| pKa | Unzutreffend |
| pH-Wert | Unzutreffend |
Sicherheit und Gefahren von Tetrabromethan
Tetrabromethan kann bei unsachgemäßer Handhabung mehrere Gefahren bergen. Es ist gesundheitsschädlich, wenn es verschluckt, eingeatmet oder mit der Haut in Berührung kommt. Der Kontakt mit Tetrabromethan kann zu Reizungen, Kopfschmerzen, Schwindel und Übelkeit führen. Eine längere Exposition kann zu Leber- und Nierenschäden führen. Es stellt außerdem eine potenzielle Gefahr für die Umwelt dar und sollte nicht in die Umwelt gelangen. Beim Umgang mit Tetrabrommethan sind entsprechende Vorsichtsmaßnahmen zu treffen, einschließlich der Verwendung von Schutzkleidung und -ausrüstung. Im Falle einer versehentlichen Exposition sollte sofort ein Arzt aufgesucht werden. Tetrabrommethan sollte in einem gut belüfteten Bereich und in Übereinstimmung mit den entsprechenden Sicherheitsprotokollen gelagert und gehandhabt werden.
| Gefahrensymbole | T (giftig) |
| Sicherheitsbeschreibung | Nicht einnehmen, einatmen oder mit der Haut in Berührung kommen. Tragen Sie Schutzkleidung und -ausrüstung. Bei versehentlicher Exposition einen Arzt konsultieren. |
| UN-Identifikationsnummern | UN 2515 |
| HS-Code | 2903.90.9000 |
| Gefahrenklasse | 6.1 |
| Verpackungsgruppe | II |
| Toxizität | Giftig bei Verschlucken, Einatmen oder Aufnahme durch die Haut. Kann Reizungen, Kopfschmerzen, Schwindel und Übelkeit verursachen. Eine längere Exposition kann Leber- und Nierenschäden verursachen. |
Methoden zur Synthese von Tetrabrommethan
Um Tetrabromethan zu synthetisieren, können Forscher Methan bromieren, Kohlenstofftetrabromid mit Wasserstoffgas reagieren lassen oder Brom mit Natriumformiat reagieren lassen.
Bei der Bromierung von Methan erfolgt die Reaktion von Methan mit Brom in Gegenwart eines Katalysators wie Eisen- oder Aluminiumbromid. Sie können das aus dem Prozess resultierende Gemisch aus Brommethanen trennen und reinigen, um Tetrabrommethan zu erhalten.
Um Tetrabromethan zu synthetisieren, kann Kohlenstofftetrabromid mit Wasserstoffgas in Gegenwart eines Katalysators wie Nickel umgesetzt werden. Bei dieser Reaktion entsteht eine Mischung aus Brommethanen, die Forscher trennen und reinigen können, um Tetrabrommethan zu erhalten.
Eine andere Methode zur Synthese von Tetrabromethan beinhaltet die Reaktion von Brom mit Natriumformiat in Gegenwart von Schwefelsäure. Die Trennung und Reinigung des resultierenden Produkts aus Tetrabromethan und Natriumsulfat ergibt Tetrabromethan.
Verwendungen von Tetrabromethan
Aufgrund seiner einzigartigen Eigenschaften findet Tetrabromethan zahlreiche Anwendungen in verschiedenen Branchen. Hier sind einige seiner Verwendungsmöglichkeiten:
- Flammhemmend: Wird als Flammschutzmittel in Kunststoffen, Textilien und anderen Materialien verwendet. Es setzt Brom frei, wenn es Hitze ausgesetzt wird, was den Verbrennungsprozess hemmt.
- Chemisches Zwischenprodukt: Wird als chemisches Zwischenprodukt bei der Herstellung anderer Chemikalien wie Pharmazeutika und Agrochemikalien verwendet.
- Lösungsmittel: Wird als Lösungsmittel für verschiedene organische Verbindungen verwendet, insbesondere bei der Herstellung von Pestiziden.
- Testmittel: Wird als Testmittel zum Nachweis von Verunreinigungen in anderen Chemikalien verwendet.
- Läutermittel: Wird als Läutermittel bei der Herstellung von Aluminium und anderen Metallen verwendet.
- Veterinärmedizin: Wird in der Veterinärmedizin als Anthelminthikum oder Entwurmungsmittel zur Behandlung parasitärer Infektionen bei Tieren verwendet.
Fragen:
F: Ist CBR4 polar oder unpolar?
A: Tetrabrommethan (cbr4) ist aufgrund seiner symmetrischen tetraedrischen Struktur und des Fehlens polarer Bindungen ein unpolares Molekül.
F: Welche der folgenden Verbindungen sind polar: cbr4, xef2, scl4, brf3, ch3oh?
A: Von den angegebenen Verbindungen sind nur CH3OH (Methanol) und BRF3 (Bromtrifluorid) aufgrund ihrer asymmetrischen Molekülstrukturen und des Vorhandenseins polarer Bindungen polare Moleküle.
F: Ist cbr4 wasserlöslich?
A: Tetrabromethan ist aufgrund seiner unpolaren Natur nicht wasserlöslich und mit der polaren Natur von Wasser nicht vereinbar.
F: Wie heißt die Verbindung der Formel cbr4? A: Die Verbindung der Formel cbr4 heißt Tetrabromethan oder Tetrabromkohlenstoff.
