Cäsiumnitrid (Cs3N) ist eine anorganische Verbindung aus Cäsium und Stickstoff mit einer geschichteten Kristallstruktur und hoher thermischer Stabilität. Es hat potenzielle Anwendungen in Bereichen wie Elektronik, Optoelektronik und Katalyse.
| IUPAC-Name | Cäsiumnitrid |
| Molekularformel | Cs3N |
| CAS-Nummer | 12134-29-1 |
| Synonyme | Tricäsiumnitrid |
| InChI | InChI=1S/3Cs.N/q3*+3;/p-3 |
Eigenschaften von Cäsiumnitrid
Cäsiumnitrid-Formel
Die chemische Formel für Cäsiumnitrid lautet Cs3N und besteht aus einem Cäsiumatom und drei Stickstoffatomen.
Molmasse von Cäsiumnitrid
Die Molmasse von Cs3N beträgt 412,7 g/mol. Sie wird als Summe der Atommassen seiner Bestandteile Cäsium (132,905 g/mol) und Stickstoff (14,01 g/mol) berechnet.
Siedepunkt von Cäsiumnitrid
Der Siedepunkt von Cs3N wurde aufgrund seiner Instabilität und Neigung zur Zersetzung bei hohen Temperaturen nicht experimentell bestimmt.
Schmelzpunkt von Cäsiumnitrid
Der Schmelzpunkt von Cs3N wird auf etwa 1000°C geschätzt. Es hat eine geschichtete Kristallstruktur und sein Schmelzpunkt hängt von den Synthesebedingungen und der Reinheit der Verbindung ab.
Cs3N Dichte g/ml
Die Dichte von Cs3N wird auf etwa 5,2 g/ml geschätzt. Aufgrund seiner Instabilität und Zerfallsneigung konnte seine Dichte jedoch nicht experimentell bestimmt werden.
Cs3N-Molekulargewicht
Das Molekulargewicht von Cs3N beträgt 412,7 g/mol. Sie wird als Summe der Atommassen seiner Bestandteile Cäsium und Stickstoff berechnet.
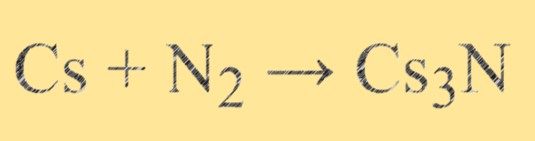
Struktur von Cäsiumnitrid
Cs3N hat eine geschichtete Kristallstruktur mit übereinander gestapelten Schichten aus Cäsium- und Stickstoffatomen. Es handelt sich um eine Verbindung mit hoher thermischer Stabilität und potenziellen Anwendungen in der Elektronik, Optoelektronik und Katalyse. Die genauen Details seiner Struktur und Eigenschaften werden von Forschern auf diesem Gebiet noch untersucht und analysiert.
| Aussehen | Nicht verfügbar |
| Spezifisches Gewicht | Nicht verfügbar |
| Farbe | Nicht verfügbar |
| Geruch | Nicht verfügbar |
| Molmasse | 412,7 g/Mol |
| Dichte | Schätzungsweise etwa 5,2 g/ml |
| Fusionspunkt | Etwa 1000°C |
| Siedepunkt | Nicht experimentell bestimmt |
| Blitzpunkt | Nicht verfügbar |
| Löslichkeit in Wasser | Nicht verfügbar |
| Löslichkeit | Nicht verfügbar |
| Dampfdruck | Nicht verfügbar |
| Wasserdampfdichte | Nicht verfügbar |
| pKa | Nicht verfügbar |
| pH-Wert | Nicht verfügbar |
Hinweis: Einige Werte sind Schätzungen oder wurden aufgrund der Instabilität von Cs3N und der Schwierigkeit der Handhabung der Verbindung nicht experimentell ermittelt.
Sicherheit und Gefahren von Cäsiumnitrid
Cs3N ist eine hochreaktive und instabile Verbindung, die sich bei hohen Temperaturen zersetzen kann. Die Handhabung kann gefährlich sein und bei der Arbeit damit sollten entsprechende Sicherheitsmaßnahmen und Vorsichtsmaßnahmen getroffen werden. Das Einatmen oder der Kontakt mit der Haut gegenüber Cs3N-Staub oder -Dämpfen kann giftig sein und Reizungen hervorrufen. Um mögliche Expositionen und Gefahren zu minimieren, wird die Lagerung in luftdichten Behältern und die ordnungsgemäße Entsorgung empfohlen.
Methoden zur Synthese von Cäsiumnitrid
Durch thermisches Nitrieren von Cäsiummetall in Stickstoffgas bei hoher Temperatur kann Cs3N synthetisiert werden. Um ein reines und stabiles Produkt zu erhalten, müssen Temperatur, Druck und Stickstofffluss sorgfältig kontrolliert werden. Hochdrucknitrieren ist eine weitere Methode zur Synthese von Cs3N, erfordert jedoch in der Regel spezielle Geräte und Bedingungen. Bei der Auswahl der zu verwendenden Synthesemethode ist es wichtig, die gewünschten Eigenschaften und Anwendungen des Endprodukts zu berücksichtigen.
Verwendung von Cäsiumnitrid
Forscher untersuchen Cs3N für mögliche Anwendungen in der Materialwissenschaft. Seine hohe thermische Stabilität und sein niedriger Reibungskoeffizient haben es zu einem Gegenstand von Studien für seinen Einsatz als Festschmierstoff gemacht. Seine Gefährlichkeit und begrenzte Stabilität erschweren jedoch den Einsatz in praktischen Anwendungen. Daher ist weitere Forschung erforderlich, um seine Eigenschaften und möglichen Verwendungsmöglichkeiten besser zu verstehen und sichere Methoden für die Handhabung und Verwendung zu entwickeln.
