Nitrobenzol oder C6H5NO2 ist eine organische Verbindung mit hellgelber Farbe und ausgeprägtem Geruch. Es wird als Vorprodukt für die Herstellung von Anilin und anderen Chemikalien verwendet. Es ist auch eine giftige Substanz.
| IUPAC-Name | Nitrobenzol |
| Molekularformel | C6H5NO2 |
| CAS-Nummer | 98-95-3 |
| Synonyme | Nitrobenzol, Nitrobenzeen, Mirbane Essence, NB |
| InChI | InChI=1S/C6H5NO2/c8-7(9)6-4-2-1-3-5-6/h1-5H |
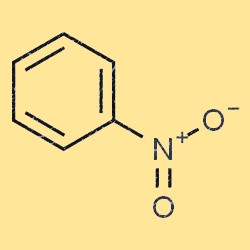
Struktur von Nitrobenzol
Nitrobenzol hat eine flache, planare Molekülstruktur. Es besteht aus einem Benzolring (C6H5) mit einer Nitrogruppe (-NO2), die an eines der Kohlenstoffatome gebunden ist. Die Nitrogruppe ist eine elektronenziehende Gruppe, was bedeutet, dass sie die Elektronendichte des Benzolrings verringert. Diese Eigenschaft macht Nitrobenzol bei vielen chemischen Reaktionen weniger reaktiv als Benzol.
Nitrobenzol-Formel
Die chemische Formel für Nitrobenzol lautet C6H5NO2. Diese Formel stellt die Anzahl und Art der Atome dar, aus denen das Molekül besteht. Der Benzolring bildet das Rückgrat des Moleküls, während die Nitrogruppe eine polare funktionelle Gruppe darstellt, die die Eigenschaften der Verbindung beeinflusst. Die Formel von Nitrobenzol ist wichtig für das Verständnis seiner chemischen und physikalischen Eigenschaften sowie seiner Reaktivität mit anderen Substanzen.
Molmasse von Nitrobenzol
Die Molmasse von Nitrobenzol, auch C6H5NO2 genannt, beträgt 123,11 g/mol. Dies wird berechnet, indem die Atommassen aller Atome in der Verbindung addiert werden. Nitrobenzol hat eine relativ hohe Molmasse, da in seiner chemischen Struktur sechs Kohlenstoffatome und ein Stickstoffatom vorhanden sind.
Siedepunkt von Nitrobenzol
Nitrobenzol hat einen Siedepunkt von 210,9 °C. Dies ist im Vergleich zu anderen organischen Verbindungen mit ähnlichen Molekulargewichten relativ hoch. Der hohe Siedepunkt ist auf das Vorhandensein starker intermolekularer Anziehungskräfte zwischen Nitrobenzolmolekülen zurückzuführen, wie etwa Wasserstoffbrückenbindungen und Dipol-Dipol-Wechselwirkungen.
Schmelzpunkt von Nitrobenzol
Der Schmelzpunkt von Nitrobenzol liegt bei 5,85°C. Dieser ist im Vergleich zu seinem Siedepunkt relativ niedrig, was dadurch erklärt werden kann, dass die intermolekularen Anziehungskräfte im festen Zustand schwächer sind als im flüssigen Zustand. Darüber hinaus kann Nitrobenzol Polymorphismus aufweisen, was bedeutet, dass es in mehreren Kristallstrukturen mit unterschiedlichen Schmelzpunkten vorliegen kann.
Dichte von Nitrobenzol g/ml
Die Dichte von Nitrobenzol beträgt 1,20 g/ml bei Raumtemperatur (25 °C). Das bedeutet, dass Nitrobenzol dichter ist als Wasser, das bei gleicher Temperatur eine Dichte von 1 g/ml hat. Die Dichte von Nitrobenzol wird durch sein Molekulargewicht sowie die Größe und Form seiner Moleküle beeinflusst.
Molekulargewicht von Nitrobenzol
Das Molekulargewicht von Nitrobenzol beträgt 123,11 g/mol. Dies wird berechnet, indem die Atommassen aller Atome in der Verbindung addiert werden. Das Molekulargewicht von Nitrobenzol ist wichtig für die Bestimmung seiner physikalischen und chemischen Eigenschaften wie Siedepunkt, Schmelzpunkt und Löslichkeit.
| Aussehen | Blassgelbe Flüssigkeit |
| Spezifisches Gewicht | 1,20 g/cm3 |
| Farbe | Blassgelb |
| Geruch | Charakteristisch |
| Molmasse | 123,11 g/Mol |
| Dichte | 1,20 g/ml bei 25 °C |
| Fusionspunkt | 5,85°C |
| Siedepunkt | 210,9°C |
| Blitzpunkt | 77°C |
| Löslichkeit in Wasser | 7,9 g/L bei 25°C |
| Löslichkeit | Löslich in organischen Lösungsmitteln |
| Dampfdruck | 0,68 mmHg bei 25°C |
| Wasserdampfdichte | 4,35 (Luft=1) |
| pKa | -1,15 |
| pH-Wert | 7 (neutral) |
Sicherheit und Gefahren von Nitrobenzol
Nitrobenzol ist eine hochgiftige Substanz, die mehrere Sicherheits- und Gesundheitsrisiken birgt. Bei Kontakt oder Einatmen kann es zu Reizungen der Haut, Augen und Atemwege kommen. Eine längere Exposition gegenüber Nitrobenzol kann Leber- und Nierenschäden, Anämie und Methämoglobinämie verursachen. Nitrobenzol ist außerdem sehr brennbar und kann sich bei relativ niedrigen Temperaturen entzünden. Darüber hinaus können beim Erhitzen, Verbrennen oder Zersetzen giftige Dämpfe freigesetzt werden. Daher ist es wichtig, mit Nitrobenzol vorsichtig umzugehen, entsprechende Schutzausrüstung zu tragen und es an einem kühlen, trockenen Ort, entfernt von Zündquellen und unverträglichen Substanzen, aufzubewahren.
| Gefahrensymbole | T,N |
| Sicherheitsbeschreibung | Sehr giftig, gesundheitsschädlich bei Verschlucken, Einatmen oder Aufnahme durch die Haut, verursacht schwere Hautverätzungen und Augenschäden. |
| AN-Kennungen | UN1662 |
| HS-Code | 2904.90.90 |
| Gefahrenklasse | 6.1 |
| Verpackungsgruppe | II |
| Toxizität | Sehr giftig |
Nitrobenzol-Synthesemethoden
Nitrobenzol kann durch verschiedene Methoden synthetisiert werden, einschließlich der Nitrierung von Benzol, der Reduktion von Nitrobenzol und der Hydrierung von Nitrobenzol. Die am häufigsten verwendete Methode ist die Benzolnitrierung, bei der Benzol mit einer Mischung aus Salpetersäure und Schwefelsäure bei einer Temperatur von etwa 50 °C reagiert. Bei der Nitrierungsreaktion entsteht eine Mischung aus Nitrobenzol sowie anderen Nitroderivaten von Benzol.
Eine weitere Methode zur Synthese von Nitrobenzol ist die Nitrobenzolreduktion, bei der Reduktionsmittel wie Eisen oder Zink und Salzsäure verwendet werden. Bei der Reduktionsreaktion wird die Nitrogruppe (-NO2) von Nitrobenzol in eine Aminogruppe (-NH2) umgewandelt, wobei Anilin als Nebenprodukt entsteht.
Die Hydrierung von Nitrobenzol ist eine weitere Methode der Anilinsynthese. Bei dieser Methode werden ein Katalysator wie Nickel oder Palladium und Wasserstoffgas verwendet, das mit Nitrobenzol unter Bildung von Anilin reagiert.
Verwendung von Nitrobenzol
Nitrobenzol ist eine vielseitige Chemikalie, die in einer Vielzahl von Anwendungen eingesetzt wird.
- Die chemische Industrie nutzt Nitrobenzol als Vorstufe für Anilin, einen wichtigen Bestandteil bei der Herstellung von Farbstoffen, Gummi und Arzneimitteln. Nitrobenzol ist ein wertvoller Rohstoff für die Herstellung anderer Chemikalien wie Phenol, die bei der Herstellung von Kunststoffen, Harzen und Klebstoffen verwendet werden.
- Organische Verbindungen wie Öle, Fette und Wachse können mit Nitrobenzol gelöst werden, was es zu einem nützlichen Lösungsmittel macht. In der Lebensmittelindustrie wird Nitrobenzol als Aromastoff verwendet, vor allem bei der Herstellung von Kaugummi.
- C6H5NO2 ist ein wesentlicher Bestandteil bei der Herstellung von Sprengstoffen wie TNT (Trinitrotoluol). Als Kraftstoffzusatz trägt Nitrobenzol dazu bei, die Oktanzahl von Benzin zu erhöhen.
- C6H5NO2 wird auch bei der Herstellung verschiedener Pestizide und Herbizide verwendet, darunter Insektizide und Fungizide.
- Auch die Herstellung synthetischer Fasern wie Nylon ist auf Nitrobenzol als wesentlichen Bestandteil angewiesen.
Insgesamt ist Nitrobenzol aufgrund seiner Vielseitigkeit in vielen Branchen, einschließlich der Chemie-, Lebensmittel- und Textilindustrie, eine unverzichtbare Chemikalie. Allerdings sind bei der Verwendung von Nitrobenzol aufgrund seiner Toxizität und Entflammbarkeit eine ordnungsgemäße Handhabung und Sicherheitsvorkehrungen erforderlich.
Fragen:
Reaktion von Nitrobenzol mit Anilin
Die Umwandlung von Nitrobenzol in Anilin ist eine zweistufige Reaktion, bei der die Nitrogruppe (-NO2) zu einer Aminogruppe (-NH2) reduziert und das Zwischenprodukt anschließend hydrolysiert wird.
Die Reduktion von C6H5NO2 erfolgt üblicherweise mit einem Reduktionsmittel wie Eisen oder Zink und einer sauren Lösung wie Salzsäure. Bei der Reaktion entsteht ein Zwischenprodukt, Nitrosobenzol, das dann in Gegenwart eines sauren oder basischen Katalysators zu Anilin reduziert wird.
Die Hydrolyse des Nitrosobenzol-Zwischenprodukts zu Anilin erfolgt durch Behandlung des Zwischenprodukts mit einer sauren Lösung, beispielsweise verdünnter Salzsäure. Bei der Reaktion entstehen Anilin sowie Wasser und Stickoxide (NO).
Die Gesamtreaktion lässt sich wie folgt darstellen: Nitrobenzol + 3 H2 → Anilin + 2 H2O + N2
