Ethylenoxid oder Epoxyethan (C2H4O) ist ein farbloses, brennbares Gas, das bei der Herstellung verschiedener Konsumgüter verwendet wird. Es ist außerdem ein starkes Sterilisationsmittel und kann gesundheitsschädlich sein.
| IUPAC-Name | Oxiran |
| Molekularformel | C2H4O |
| CAS-Nummer | 75-21-8 |
| Synonyme | Dimethylenoxid, Epoxyethan, Oxacyclopropan, 1,2-Epoxyethan, 2-Oxacyclopropan, Dihydrooxiren |
| InChI | InChI=1S/C2H4O/c1-2-4-3-1/h1-2H2 |
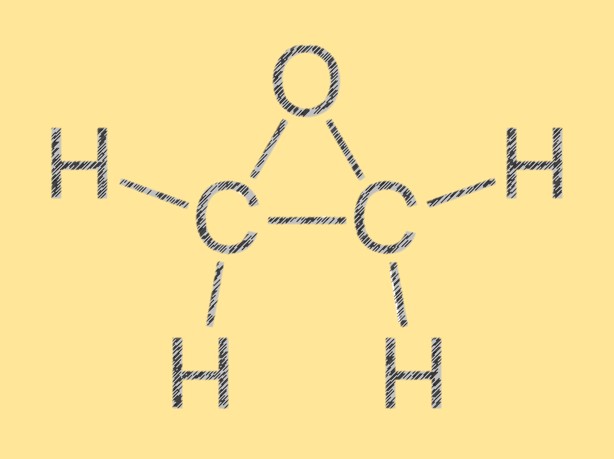
Epoxyethan-Struktur
Die Struktur von Epoxyethan ist ein dreigliedriger Ring, der aus zwei Kohlenstoffatomen und einem Sauerstoffatom besteht. Kohlenstoffatome sind durch eine Einfachbindung verbunden und jedes Kohlenstoffatom ist außerdem an ein Wasserstoffatom gebunden. Das Sauerstoffatom ist über eine Doppelbindung mit einem der Kohlenstoffatome verbunden. Die Molekülgeometrie von Epoxyethan ist trigonal-planar.
Molekulargewicht von Epoxyethan
Das Molekulargewicht von Epoxyethan beträgt 44,05 g/mol. Das Molekulargewicht ist die Summe der Atomgewichte aller Atome in einem Molekül und wird in Gramm pro Mol (g/mol) ausgedrückt. Das Molekulargewicht einer Verbindung ist bei vielen chemischen Berechnungen nützlich, beispielsweise bei der Bestimmung der Menge einer Substanz, die für eine bestimmte Reaktion erforderlich ist.
Molmasse von Ethylenoxid
Die Molmasse von Ethylenoxid beträgt 44,05 g/mol. Die Molmasse ist die Masse eines Mols einer Substanz und wird in Gramm pro Mol (g/mol) ausgedrückt. Die Molmasse einer Verbindung ist für viele chemische Berechnungen nützlich, beispielsweise zur Bestimmung der Masse einer bestimmten Anzahl von Molen einer Substanz oder zur Berechnung der Konzentration einer Lösung in Mol pro Liter.
Siedepunkt von C2H4O
Der Siedepunkt von Ethylenoxid beträgt 10,4 °C (50,7 °F) bei normalem Atmosphärendruck. Ethylenoxid ist ein flüchtiges und leicht entzündliches Gas, das bei relativ niedriger Temperatur siedet. Diese Eigenschaft macht es für bestimmte industrielle Anwendungen nützlich, beispielsweise für die Herstellung von Kunststoffen und synthetischen Fasern. Dies macht jedoch auch die Handhabung und den Transport von Ethylenoxid gefährlich.
Schmelzpunkt von Ethylenoxid
Ethylenoxid ist bei Raumtemperatur ein Gas und hat keinen Schmelzpunkt. Es kann bei niedrigen Temperaturen und hohen Drücken verflüssigt werden, liegt jedoch unter normalen Bedingungen nicht in festem Zustand vor.
Dichte von Ethylenoxid g/ml
Die Dichte von Epoxyethan beträgt 0,882 g/ml bei 20 °C (68 °F). Die Dichte ist die Masse einer Substanz pro Volumeneinheit und wird in Gramm pro Milliliter (g/ml) oder Kilogramm pro Kubikmeter (kg/m³) ausgedrückt. Die Dichte von Epoxyethan ist geringer als die von Wasser, was bedeutet, dass es auf der Wasseroberfläche schwimmt.
Epoxyethan-Formel
Die chemische Formel für Epoxyethan lautet C2H4O. Die Formel gibt die Anzahl und Art der in einem Molekül der Verbindung vorhandenen Atome an. In Epoxyethan gibt es zwei Kohlenstoffatome, vier Wasserstoffatome und ein Sauerstoffatom. Die Formel für Ethylenoxid ist für viele chemische Berechnungen wichtig, beispielsweise für den Ausgleich chemischer Gleichungen und die Bestimmung des Molekulargewichts der Verbindung.
| Aussehen | Farbloses Gas |
| Spezifisches Gewicht | 0,882 (20°C) |
| Farbe | Farblos |
| Geruch | Weich, wie Äther |
| Molmasse | 44,05 g/Mol |
| Dichte | 0,882 g/ml bei 20 °C |
| Fusionspunkt | N / A |
| Siedepunkt | 10,4 °C (50,7 °F) |
| Blitzpunkt | -18°C (-0,4°F) |
| Löslichkeit in Wasser | Vollständig löslich |
| Löslichkeit | Löslich in den meisten organischen Lösungsmitteln |
| Dampfdruck | 1075 mmHg (20 °C) |
| Wasserdampfdichte | 1,52 (Luft = 1) |
| pKa | 11.6 |
| pH-Wert | 7 (neutral) |
Sicherheit und Gefahren von Ethylenoxid
Epoxyethan (C2H4O) ist ein leicht entzündliches und reaktives Gas, das mehrere Sicherheits- und Gesundheitsrisiken birgt. Es kann zu Haut- und Augenreizungen, Atemproblemen und neurologischen Auswirkungen führen. C2H4O ist ebenfalls ein bekanntes Karzinogen und eine längere Exposition kann zu einem erhöhten Krebsrisiko führen. Daher sollten bei der Handhabung oder Arbeit mit C2H4O entsprechende Vorsichtsmaßnahmen getroffen werden, einschließlich des Tragens persönlicher Schutzausrüstung, der Gewährleistung einer ausreichenden Belüftung und der Einhaltung sicherer Lagerungs- und Handhabungsverfahren. Bei Exposition sollte sofort ein Arzt aufgesucht werden und je nach Schwere der Symptome Erste Hilfe geleistet werden.
| Gefahrensymbole | Totenkopf, Flamme |
| Sicherheitsbeschreibung | Leicht entzündlich, giftig, krebserregend, ätzend |
| UN-Identifikationsnummern | UN 1040 |
| HS-Code | 2909.11.00 |
| Gefahrenklasse | 2.3 (Brennbares Gas) |
| Verpackungsgruppe | ICH |
| Toxizität | Sehr giftig und krebserregend |
Methoden zur Synthese von Ethylenoxid
Ethylenoxid kann auf verschiedene Weise synthetisiert werden. Eine der gebräuchlichsten Methoden ist die katalytische Oxidation von Ethylen mit Luft oder Sauerstoff. Bei diesem Verfahren wird Ethylen bei hohen Temperaturen (200–300 °C) und Drücken (1–2 atm) über einen Silber- oder Goldkatalysator geleitet. Bei der Reaktion entstehen als Nebenprodukte Ethylenoxid und Wasser.
Eine andere Methode ist das Chlorhydrin-Verfahren, bei dem Ethylen mit Chlor und Wasser zu Ethylenchlorhydrin reagiert, das dann hydrolysiert wird, um Ethylenoxid und Salzsäure zu erzeugen. Aufgrund von Umweltbedenken im Zusammenhang mit der Verwendung von Chlor ist diese Methode weniger verbreitet.
Eine andere Methode beinhaltet die direkte Epoxidierung von Ethylen unter Verwendung organischer Peroxide oder Peroxysäuren. Diese Methode erfordert hohe Temperaturen und Drücke und ist aufgrund von Sicherheitsbedenken im Zusammenhang mit der Verwendung hochreaktiver und explosiver Reagenzien weniger verbreitet.
Kürzlich wurden neue Methoden zur Synthese von Ethylenoxid entwickelt, beispielsweise die elektrochemische Umwandlung von Ethylen mithilfe einer Festoxid-Elektrolysezelle. Diese Methode befindet sich noch im experimentellen Stadium, verspricht jedoch eine Verringerung der Umweltbelastung und eine Steigerung der Effizienz der Ethylenoxidproduktion.
Verwendung von Ethylenoxid
Ethylenoxid hat verschiedene industrielle und kommerzielle Anwendungen.
- C2H4O spielt eine entscheidende Rolle bei der Herstellung von Ethylenglykol, das in verschiedenen Industriezweigen als Kühlmittel und Frostschutzmittel verwendet wird.
- Die Fähigkeit der Verbindung, Mikroorganismen, darunter Bakterien, Viren und Pilze, zu durchdringen und abzutöten, macht sie zu einem wertvollen Sterilisationsmittel für medizinische Geräte und Hilfsmittel.
- C2H4O dient als Rohstoff bei der Herstellung von Ethoxylaten, die als Emulgatoren, Netzmittel und Dispergiermittel bei der Herstellung von Tensiden und Waschmitteln fungieren.
- Die Verbindung ist auch bei der Herstellung von Polyurethanschäumen und -kunststoffen sowie bei der Synthese verschiedener Chemikalien wie Ethanolamine, Glykolether und Fettsäureester nützlich.
- C2H4O findet Anwendung bei der Herstellung von Textilien, Klebstoffen und Beschichtungen sowie bei der Gewinnung von Naturprodukten wie Ölen und Aromen.
- C2H4O ist ein Begasungsmittel, das bei der Bekämpfung von Schädlingen und Insekten in Getreide und anderen Lebensmitteln hilft.
Insgesamt verfügt C2H4O aufgrund seiner Fähigkeit, mit verschiedenen Verbindungen zu reagieren, sowie seiner hohen Reaktivität und Vielseitigkeit über ein breites Anwendungsspektrum. Allerdings erfordert die Verwendung von Ethylenoxid eine sorgfältige Abwägung von Sicherheit, Umweltauswirkungen und behördlichen Anforderungen, und es müssen geeignete Maßnahmen ergriffen werden, um eine sichere Handhabung, einen sicheren Transport und eine sichere Verteilung zu gewährleisten. Verwendung der Verbindung.
Fragen:
Ethylenoxid-Sterilisatoren?
Ethylenoxid-Sterilisatoren sind Geräte, die Ethylenoxidgas zum Sterilisieren medizinischer Geräte und Hilfsmittel verwenden. Diese Sterilisatoren funktionieren, indem sie Geräte oder Vorräte in einer versiegelten Kammer oder einem geschlossenen Raum Ethylenoxidgas aussetzen. Das Gas dringt in Verpackungen und Materialien ein und zerstört eventuell vorhandene Mikroorganismen.
Sterilisation mit Ethylenoxid?
Epoxidethan wird häufig zur Sterilisation im Gesundheitswesen verwendet. Aufgrund seiner Fähigkeit, Verpackungen und andere Materialien zu durchdringen, ist es besonders wirksam bei der Abtötung von Mikroorganismen, einschließlich Bakterien, Viren und Pilzen. Die Sterilisation mit Epoxidethan wird häufig für hitzeempfindliche medizinische Geräte und Verbrauchsmaterialien eingesetzt, die herkömmlichen Sterilisationsmethoden wie Autoklavieren oder Bestrahlung nicht standhalten.
Warum ist Ethylenoxid gefährlich?
Epoxidethan ist aufgrund seiner Entflammbarkeit, Reaktivität und Toxizität ein sehr gefährlicher Stoff. Es ist ein bekanntes Karzinogen und kann eine Reihe von gesundheitlichen Auswirkungen haben, darunter Haut- und Augenreizungen, Atemwegsprobleme und neurologische Auswirkungen. Eine längere Exposition gegenüber Epoxyethan kann das Krebsrisiko erhöhen. Darüber hinaus ist Epoxyethan leicht entzündlich und kann mit Luft explosive Gemische bilden. Daher sollten bei der Handhabung oder Arbeit mit Epoxyethan entsprechende Vorsichtsmaßnahmen getroffen werden, einschließlich des Tragens persönlicher Schutzausrüstung, der Gewährleistung einer ausreichenden Belüftung und der Einhaltung sicherer Lagerungs- und Handhabungsverfahren.
