Butan (C₄H₁₀) ist ein leicht entzündliches Kohlenwasserstoffgas. Aufgrund seiner effizienten Brenneigenschaften und seiner Tragbarkeit wird es häufig als Brennstoff für Feuerzeuge und Campingkocher verwendet.
| IUPAC-Name | Butan |
| Molekularformel | C₄H₁₀ |
| CAS-Nummer | 106-97-8 |
| Synonyme | n-Butan, Butylhydrid, Methylethylmethan, Diethyl |
| InChI | InChI=1S/C4H10/c1-3-4-2/h3-4H2.1-2H3 |
Eigenschaften von Butan
Butan-Formel
Die Formel für Butan lautet C₄H₁₀, was bedeutet, dass es aus vier Kohlenstoffatomen und zehn Wasserstoffatomen besteht. Die Formel liefert wertvolle Informationen über die chemische Zusammensetzung von Butan und ermöglicht es Wissenschaftlern, seine Eigenschaften und sein Verhalten zu untersuchen.
Molmasse von Butan
Die Molmasse von Butylhydrid kann durch Addition der Atommassen seiner Bestandteile berechnet werden. Für Butylhydrid (C₄H₁₀) beträgt die Molmasse etwa 58,12 Gramm pro Mol. Die Molmasse ist ein entscheidender Parameter in verschiedenen chemischen Berechnungen und spielt eine wichtige Rolle bei der Bestimmung der physikalischen und chemischen Eigenschaften von Butylhydrid.
Siedepunkt von Butan
Butylhydrid hat einen relativ niedrigen Siedepunkt von etwa -1 °C (30 °F). Das bedeutet, dass Butylhydrid bei oder oberhalb dieser Temperatur leicht von einer flüssigen Phase in eine Gasphase übergeht. Der niedrige Siedepunkt macht Butylhydrid zu einem idealen Brennstoff für Anwendungen wie Feuerzeuge und tragbare Campingkocher.
Butan-Schmelzpunkt
Der Schmelzpunkt von Butylhydrid liegt bei etwa -138,4 °C (-217,12 °F). Bei oder unterhalb dieser Temperatur erfährt festes Butylhydrid einen Phasenwechsel und wird flüssig. Unter normalen atmosphärischen Bedingungen kommt Butylhydrid jedoch häufig in gasförmiger Form vor.
Butandichte g/ml
Die Dichte von Butylhydrid beträgt etwa 2,48 Gramm pro Milliliter. Dies weist darauf hin, dass Butylhydrid leichter ist als Wasser, das eine Dichte von 1 g/ml hat. Die Dichte von Butylhydrid ist eine entscheidende Eigenschaft, die sein Verhalten bei Lagerung oder Transport sowie seine Verbrennungseigenschaften bestimmt.
Molekulargewicht von Butan
Das Molekulargewicht von Butylhydrid beträgt etwa 58,12 Gramm pro Mol. Es stellt die Summe der Atomgewichte aller Atome in einem einzelnen Butylhydridmolekül dar. Das Molekulargewicht ist ein wesentlicher Parameter für verschiedene wissenschaftliche Berechnungen und hilft, die Eigenschaften und das Verhalten von Butylhydrid zu verstehen.
Struktur von Butan
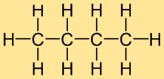
Die Struktur von Butylhydrid besteht aus einer geraden Kette von vier Kohlenstoffatomen, an die zehn Wasserstoffatome gebunden sind. Die Kohlenstoffatome sind in einer durchgehenden Linie angeordnet und jedes Kohlenstoffatom bildet Einfachbindungen mit zwei benachbarten Kohlenstoffatomen und drei Wasserstoffatomen. Diese lineare Struktur trägt zu den physikalischen und chemischen Eigenschaften von Butylhydrid bei.
Löslichkeit von Butan
Butylhydrid gilt als relativ wasserunlöslich. Aufgrund seiner unpolaren Natur und schwachen intermolekularen Wechselwirkungen mit Wassermolekülen weist es eine geringe Löslichkeit auf. Butylhydrid ist jedoch in organischen Lösungsmitteln wie Ethanol und Aceton gut löslich. Dieses Löslichkeitsverhalten ist in verschiedenen Anwendungen wichtig, beispielsweise bei Extraktionsprozessen und lösungsmittelbasierten Reaktionen.
| Aussehen | Farbloses Gas |
| Spezifisches Gewicht | 2,48 |
| Farbe | N / A |
| Geruch | Geruchlos |
| Molmasse | 58,12 g/Mol |
| Dichte | 2,48 g/ml |
| Fusionspunkt | -138,4°C (-217,12°F) |
| Siedepunkt | -1°C (30°F) |
| Blitzpunkt | -60 °C (-76 °F) |
| Löslichkeit in Wasser | Unlöslich |
| Löslichkeit | Löslich in organischen Lösungsmitteln |
| Dampfdruck | 2,4 Geldautomaten bei 20°C |
| Wasserdampfdichte | 2,07 (Luft = 1) |
| pKa | N / A |
| pH-Wert | N / A |
Sicherheit und Gefahren von Butan
Butylhydrid birgt bestimmte Sicherheitsrisiken, die berücksichtigt werden müssen. Es ist ein leicht entzündliches Gas und kann sich in Gegenwart einer Zündquelle leicht entzünden. Es sollten Vorkehrungen getroffen werden, um unbeabsichtigte Brände oder Explosionen zu vermeiden. Es ist wichtig, Butylhydrid in gut belüfteten Bereichen zu lagern und zu handhaben, um die Ansammlung brennbarer Dämpfe zu vermeiden. Das direkte Einatmen von Butylhydrid kann schädlich sein, da es Sauerstoff verdrängt und zum Ersticken führen kann. Darüber hinaus kann die Exposition gegenüber hohen Konzentrationen von Butylhydrid Schwindel, Schläfrigkeit und Übelkeit verursachen. Es ist wichtig, die richtigen Sicherheitsvorkehrungen zu befolgen, wie z. B. die Verwendung von Butylhydrid in ordnungsgemäß konstruierten und zugelassenen Geräten und die Vermeidung des Kontakts mit offenen Flammen oder Funken.
| Gefahrensymbole | Brennbares Gas |
| Sicherheitsbeschreibung | Von offenen Flammen und Funken fernhalten. An einem gut belüfteten Ort aufbewahren. Einatmen und direkten Kontakt vermeiden. |
| Identifikatoren der Vereinten Nationen | UN 1011 |
| HS-Code | 2711.12.20 |
| Gefahrenklasse | Klasse 2.1 (brennbares Gas) |
| Verpackungsgruppe | Verpackungsgruppe II |
| Toxizität | Butylhydrid gilt allgemein als wenig toxisch. Allerdings kann das Einatmen hoher Konzentrationen zu Schwindel, Schläfrigkeit und Übelkeit führen. Es kann auch in geschlossenen Räumen Sauerstoff verdrängen und zur Erstickung führen. Um die Sicherheit zu gewährleisten, müssen ordnungsgemäße Belüftungs- und Handhabungsverfahren befolgt werden. |
Butan-Synthesemethoden
Zur Synthese von Butylhydrid gibt es verschiedene Methoden, vor allem bei der Produktion von Erdöl oder Erdgas.
Fraktionierte Destillation: Bei der fraktionierten Destillation von Rohöl oder Erdöl entsteht als Nebenprodukt Butylhydrid. Beim Raffinierungsprozess werden verschiedene Kohlenwasserstofffraktionen anhand ihrer Siedepunkte getrennt, und Butylhydrid ist eine der Komponenten, die isoliert werden können.
Erdgasverarbeitung: Bei der Erdgasverarbeitung entsteht auch Butylhydrid. Erdgas enthält verschiedene Kohlenwasserstoffe, darunter Methan und höhere Kohlenwasserstoffe wie Butylhydrid. Das Erdgasgemisch durchläuft Prozesse wie Absorption oder kryogene Trennung, um das Butylhydrid abzutrennen.
Kohlenwasserstoffcracken: Beim Crackprozess werden größere Kohlenwasserstoffketten in kleinere Ketten zerlegt, wodurch Butylhydrid entsteht. Dabei werden schwerere Kohlenwasserstoffe hohen Temperaturen ausgesetzt oder Katalysatoren eingesetzt, um Butylhydrid als Produkt zu erzeugen.
Isomerisierung: Die Isomerisierung ordnet die Molekülstruktur von Kohlenwasserstoffen neu und ermöglicht die Synthese von Butylhydrid durch Isomerisierung anderer Kohlenwasserstoffe wie Pentan oder Hexan in ihre Isomere. Spezielle Katalysatoren katalysieren diesen Prozess unter geeigneten Bedingungen.
Syntheseprozess: Im Labor können Wissenschaftler Butylhydrid auf synthetischen Wegen synthetisieren. Sie können verschiedene chemische Reaktionen wie Hydrierung oder Reduktion nutzen, um Butylhydrid aus Vorläuferverbindungen herzustellen.
Diese Methoden ermöglichen die Herstellung von Butylhydrid sowohl in großtechnischen Prozessen als auch in kleineren Laboren. Die Wahl der Methode hängt von der Verfügbarkeit der Rohstoffe, der gewünschten Reinheit und den spezifischen Anforderungen der Anwendung ab.
Verwendung von Butan
Aufgrund seiner vorteilhaften Eigenschaften findet Butylhydrid in verschiedenen Branchen und im täglichen Gebrauch Anwendung. Hier sind einige häufige Verwendungszwecke für Butylhydrid:
- Brennstoff: Butylhydrid dient dank seines hohen Energiegehalts und seiner effizienten Verbrennungseigenschaften als Brennstoff für tragbare Kocher, Campingöfen und Feuerzeuge.
- Aerosol-Treibmittel: Butylhydrid treibt Aerosolprodukte wie Haarsprays, Lufterfrischer und Aerosolfarben an, sodass sie als feiner Nebel oder Spray freigesetzt werden können.
- Kältemittel: Butylhydrid kühlt und hält niedrige Temperaturen in kleinen Kühlsystemen wie Haushaltskühlschränken und Gefrierschränken aufrecht und dient als Kältemittel.
- Feuerzeugflüssigkeit: Butylhydrid treibt Zigarettenanzünder und Taschenlampen an und erzeugt eine Flamme, die ein wichtiger Bestandteil von Feuerzeugflüssigkeiten ist.
- Extraktion: Butylhydrid fungiert als Lösungsmittel bei der Extraktion ätherischer Öle und Pflanzenstoffe aus pflanzlichen Materialien und löst die gewünschten Verbindungen effektiv auf.
- Verwendung im Labor: Labore verwenden Butylhydrid als Brennstoff für Bunsenbrenner und Gaschromatographie.
- Kalibriergas: Butylhydrid dient als Kalibriergas für Gasdetektoren und Sensoren und sorgt für genau definierte und leicht messbare Eigenschaften.
- Schweißen und Löten: Butylhydrid-Brenner erleichtern Schweiß- und Lötarbeiten dank ihrer hohen Temperaturen, Präzision und Benutzerfreundlichkeit.
- Freizeit: Butylhydrid versorgt tragbare Campingkocher und Taschenlampen mit Strom und verbessert so Freizeitaktivitäten im Freien wie Camping, Wandern und Kochen.
- Verbrauchsquelle: Butylhydrid dient als Wärmequelle in einer Vielzahl von Anwendungen, einschließlich Heizwerkzeugen, kleinen Heizgeräten und flammenbasierten Anwendungen in bestimmten Branchen.
Die Vielseitigkeit von Butylhydrid und sein Anwendungsspektrum machen es zu einer wertvollen Verbindung in verschiedenen Branchen, Haushaltsartikeln und Freizeitaktivitäten.
Frage:
F: Wo kann ich in meiner Nähe Butangas kaufen?
A: Normalerweise finden Sie Butylhydridgas in örtlichen Baumärkten, Supermärkten oder Convenience-Stores, die Campingbedarf verkaufen.
F: Ist Butangas Erdgas?
A: Nein, Butylhydrid gilt nicht als Erdgas. Es handelt sich um ein Kohlenwasserstoffgas, das bei der Verarbeitung von Erdöl oder Erdgas gewonnen wird.
F: Was ist Butan?
A: Butylhydrid ist ein gasförmiger Kohlenwasserstoff mit der chemischen Formel C₄H₁₀. Es ist ein farb- und geruchloses brennbares Gas, das häufig als Brennstoff und für verschiedene Anwendungen verwendet wird.
F: Wie wird Butan hergestellt?
A: Butylhydrid wird hauptsächlich durch Prozesse wie fraktionierte Destillation von Erdöl oder Erdgas, Cracken schwererer Kohlenwasserstoffe oder Isomerisierung anderer Kohlenwasserstoffe hergestellt.
F: Wie fülle ich ein Butanfeuerzeug nach?
A: Um ein Butylhydrid-Feuerzeug zu füllen, suchen Sie zunächst nach dem Nachfüllventil, normalerweise unten. Führen Sie die Butylhydrid-Düse in das Ventil ein und drücken Sie fest darauf, um das Butylhydrid in das Lumen freizusetzen, bis es voll ist.
F: Welche der folgenden Verbindungen ist ein Strukturisomer von Butan?
A: Pentan (C₅H₁₂) ist ein Strukturisomer von Butylhydrid, da beide Verbindungen vier Kohlenstoffatome enthalten, aber unterschiedliche Anordnungen haben.
F: Wie fülle ich ein Butanfeuerzeug nach?
A: Um ein Butylhydrid-Feuerzeug nachzufüllen, halten Sie das Feuerzeug verkehrt herum, richten Sie die Düse der Butylhydrid-Nachfüllkartusche auf das Nachfüllventil des Feuerzeugs aus und drücken Sie fest auf die Kartusche, um das Hydrid aus Butyl in das Feuerzeug freizusetzen.
F: Wo kann ich Butan in meiner Nähe kaufen?
A: Sie können Butylhydrid in örtlichen Baumärkten, Supermärkten oder Convenience-Stores kaufen, die Campingbedarf oder Haushaltsartikel führen.
F: Wo kann man Butan kaufen?
A: Butylhydrid kann aus verschiedenen Quellen bezogen werden, darunter Online-Händler, Baumärkte, Campingbedarfsgeschäfte und einige Supermärkte.
F: Welche Aussage vergleicht den Schmelzpunkt von Butan (C₄H₁₀) am besten mit dem von Oktan (C₈H₁₈)?
A: Oktan hat aufgrund seiner größeren und komplexeren Molekülstruktur im Allgemeinen einen höheren Schmelzpunkt als Butylhydrid.
F: Wie groß ist die Molmasse von Butan, C₄H₁₀?
A: Die Molmasse von Butylhydrid (C₄H₁₀) beträgt etwa 58,12 Gramm pro Mol.
F: Wie viele Isomere sind für C₄H₁₀ möglich?
A: Butylhydrid (C₄H₁₀) hat zwei Isomere: n-Butan (normales Butan) und Isobutan (2-Methylpropan).
F: Welche der Verbindungen C₄H₁₀, SrCl₂, Cr(NO₃)₃, OF₂ sollten als Moleküle existieren?
A: Es wird erwartet, dass C₄H₁₀ (Butylhydrid) und OF₂ (Sauerstoffdifluorid) als Moleküle vorliegen, während SrCl₂ und Cr(NO₃)₃ ionische Verbindungen sind.
